Пиперидин - Piperidine
| |||
 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Пиперидин[2] | |||
| Другие имена Гексагидропиридин Азациклогексан Пентаметиленамин Азинан | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.467 | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| |||
| |||
| Характеристики | |||
| C5ЧАС11N | |||
| Молярная масса | 85.150 г · моль−1 | ||
| Внешность | Бесцветная жидкость | ||
| Запах | Подобный семени[3], ихтисовый, аммиачный, острый | ||
| Плотность | 0,862 г / мл | ||
| Температура плавления | -7 ° С (19 ° F, 266 К) | ||
| Точка кипения | 106 ° С (223 ° F, 379 К) | ||
| Смешиваемый | |||
| Кислотность (пKа) | 11.22[4][5] | ||
| -64.2·10−6 см3/ моль | |||
| Вязкость | 1.573 cP при 25 ° C | ||
| Опасности | |||
| Паспорт безопасности | MSDS1,MSDS2 | ||
Классификация ЕС (DSD) (устарело) | Легковоспламеняющийся (F) Токсичный (Т) | ||
| R-фразы (устарело) | R11, R23 / 24, R34 | ||
| NFPA 704 (огненный алмаз) | |||
| Родственные соединения | |||
Родственные соединения | Пиридин Пирролидин Пиперазин | ||
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
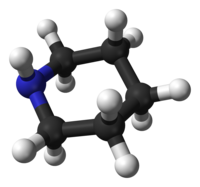
Пиперидин является органическое соединение с молекулярной формулой (CH2)5NH. Этот гетероциклический амин состоит из шестичленного кольца, содержащего пять метиленовые мостики (–CH2-) и один аминный мостик (–NH–). Это бесцветная жидкость с неприятным запахом, типичным для амины.[6] Название происходит от названия рода Пайпер, что на латыни означает перец.[7] Хотя пиперидин является распространенным органическим соединением, он наиболее известен как типичный структурный элемент во многих фармацевтических и алкалоиды, например, встречающиеся в природе соленопсины.[8]
Производство
О пиперидине впервые сообщил в 1850 году шотландский химик. Томас Андерсон и снова, независимо, в 1852 году французский химик Огюст Кахур, который назвал это.[9][10][11] Оба мужчины получили пиперидин в результате реакции пиперин с азотной кислотой.
Промышленно пиперидин производится гидрирование из пиридин, обычно более дисульфид молибдена катализатор:[12]
- C5ЧАС5N + 3 H2 → С5ЧАС10NH
Пиридин также может быть восстановлен до пиперидина посредством модифицированного Сокращение березы с помощью натрий в этиловый спирт.[13]
Естественное появление пиперидина и производных
Сам пиперидин был получен из черный перец,[14][15] из Псилокаулон абсимил (Aizoaceae ),[16] И в Петросимония монандра.[17]
Структурный мотив пиперидина присутствует во многих природных алкалоиды. К ним относятся пиперин, который дает черный перец его пряный вкус. Это дало составу название. Другими примерами являются огненный муравей токсин соленопсин,[18] то никотин аналог анабазин древесного табака (Никотиана глаука ), лобелин из Индийский табак, и токсичный алкалоид Coniine из яд болиголов, который использовался для Сократ до смерти.[19]
Конформация
Пиперидин предпочитает конформация стула, похожий на циклогексан. В отличие от циклогексана, пиперидин имеет две различные конформации кресла: одна со связью N – H в осевое положение, а другой в экваториальном положении. После долгих споров в 1950–1970-х годах было обнаружено, что экваториальная конформация более стабильна на 0,72 ккал / моль в газовой фазе.[20] В неполярные растворители был оценен диапазон от 0,2 до 0,6 ккал / моль, но в полярных растворителях аксиальный конформер может быть более стабильным.[21] Два конформера быстро преобразуются через азотная инверсия; свободная энергия активационный барьер для этого процесса, оцениваемое в 6,1 ккал / моль, значительно ниже, чем 10,4 ккал / моль для инверсия кольца.[22] В случае N-метилпиперидин, экваториальная конформация предпочтительнее 3,16 ккал / моль,[20] что намного больше, чем предпочтение в метилциклогексан, 1,74 ккал / моль.
 |  |
Реакции
Пиперидин широко используется для превращения кетоны к енамины.[23] Енамины, полученные из пиперидина, являются субстратами в Алкилирование енамином аиста реакция.[24]
При лечении гипохлорит кальция, пиперидин превращается в N-хлорпиперидин, а хлорамин с формулой C5ЧАС10NCl. Образующийся хлорамин подвергается дегидрогалогенирование чтобы предоставить циклический имин.[25]
Химические сдвиги ЯМР
- 13C ЯМР: (CDCl3, м.д.) 47,2 7,2, 25,2[нужна цитата ]
- 1H ЯМР: (CDCl3, частей на миллион) 2,79, 2,19, 1,51[нужна цитата ]
Использует
Пиперидин используется как растворитель и как основание. То же верно и для некоторых производных: N-формилпиперидин это полярный апротонный растворитель с лучшей растворимостью в углеводородах, чем другие амидные растворители, и 2,2,6,6-тетраметилпиперидин очень стерически затрудненный база, полезная из-за низкого нуклеофильность и высокая растворимость в органические растворители.
Существенное промышленное применение пиперидина - производство дипиперидинилдитиурамтетрасульфида, который используется в качестве ускорителя вулканизация серы резины.[12]
Список лекарств пиперидина
Пиперидин и его производные являются стандартными строительными блоками в фармацевтических препаратах.[26] и тонкие химикаты. Структура пиперидина встречается, например, в:
- Икаридин (Средство от насекомых)
- СИОЗС (селективные ингибиторы обратного захвата серотонина )
- стимуляторы и ноотропы:
- SERM (селективные модуляторы рецепторов эстрогена )
- Вазодилататоры
- Нейролептики лекарства:
- Опиоиды:
- Арилциклогексиламины:
- PCP и аналоги
- холинолитик химическое оружие
- Дитран
- N-Метил-3-пиперидил бензилат (JB-336, БЖ)
Пиперидин также обычно используется в реакциях химического разложения, таких как определение последовательности ДНК в расщеплении конкретных модифицированных нуклеотиды. Пиперидин также обычно используется в качестве основы для снятие защиты из Fmoc -аминокислоты используется в твердой фазе пептидный синтез.
Пиперидин указан как прекурсор Таблицы II под Конвенция Организации Объединенных Наций о борьбе с незаконным оборотом наркотических средств и психотропных веществ из-за его использования (пик в 1970-х годах) в подпольном производстве PCP (1- (1-фенилциклогексил) пиперидин, также известный как ангельская пыль, шермы, влажные и т. Д.).[27]
Рекомендации
- ^ Международная карта химической безопасности 0317
- ^ «Переднее дело». Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга). Кембридж: Королевское химическое общество. 2014. с. 142. Дои:10.1039 / 9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ Амур, Дж. Э. (1975). «Специфическая аносмия к 1-пирролину: первичный запах спермы». J. Chem. Ecol. 1 (3): 299–310. Дои:10.1007 / BF00988831. S2CID 19318345.
- ^ Холл, Х. К. (1957). «Соотношение основных сильных сторон аминов». Варенье. Chem. Soc. 79 (20): 5441–5444. Дои:10.1021 / ja01577a030.
- ^ пKа значение пиперидиния (протонированного пиперидина), соответствующее pKб значение 2,78 для пиперидина.
- ^ Фрэнк Джонсон Велчер (1947). Органические аналитические реагенты. Д. Ван Ностранд. п.149.
- ^ Сеннинг, Александр (2006). Словарь химиоэтимологии Elsevier. Амстердам: Эльзевир. ISBN 978-0-444-52239-9.
- ^ Пианаро, Адриана; Фокс, Эдуардо Г.П .; Bueno, Odair C .; Марсайоли, Анита Дж. (Май 2012 г.). «Экспресс-анализ конфигурации соленопсинов». Тетраэдр: асимметрия. 23 (9): 635–642. Дои:10.1016 / j.tetasy.2012.05.005.
- ^ Варнхофф, Эдгар В. (1998). «Когда пиперидин был структурной проблемой» (PDF). Вестник истории химии. 22: 29–34.

- ^ Андерсон, Томас (1850). "Vorläufiger Bericht über die Wirkung der Salpetersäure auf organische Alkalien" [Предварительный отчет о влиянии азотной кислоты на органические щелочи]. Annalen der Chemie und Pharmacie. 75: 80–83. Дои:10.1002 / jlac.18500750110.

- ^ Каур, Огюст (1852). "Recherches sur un nouvel alcali dérivé de la pipérine" [Исследования новой щелочи на основе пиперина]. Comptes Rendus. 34: 481–484.
L'alcali nouveau dérivé de la pipérine, que je désignerai sous le nom de 'pipéridine',… (Новая щелочь, полученная из пиперина, которую я назову «пиперидин»,…

- ^ а б Эллер, Карстен; Хенкес, Эрхард; Россбахер, Роланд; Хёке, Хартмут. «Амины алифатические». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a02_001.
- ^ Marvel, C. S .; Лазье, В. А. (1929). «Бензоилпиперидин». Орг. Синтезатор. 9: 16. Дои:10.15227 / orgsyn.009.0016.
- ^ Späth; Englaender (1935). "Über das Vorkommen von Piperidin im schwarzen Pfeffer". Chemische Berichte. 68 (12): 2218–2221. Дои:10.1002 / cber.19350681211.
- ^ Пикте, Аме; Пикте, Рене (1927). "Sur l'alcaloïde volatil du poivre". Helvetica Chimica Acta. 10: 593–595. Дои:10.1002 / hlca.19270100175.
- ^ Римингтон, Клод (1934). "Псилокаулон абсимил N.E.Br. как базовый яд ». Южноафриканский научный журнал. 31: 184–193. HDL:10520 / AJA00382353_6425.
- ^ Юращевский; Степанов (1939). J. Gen. Chem. СССР. 9: 1687. Отсутствует или пусто
| название =(помощь) - ^ Arbiser, J. L .; Кау, Т .; Конар, М .; и другие. (2007). «Соленопсин, алкалоидный компонент огненного муравья (Solenopsis invicta), представляет собой встречающийся в природе ингибитор передачи сигналов фосфатидилинозитол-3-киназы и ангиогенеза ». Кровь. 109 (2): 560–5. Дои:10.1182 / кровь-2006-06-029934. ЧВК 1785094. PMID 16990598.
- ^ Томас Андерсон Генри (1949). Алкалоиды растений (4-е изд.). Компания Блейкистон.
- ^ а б Карбаллейра, Луис; Перес Хусте, Игнасио (1998). «Влияние уровня расчета и эффект метилирования на аксиальное / экваториальное равновесие в пиперидинах». Журнал вычислительной химии. 19 (8): 961–976. Дои:10.1002 / (SICI) 1096-987X (199806) 19: 8 <961 :: AID-JCC14> 3.0.CO; 2-A.
- ^ Блэкберн, Ян Д.; Катрицки, Алан Р .; Ёсито Такеучи (1975). «Конформация пиперидина и его производных с дополнительными кольцевыми гетероатомами». Соотв. Chem. Res. 8 (9): 300–306. Дои:10.1021 / ar50093a003.
- ^ Anet, F. A. L .; Явари, Исса (1977). «Азотная инверсия в пиперидине». Варенье. Chem. Soc. 99 (8): 2794–2796. Дои:10.1021 / ja00450a064.
- ^ Kane, Vinayak V .; Джонс, Мейтленд младший (1990). «Спиро [5.7] тридека-1,4-диен-3-он». Органический синтез.; Коллективный объем, 7, п. 473
- ^ Смит, Майкл Б .; Март, Джерри (2001). Мартовская продвинутая органическая химия: реакции, механизмы и структура (5-е изд.). Wiley-Interscience. ISBN 978-0-471-58589-3.
- ^ Claxton, Джордж П .; Аллен, Ллойд; Гризар, Дж. Мартин (1977). «Тример 2,3,4,5-тетрагидропиридина». Органический синтез. 56: 118. Дои:10.15227 / orgsyn.056.0118.
- ^ Витаку, Э., Д. Т. Смит и Дж. Т. Нджардарсон (2014). «Анализ структурного разнообразия, моделей замещения и частоты гетероциклов азота среди фармацевтических препаратов, одобренных FDA США». Журнал медицинской химии. 57 (24): 10257–10274. Дои:10.1021 / jm501100b. PMID 25255204.CS1 maint: использует параметр авторов (связь)
- ^ «Список прекурсоров и химических веществ, часто используемых при незаконном изготовлении наркотических средств и психотропных веществ, находящихся под международным контролем» (PDF). Международный комитет по контролю над наркотиками. Архивировано из оригинал (PDF) на 27 февраля 2008 г.
внешняя ссылка
 СМИ, связанные с Пиперидин в Wikimedia Commons
СМИ, связанные с Пиперидин в Wikimedia Commons



