Метан - Methane
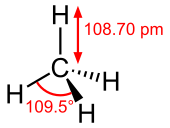 | |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Метан[1] | |||
| Систематическое название ИЮПАК Карбон (никогда не рекомендуется[1]) | |||
Другие имена
| |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| 3DMet | |||
| 1718732 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.739 | ||
| Номер ЕС |
| ||
| 59 | |||
| КЕГГ | |||
| MeSH | Метан | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1971 | ||
| |||
| Характеристики | |||
| CЧАС4 | |||
| Молярная масса | 16.043 г · моль−1 | ||
| Внешность | Бесцветный газ | ||
| Запах | Без запаха | ||
| Плотность |
| ||
| Температура плавления | -182,5 ° С; -296,4 ° F; 90,7 тыс. | ||
| Точка кипения | -161,50 ° С; -258,70 ° F; 111,65 К[3] | ||
| Критическая точка (Т, п) | 190,56 К, 4,5992 МПа | ||
| 22.7 мг · л−1 | |||
| Растворимость | Растворим в этиловый спирт, диэтиловый эфир, бензол, толуол, метанол, ацетон и нерастворим в воде | ||
| бревно п | 1.09 | ||
Закон Генри постоянный (kЧАС) | 14 нмоль · Па−1·кг−1 | ||
| Конъюгированная кислота | Метан | ||
| Основание конъюгата | Метил анион | ||
| −12.2×10−6 см3· Моль−1 | |||
| Структура | |||
| Тd | |||
| Тетраэдр | |||
| 0 D | |||
| Термохимия | |||
Теплоемкость (C) | 35.69 Дж · (К · моль)−1 | ||
Стандартный моляр энтропия (S | 186.25 Дж · (К · моль)−1 | ||
Станд. Энтальпия формирование (ΔжЧАС⦵298) | −74.87 кДж · моль−1 | ||
Станд. Энтальпия горение (ΔcЧАС⦵298) | От -891,1 до -890,3 кДж · моль−1 | ||
| Опасности[4] | |||
| Паспорт безопасности | Видеть: страница данных | ||
| Пиктограммы GHS |  | ||
| Сигнальное слово GHS | Опасность | ||
| H220 | |||
| P210 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | -188 ° С (-306,4 ° F, 85,1 К) | ||
| 537 ° С (999 ° F, 810 К) | |||
| Пределы взрываемости | 4.4–17% | ||
| Родственные соединения | |||
Родственные алканы | |||
| Страница дополнительных данных | |||
| Показатель преломления (п), Диэлектрическая постоянная (εр), так далее. | |||
Термодинамический данные | Фазовое поведение твердое тело – жидкость – газ | ||
| УФ, ИК, ЯМР, РС | |||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Метан (нас: /ˈмɛθeɪп/ или же Великобритания: /ˈмяθeɪп/) представляет собой химическое соединение с химическая формула CH4 (один атом углерод и четыре атома водород ). Это группа-14 гидрид и самый простой алкан, и является основным компонентом натуральный газ. Относительное содержание метана на земной шар делает его экономически привлекательным топливо, хотя его захват и хранение создает технические проблемы из-за его газообразный состояние под нормальные условия по температуре и давлению.
Природный метан находится как под землей, так и под землей. морское дно, и формируется как геологическими, так и биологическими процессами. Самый большой резервуар метана находится под морским дном в виде клатраты метана. Когда метан достигает поверхности и атмосфера, он известен как атмосферный метан.[6] Концентрация метана в атмосфере Земли увеличилось примерно на 150% с 1750 г., и составляет 20% от общего радиационное воздействие от всех долгоживущих и глобально смешанных парниковые газы.[7] Метан также был обнаружен на других планетах, в том числе Марс, что имеет значение для астробиология исследование.[8]
Свойства и связь
Метан - это четырехгранный молекула с четырьмя эквивалентами C – H связи. Его электронная структура описывается четырьмя связывающими молекулярными орбиталями (МО) в результате перекрытия валентных орбиталей на C и ЧАС. MO с наименьшей энергией является результатом перекрытия 2s-орбиталей на углероде с синфазной комбинацией 1s-орбиталей на четырех атомах водорода. Выше этого энергетического уровня находится тройной вырожденный набор МО, который включает перекрытие 2p-орбиталей на углероде с различными линейными комбинациями 1s-орбиталей на водороде. Полученная в результате схема соединения «три на один» согласуется с измерениями фотоэлектронной спектроскопии.
В комнатная температура и стандартное давление, метан - бесцветный газ без запаха.[9] Знакомый запах природного газа, который используется в домах, достигается добавлением одорант, обычно смеси, содержащие трет-бутилтиол, в качестве меры безопасности. Метан имеет температуру кипения −164 °C (−257.8 °F ) при давлении в один атмосфера.[10] Как газ это легковоспламеняющийся в диапазоне концентраций (5,4–17%) в воздухе при стандартное давление.
Твердый метан существует в нескольких модификации. В настоящее время известно девять.[11] Охлаждение метана при нормальном давлении приводит к образованию метана I. Это вещество кристаллизуется в кубической системе (космическая группа FM3м). Положение атомов водорода в метане I не фиксировано, т.е. молекулы метана могут свободно вращаться. Следовательно, это пластиковый кристалл.[12]
Химические реакции
Основные химические реакции метана: горение, паровой риформинг к синтез-газ, и галогенирование. В общем, реакции с метаном трудно контролировать.
Селективное окисление
Частичное окисление метана в метанол сложно, потому что реакция обычно прогрессирует до углекислый газ и воды даже при недостаточном количестве кислород. В фермент метанмонооксигеназа производит метанол из метана, но не может использоваться для реакций промышленного масштаба.[13] Некоторые однородно катализированный системы и гетерогенные системы были разработаны, но все они имеют существенные недостатки. Обычно они работают, производя защищенные продукты, защищенные от переокисления. Примеры включают Каталитическая система, медь цеолиты, и железные цеолиты, стабилизирующие альфа-кислород активный сайт.[14]
Одна группа бактерии управлять окислением метана с помощью нитрит как окислитель в отсутствие кислород, вызывая так называемые анаэробное окисление метана.[15]
Кислотно-основные реакции
Как и другие углеводороды, метан очень слабая кислота. Его pKа в ДМСО оценивается в 56.[16] Не может быть депротонированный в растворе, но сопряженное основание известен в таких формах, как метиллитий.
Разнообразие положительные ионы полученные из метана, наблюдались в основном как нестабильные частицы в газовых смесях низкого давления. К ним относятся метений или метильный катион CH+
3, катион метана CH+
4, и метаний или протонированный метан CH+
5. Некоторые из них были обнаружен в космическом пространстве. Метан также может быть получен в виде разбавленных растворов из метана с суперкислоты. Катионы с более высоким зарядом, например CH2+
6 и CH3+
7, были изучены теоретически и предположительно устойчивы.[17]
Несмотря на прочность связей C – H, существует большой интерес к катализаторы что облегчает Активация связи C – H в метане (и других алканы ).[18]
Горение

Метана теплота сгорания составляет 55,5 МДж / кг.[19] Горение метана представляет собой многостадийную реакцию, резюмируемую следующим образом:
Четырехступенчатая химия Петерса представляет собой систематически сокращенную четырехступенчатую химию, объясняющую горение метана.
Метановые радикальные реакции
В соответствующих условиях метан реагирует с галоген радикалы следующее:
- X • + CH4 → HX + CH3•
- CH3• + X2 → CH3X + X •
где X - это галоген: фтор (F), хлор (Cl), бром (Br), или йод (Я). Этот механизм для этого процесса называется свободнорадикальное галогенирование. Он инициируется, когда УФ-излучение или какой-то другой радикальный инициатор (подобно перекиси ) производит галоген атом. Двухступенчатый цепная реакция следует, в котором атом галогена отрывает атом водорода от молекулы метана, в результате чего образуется галогенид водорода молекула и метильный радикал (CH3•). Затем метильный радикал вступает в реакцию с молекулой галогена с образованием молекулы галогенметана с новым атомом галогена в качестве побочного продукта.[20] Подобные реакции могут происходить с галогенированным продуктом, приводя к замене дополнительных атомов водорода атомами галогена на дигалогенметан, тригалометан, и в конечном итоге тетрагалогенметан структуры, в зависимости от условий реакции и соотношения галогена и метана.
Использует
Метан используется в промышленных химических процессах и может транспортироваться в виде охлажденной жидкости (сжиженный природный газ или СПГ ). В то время как утечки из охлаждаемого контейнера для жидкости изначально тяжелее воздуха из-за повышенной плотности холодного газа, газ при температуре окружающей среды легче воздуха. Газопроводы распределяют большие объемы природного газа, основным компонентом которого является метан.
Топливо
Метан используется как топливо для печей, домов, водонагревателей, обжиговых печей, автомобилей,[21][22] турбины и прочее. Активированный уголь используется для хранения метана. Очищенный жидкий метан используется как а ракетное горючие,[23] в сочетании с жидкий кислород, как в BE-4 и Raptor двигатели.[24]
В качестве основной составляющей натуральный газ, метан важен для производство электроэнергии сжигая его как топливо в газовая турбина или же парогенератор. По сравнению с другими углеводородное топливо, метан производит меньше углекислый газ на каждую единицу выделяемого тепла. При примерно 891 кДж / моль метан теплота сгорания ниже, чем у любого другого углеводорода. Однако он выделяет больше тепла на массу (55,7 кДж / г), чем любая другая органическая молекула, из-за относительно большого содержания водорода, на который приходится 55% теплоты сгорания.[25] но составляет только 25% молекулярной массы метана. Во многих городах метан подается в дома для бытовых нужд. обогрев и приготовление пищи. В этом контексте он обычно известен как натуральный газ, который, как считается, имеет энергосодержание 39 мегаджоули за кубический метр, или 1000 БТЕ на стандартный кубический фут. Сжиженный природный газ (СПГ) преимущественно метан (CH4) переведены в жидкую форму для удобства хранения или транспортировки.
В качестве ракетного топлива метан имеет преимущество перед керосин производства небольших молекул выхлопных газов. Это вносит меньше сажа на внутренних частях ракетных двигателей, что снижает трудность повторного использования ускорителя. Нижний молекулярный вес выхлопа также увеличивает долю тепловой энергии, которая находится в форме кинетической энергии, доступной для движения, увеличивая удельный импульс ракеты. Жидкий метан также имеет диапазон температур (91–112 К), почти совместимый с жидкий кислород (54–90 К).
Химическое сырье
Натуральный газ, который в основном состоит из метана, используется для производства газообразного водорода в промышленных масштабах. Паровой риформинг метана (SMR), или просто известный как паровой риформинг, является наиболее распространенным методом производства промышленного газообразного водорода. Ежегодно во всем мире (2013 г.) добывается более 50 миллионов метрических тонн, в основном из SMR природного газа.[26] Большая часть этого водорода используется в нефть нефтеперерабатывающие заводы, в производстве химикатов и в пищевой промышленности. Очень большое количество водорода используется в промышленный синтез аммиака.
При высоких температурах (700 - 1100 ° C) и при наличии металл -основан катализатор (никель ), пар реагирует с метаном с образованием смеси CO и ЧАС2, известный как "водяной газ" или "синтетический газ":
Эта реакция сильно эндотермический (потребляет тепло, ΔHр= 206 кДж / моль). Дополнительный водород получают по реакции CO с водой через реакция конверсии водяного газа.
- CO + H2O ⇌ CO2 + H2
Эта реакция мягко говоря экзотермический (выделяет тепло, ΔHр= -41 кДж / моль).
Метан также подвержен свободнорадикальному хлорирование в производстве хлорметанов, хотя метанол является более типичным предшественником.[27]
Поколение
Геологические маршруты
Двумя основными путями геологического образования метана являются: (i) органический (генерируемый термически или термогенный) и (ii) неорганический (абиотический ).[8] Термогенный метан возникает из-за разрушения органических веществ при повышенных температурах и давлениях в глубоких осадочных породах. слои. Большая часть метана в осадочных бассейнах термогенная; Следовательно, термогенный метан является наиболее важным источником природного газа. Компоненты термогенного метана обычно считаются реликтовыми (более ранними). Как правило, образование термогенного метана (на глубине) может происходить в результате разрушения органических веществ или органического синтеза. Оба пути могут вовлекать микроорганизмы (метаногенез ), но может встречаться и неорганически. Соответствующие процессы также могут потреблять метан с микроорганизмами и без них.
Более важный источник метана на глубине (кристаллическая порода) - абиотический. Абиотический означает, что метан создается из неорганических соединений без биологической активности либо в результате магматических процессов, либо в результате реакций вода-порода, которые происходят при низких температурах и давлениях, например серпентинизация.[28][29]
Биологические маршруты
Большая часть метана на Земле биогенный и производится метаногенез,[30][31] форма анаэробного дыхания, которую, как известно, проводят только некоторые члены домена Археи.[32] Метаногены занимают свалки и другие почвы,[33] жвачные животные (Например коровы или же крупный рогатый скот ),[34] кишки термитов и аноксический отложения ниже морского дна и дна озер. Рис поля также производят большое количество метана во время роста растений.[35] Этот многоступенчатый процесс используется этими микроорганизмами для получения энергии. Чистая реакция метаногенеза:
- CO2 + 4 часа2→ CH4 + 2 часа2О
Последний этап процесса катализируется ферментом метил-кофермент М редуктаза (MCR).[36]

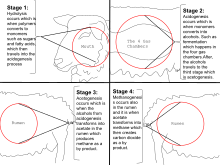
Жвачные животные
Жвачные животные, такие как крупный рогатый скот, отрыгивают метан, что составляет ~ 22% годовых выбросов метана в атмосферу в США.[37] Одно исследование показало, что сектор животноводства в целом (в основном крупный рогатый скот, куры и свиньи) производит 37% всего антропогенного метана.[38] Исследование 2013 года показало, что на домашний скот приходится 44% антропогенного метана и ~ 15% антропогенных выбросов парниковых газов.[39] В настоящее время предпринимаются многочисленные усилия по сокращению производства метана в животноводстве, например, лечение и корректировка рациона питания,[40] и улавливать газ для использования в качестве энергии.[41]
Отложения морского дна
Большая часть подпольного этажа аноксический потому что кислород удаляется аэробный микроорганизмы в пределах первых нескольких сантиметров осадка. Ниже насыщенного кислородом морского дна метаногены производят метан, который либо используется другими организмами, либо попадает в ловушку. газовые гидраты.[32] Эти другие организмы, которые используют метан для получения энергии, известны как метанотрофы (поедание метана), и являются основной причиной того, что мало метана, образующегося на глубине, достигает поверхности моря.[32] Консорциумы архей и бактерий окисляют метан через Анаэробное окисление метана (АОМ); организмы, ответственные за это, Анаэробные метанотрофные археи (ANME) и Сульфатредуцирующие бактерии (SRB).[42]
Промышленные маршруты
Стимулы к промышленному производству метана практически отсутствуют. Метан производится гидрогенизация углекислый газ через Сабатье процесс. Метан также является побочным продуктом гидрирования оксида углерода в Процесс Фишера-Тропша, который широко практикуется для производства молекул с более длинной цепью, чем метан.
Примером крупномасштабной газификации угля в метан является Great Plains Synfuels завод, начатый в 1984 году в Беуле, Северная Дакота, как способ разработки обильных местных ресурсов низкосортных лигнит, ресурс, который иначе трудно транспортировать из-за его веса, пепел содержание, низкая теплотворная способность и склонность к случайное возгорание при хранении и транспортировке.
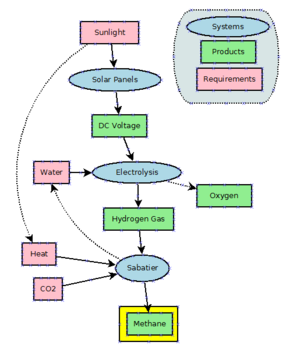
Энергия на метан это технология, которая использует электричество производить водород из воды электролиз и использует Сабатье реакция соединить водород с углекислый газ для производства метана. По состоянию на 2016 год он в основном находится в стадии разработки и не используется в больших масштабах. Теоретически этот процесс может использоваться в качестве буфера для избыточной и непиковой мощности, генерируемой сильно колеблющимся ветряные генераторы и солнечные батареи. Однако, поскольку в настоящее время на электростанциях используется очень большое количество природного газа (например, CCGT ) для производства электроэнергии потери КПД недопустимы.
Лабораторный синтез
Метан может производиться протонирование из метиллитий и метилмагний йодид. На практике потребность в чистом метане будет удовлетворяться за счет стального газового баллона от стандартных поставщиков.
Вхождение
Метан был открыт и выделен Алессандро Вольта между 1776 и 1778 годами при обучении болотный газ из Озеро Маджоре. Это основной компонент природного газа, около 87% по объему. Основным источником метана является добыча из геологических отложений, известных как месторождения природного газа, с газ из угольных пластов добыча становится основным источником (см. Добыча метана из угольных пластов, способ извлечения метана из каменный уголь депозит, пока усиленное извлечение метана из угольных пластов метод добычи метана из недобываемых угольных пластов). Это связано с другими углеводород топлива, а иногда и в сопровождении гелий и азот. Метан производится на мелководье (низкое давление) за счет анаэробный разлагаться из органическая материя и переработал метан из глубин земли. В целом отложения которые производят природный газ, находятся глубже и при более высоких температурах, чем те, которые содержат масло.
Метан обычно перевозится наливом трубопровод в виде природного газа или танкеры для перевозки СПГ в сжиженном виде; немногие страны перевозят его грузовиками.
Атмосферный метан

В 2010 году уровень метана в Арктике составлял 1850 нмоль / моль. Этот уровень более чем в два раза выше, чем когда-либо за последние 400 000 лет. Исторические концентрации метана в атмосфере мира колеблется от 300 до 400 нмоль / моль во время ледниковых периодов, обычно известных как ледниковые периоды, и от 600 до 700 нмоль / моль во время теплого межледниковый периоды. Океаны Земли являются потенциально важным источником метана в Арктике.[43]
Метан важен парниковый газ с потенциал глобального потепления из 34 по сравнению с CO2 (потенциал 1) за 100-летний период и 72 за 20-летний период.[44][45]
Концентрация метана в атмосфере Земли с 1750 года увеличилась примерно на 150%, и на нее приходится 20% от общего количества метана. радиационное воздействие от всех долгоживущих и глобально смешанных парниковых газов (эти газы не включают водяной пар, который на сегодняшний день является самым большим компонентом парниковый эффект ).[7]
С 2015 по 2019 год зафиксировано резкое повышение уровня атмосферного метана.[46][47] В феврале 2020 года сообщалось о выбросах метана из промышленность ископаемого топлива могло быть значительно недооценено.[48]
Изменение климата может повысить уровень метана в атмосфере за счет увеличения производства метана в естественных экосистемах, формируя Обратная связь об изменении климата.[32][49]
Клатраты
Клатраты метана (также известные как гидраты метана) представляют собой твердые клетки из молекул воды, которые удерживают отдельные молекулы метана. Значительные резервуары клатратов метана были обнаружены в арктической вечной мерзлоте и вдоль побережья. континентальные окраины под дно океана в пределах зона устойчивости клатратов газа, расположенных при высоких давлениях (от 1 до 100 МПа; нижний конец требует более низкой температуры) и низких температурах (<15 ° C; верхний конец требует более высокого давления).[50] Клатраты метана могут образовываться из биогенного метана, термогенного метана или их смеси. Эти отложения являются как потенциальным источником метанового топлива, так и потенциальным фактором глобального потепления.[51][52] Глобальная масса углерода, хранящегося в газовых клатратах, все еще остается неопределенной и оценивается в 12500 Gt углерод и всего 500 Гт углерода.[53] Оценка со временем снизилась, и последняя оценка составляет ~ 1800 Гт углерода.[54] Большая часть этой неопределенности связана с недостатком наших знаний об источниках и стоках метана и распределении клатратов метана в глобальном масштабе. Например, относительно недавно обнаруженный источник метана был обнаружен в сверхмедленный гребень разбрасывания в Арктике.[55] Некоторые климатические модели предполагают, что сегодняшний режим эмиссии метана со дна океана потенциально аналогичен режиму в период Палеоцен – эоцен термический максимум (ПЭТМ ) около 55,5 миллионов лет назад, хотя нет данных, указывающих на то, что метан в результате диссоциации клатратов в настоящее время достигает атмосферы.[54] Выброс метана в Арктике из вечная мерзлота и клатраты метана на морском дне являются потенциальным следствием и дополнительной причиной глобальное потепление; это известно как гипотеза клатратной пушки.[56][57][58][59] Данные за 2016 год показывают, что вечная мерзлота в Арктике тает быстрее, чем прогнозировалось.[60]
Внеземной метан
Межзвездная среда
Метан присутствует в большом количестве во многих частях Солнечной системы и потенциально может собираться на поверхности другого тела Солнечной системы (в частности, с использованием производство метана из местных материалов найти на Марс[61] или же Титан ), обеспечивая топливо для обратного пути.[23][62]
Марс
Метан обнаружен на всех планетах Солнечная система и большинство более крупных лун. За возможным исключением Марс, считается, что он произошел от абиотический процессы.[63][64]

В Любопытство ровер задокументировал сезонные колебания атмосферный метан уровни на Марсе. Эти колебания достигли пика в конце марсианского лета и составили 0,6 частей на миллиард.[65][66][67][68][69][70][71][72]
Метан был предложен в качестве возможного ракетное топливо на будущее Марсианские миссии отчасти из-за возможности синтезировать его на планете путем использование ресурсов на месте.[73] Адаптация Сабатье реакция метанирования может использоваться со смешанным слоем катализатора и обратная смена водяного газа в одном реакторе для производства метана из сырья, доступного на Марсе, с использованием воды из Марсианские недра и углекислый газ в Марсианская атмосфера.[61]
Метан может быть произведен небиологическим процессом, называемым серпентинизация[а] с участием воды, двуокиси углерода и минералов оливин, который, как известно, обычен на Марсе.[74]
История
В ноябре 1776 года метан был впервые научно идентифицирован Итальянский физик Алессандро Вольта в болотах Озеро Маджоре трансграничный Италия и Швейцария. На поиски этого вещества Вольта был вдохновлен после прочтения статьи, написанной Бенджамин Франклин про «горючий воздух».[75] Вольта собирал газ, поднимающийся с болота, и к 1778 году выделил чистый газ.[76] Он также продемонстрировал, что газ можно зажечь от электрической искры.[76]
Название «метан» было придумано в 1866 году немецким химиком. Август Вильгельм фон Хофманн.[77] Название произошло от метанол.
Этимология
Этимологически слово "метан"образовано от химического суффикса"-ан", что означает вещества, принадлежащие к семейству алканов; и слово"метил", которое происходит от немецкого"метил"(1840 г. н.э.) или напрямую от французов"Метил"что является бэк-формацией от французов"Метилен"(соответствует английскому" метилену "), корень которого был придуман Жан-Батистом Дюма и Эженом Пелиго в 1834 году от греческого"мети"(родственный англ. mead") и "Hyle"(что означает" дерево "). Радикал назван в честь этого, потому что он был впервые обнаружен в метанол, спирт, впервые выделенный перегонкой древесины. Химический суффикс "-ан"происходит от координирующего химического суффикса"-ine"от латинского суффикса женского рода"-в", который применяется для представления абстрактов. Согласование" -ane "," -ene "," -one "и т. д. было предложено в 1866 году немецким химиком Августом Вильгельмом фон Хофманном (1818-1892).
Сокращения
Аббревиатура CH4-C может означать массу углерода, содержащегося в массе метана, а масса метана всегда в 1,33 раза больше массы CH4-C.[78][79] CH4-C также может означать соотношение метан-углерод, которое составляет 1,33 по массе.[80]Метан в масштабах атмосферы обычно измеряется в тераграммах (Tg CH4) или миллионы метрических тонн (MMT CH4), что означает одно и то же.[81] Также используются другие стандартные единицы измерения, такие как наномоль (нмоль = одна миллиардная моля), крот (моль), килограмм, и грамм.
Безопасность
Метан нетоксичный, но он чрезвычайно огнеопасен и может образовывать взрывной смеси с воздухом. Метан также удушающий если концентрация кислорода снижается до менее 16% за счет вытеснения, как это может сделать большинство людей переносят снижение с 21% до 16% без побочных эффектов. Концентрация метана, при которой опасность удушья становится значительной, намного выше, чем концентрация 5–15% в легковоспламеняющейся или взрывоопасной смеси. Отходящий метан может проникать внутрь зданий вблизи свалки и подвергать жителей воздействию значительного количества метана. В некоторых зданиях под подвалом есть специально спроектированные системы рекуперации для активного улавливания этого газа и отвода его от здания.
Взрывы метана являются причиной многих смертельных катастроф на шахтах.[82] Взрыв метана стал причиной Катастрофа на угольной шахте Верхнего Биг Бранч в Западная Виргиния 5 апреля 2010 г. погибло 29 человек.[83]
Смотрите также
- 2007 г. катастрофа на шахте Засядько
- Абиогенное происхождение нефти
- Производство аэробного метана
- Анаэробное пищеварение
- Анаэробное дыхание
- Выбросы метана в Арктике
- Биогаз
- Месторождение добычи угля
- Плотность энергии
- Неорганизованные выбросы газа
- Глобальная инициатива по метану
- Галометан, галогенированные производные метана.
- Водородный цикл
- Промышленный газ
- Озеро Киву (более общий: лимническая сыпь )
- Список алканов с прямой цепью
- Метанирование
- Выбросы метана
- Метан на Марсе: атмосфера
- Метан на Марсе: климат
- Метаноген, археи которые производят метан.
- Метаногенез, микробы которые производят метан.
- Метанотроф, бактерии которые растут с метаном.
- Метильная группа, функциональная группа, относящаяся к метану.
- Томас Голд
Примечания
- ^ Есть много серпентинизация реакции. Оливин это Твердый раствор между форстерит и фаялит общая формула которого (Fe, Mg)2SiO4. Реакция получения метана из оливина может быть записана как: Форстерит + фаялит + вода + угольная кислота → серпентин + магнетит + метан , или (в сбалансированной форме): 18 мг2SiO4 + 6 Fe2SiO4 + 26 часов2O + CO2 → 12 мг3Si2О5(ОЙ)4 + 4 Fe3О4 + CH4
Рекомендации
- ^ а б «Переднее дело». Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга). Кембридж: Королевское химическое общество. 2014. С. 3–4. Дои:10.1039 / 9781849733069-FP001. ISBN 978-0-85404-182-4.
Метан - это сохраненное название (см. P-12.3), которое предпочтительнее систематического названия «карбан», имя, которое никогда не рекомендуется для замены метана, но используется для получения названий «карбен» и «карбин» для радикалов H2C2• и HC3•, соответственно.
- ^ «Газовая энциклопедия». Получено 7 ноября, 2013.
- ^ Pubchem. «Метан». pubchem.ncbi.nlm.nih.gov.
- ^ «Паспорт безопасности, название материала: метан» (PDF). США: Metheson Tri-Gas Incorporated. 4 декабря 2009 г. Архивировано с оригинал (PDF) 4 июня 2012 г.. Получено 4 декабря, 2011.
- ^ Управление реагирования и восстановления NOAA, Правительство США. «МЕТАН». noaa.gov.
- ^ Халил, М.А.К. (1999). «Парниковые газы, отличные от СО2, в атмосфере». Ежегодный обзор энергетики и окружающей среды. 24: 645–661. Дои:10.1146 / annurev.energy.24.1.645.
- ^ а б «Техническое резюме». Изменение климата 2001 г.. Программа ООН по окружающей среде. Архивировано из оригинал 4 июня 2011 г.
- ^ а б Этиопа, Джузеппе; Лоллар, Барбара Шервуд (2013). «Абиотический метан на Земле». Обзоры геофизики. 51 (2): 276–299. Bibcode:2013RvGeo..51..276E. Дои:10.1002 / rog.20011. ISSN 1944-9208.
- ^ Хеншер, Дэвид А. и Баттон, Кеннет Дж. (2003). Справочник транспорта и окружающей среды. Издательство «Изумруд Групп». п. 168. ISBN 978-0-08-044103-0.
- ^ Данные об изменении фазы метана. Интернет-книга NIST по химии.
- ^ Bini, R .; Пратеси, Г. (1997). «Инфракрасное исследование твердого метана под высоким давлением. Фазовая диаграмма до 30 ГПа». Физический обзор B. 55 (22): 14800–14809. Bibcode:1997ПхРвБ..5514800Б. Дои:10.1103 / Physrevb.55.14800.
- ^ Венделин Химмельхебер. «Кристаллические структуры». Получено 10 декабря, 2019.
- ^ Байк, Му-Хён; Ньюкомб, Мартин; Фриснер, Ричард А .; Липпард, Стивен Дж. (2003). «Механистические исследования гидроксилирования метана метаномонооксигеназой». Химические обзоры. 103 (6): 2385–419. Дои:10.1021 / cr950244f. PMID 12797835.
- ^ Снайдер, Бенджамин Э. Р .; Bols, Max L .; Schoonheydt, Robert A .; Sels, Bert F .; Соломон, Эдвард I. (19 декабря 2017 г.). «Активные центры железа и меди в цеолитах и их корреляция с металлоферментами». Химические обзоры. 118 (5): 2718–2768. Дои:10.1021 / acs.chemrev.7b00344. ISSN 0009-2665. PMID 29256242.
- ^ Рейманн, Иоахим; Jetten, Mike S.M .; Кельтьенс, Ян Т. (2015). "Глава 7 Металлические ферменты в «невозможных» микроорганизмах, катализирующие анаэробное окисление аммония и метана"В книге Питера М. Х. Кронека и Марты Э. Соса Торрес (ред.). Поддержание жизни на планете Земля: металлоферменты, усваивающие кислород и другие жевательные газы. Ионы металлов в науках о жизни. 15. Springer. С. 257–313. Дои:10.1007/978-3-319-12415-5_7. ISBN 978-3-319-12414-8. PMID 25707470.
- ^ Бордвелл, Фредерик Г. (1988). «Равновесные кислотности в растворе диметилсульфоксида». Отчеты о химических исследованиях. 21 (12): 456–463. Дои:10.1021 / ar00156a004.
- ^ Расул, Г .; Сурья Пракаш, Г.К .; Олах, Г.А. (2011). «Сравнительное исследование гиперкоординированных ионов карбония и их борных аналогов: задача для спектроскопистов». Письма по химической физике. 517 (1): 1–8. Bibcode:2011CPL ... 517 .... 1R. Дои:10.1016 / j.cplett.2011.10.020.
- ^ Bernskoetter, W.H .; Schauer, C.K .; Goldberg, K.I .; Брукхарт, М. (2009). "Характеристика комплекса родия (I) σ-метана в растворе". Наука. 326 (5952): 553–556. Bibcode:2009Sci ... 326..553B. Дои:10.1126 / science.1177485. PMID 19900892. S2CID 5597392.
- ^ Энергосодержание некоторых горючих материалов (в МДж / кг) В архиве 9 января 2014 г. Wayback Machine. People.hofstra.edu. Проверено 30 марта, 2014.
- ^ Марш, Джерри (1968). Развитие органической химии: реакции, механизмы и структура. Нью-Йорк: Книжная компания Макгроу-Хилл. С. 533–534.
- ^ «Компания Lumber Company размещает печи на полигоне для использования метана - сегодня менеджер по энергии». Энергоменеджер сегодня. Получено Одиннадцатое марта, 2016.
- ^ Корнелл, Клейтон Б. (29 апреля 2008 г.). «Автомобили, работающие на природном газе: топливо для КПГ почти бесплатно в некоторых частях страны». Архивировано из оригинал 20 января 2019 г.. Получено 25 июля, 2009.
Сжатый природный газ рекламируется как «наиболее чистое горючее» альтернативное топливо, поскольку простота молекулы метана снижает выбросы различных загрязняющих веществ в выхлопные трубы на 35–97%. Не столь драматично сокращение чистых выбросов парниковых газов, которое примерно такое же, как у этанола из кукурузного зерна, примерно на 20% по сравнению с бензином.
- ^ а б Thunnissen, Daniel P .; Guernsey, C. S .; Baker, R. S .; Мияке, Р. Н. (2004). "Продвинутое космическое топливо для исследования внешних планет". Американский институт аэронавтики и астронавтики (4–0799): 28.
- ^ "Двигатель Blue Origin BE-4". Получено 14 июня, 2019.
Мы выбрали СПГ, потому что он очень эффективен, дешев и широко доступен. В отличие от керосина, сжиженный природный газ можно использовать для создания избыточного давления в резервуаре. Это, известное как автогенное восстановление давления, устраняет необходимость в дорогостоящих и сложных системах, которые используют скудные запасы гелия на Земле. СПГ также обладает чистыми характеристиками сгорания даже при малом открытии дроссельной заслонки, что упрощает повторное использование двигателя по сравнению с керосиновым топливом.
- ^ Шмидт-Рор, Клаус (2015). «Почему процессы горения всегда экзотермичны, давая около 418 кДж на моль O2». Журнал химического образования. 92 (12): 2094–2099. Bibcode:2015JChEd..92.2094S. Дои:10.1021 / acs.jchemed.5b00333.
- ^ https://www.hydrogen.energy.gov/pdfs/hpep_report_2013.pdf
- ^ Россберг, М. и другие. (2006) «Хлорированные углеводороды» в Энциклопедия промышленной химии Ульмана, Wiley-VCH, Weinheim. Дои:10.1002 / 14356007.a06_233.pub2
- ^ Кьетявяйнен и Пуркамо (2015). «Происхождение, источник и круговорот метана в биосфере глубоких кристаллических пород». Передний. Микробиол. 6: 725. Дои:10.3389 / fmicb.2015.00725. ЧВК 4505394. PMID 26236303.
- ^ Крамер и Франке (2005). «Признаки активной нефтегазовой системы в море Лаптевых, северо-восток Сибири». Журнал нефтяной геологии. 28 (4): 369–384. Bibcode:2005JPetG..28..369C. Дои:10.1111 / j.1747-5457.2005.tb00088.x.
- ^ Лесснер, Дэниел Дж. (Декабрь 2009 г.) Биохимия метаногенеза. В: eLS. John Wiley & Sons Ltd, Чичестер. http://www.els.net [DOI: 10.1002 / 9780470015902.a0000573.pub2]
- ^ Тиль, Фолькер (2018), «Цикл углерода метана в прошлом: выводы из биомаркеров углеводородов и липидов», в Wilkes, Heinz (ed.), Углеводороды, масла и липиды: разнообразие, происхождение, химия и судьба, Справочник по углеводородной и липидной микробиологии, Springer International Publishing, стр. 1–30, Дои:10.1007/978-3-319-54529-5_6-1, ISBN 9783319545295
- ^ а б c d Дин, Джошуа Ф .; Мидделбург, Джек Дж .; Рёкманн, Томас; Aerts, Rien; Blauw, Luke G .; Эггер, Матиас; Jetten, Mike S.M .; де Йонг, Анник Э. Э .; Мейзел, Уве Х. (2018). «Метановая обратная связь с глобальной климатической системой в более теплом мире». Обзоры геофизики. 56 (1): 207–250. Bibcode:2018RvGeo..56..207D. Дои:10.1002 / 2017RG000559. HDL:1874/366386.
- ^ Серрано-Силва, Н .; Sarria-Guzman, Y .; Dendooven, L .; Луна-Гвидо, М. (2014). «Метаногенез и метанотрофия в почве: обзор». Педосфера. 24 (3): 291–307. Дои:10.1016 / с1002-0160 (14) 60016-3.
- ^ Sirohi, S.K .; Панди, Неха; Singh, B .; Пуния, А. К. (1 сентября 2010 г.). «Метаногены рубца: обзор». Индийский журнал микробиологии. 50 (3): 253–262. Дои:10.1007 / s12088-010-0061-6. ISSN 0973-7715. ЧВК 3450062. PMID 23100838.
- ^ МГЭИК. Изменение климата 2013: основы физических наук В архиве 3 октября 2018 г. Wayback Machine. Программа ООН по окружающей среде, 2013: гл. 6, стр. 507 IPCC.ch
- ^ Лю, Чжэ; Шао, Нана; Акинеми, Тайво; Уитмен, Уильям Б. (2018). «Метаногенез». Текущая биология. 28 (13): R727 – R732. Дои:10.1016 / j.cub.2018.05.021. ISSN 0960-9822. PMID 29990451.
- ^ «Инвентаризация выбросов и стоков парниковых газов в США: 1990–2014 гг.». 2016. Цитировать журнал требует
| журнал =(помощь) - ^ ФАО (2006). Длинная тень домашнего скота - экологические проблемы и возможности. Рим, Италия: Продовольственная и сельскохозяйственная организация Объединенных Наций (ФАО).. Получено 27 октября, 2009.
- ^ Гербер, П.Дж .; Steinfeld, H .; Хендерсон, В .; Mottet, A .; Opio, C .; Dijkman, J .; Фалькуччи А. и Темпио Г. (2013). «Решение проблемы изменения климата с помощью животноводства». Рим: Продовольственная и сельскохозяйственная организация Объединенных Наций (ФАО).
- ^ Плотва, Джон (13 мая 2002 г.). "Новая Зеландия пытается ограничить газообразную отрыжку овец". Национальная география. Получено 2 марта, 2011.
- ^ Сильверман, Джейкоб (16 июля 2007 г.). «Коровы загрязняют столько же, сколько машины?». HowStuffWorks.com.
- ^ Knittel, K .; Wegener, G .; Боэтиус, А. (2019), МакГенити, Терри Дж. (Редактор), «Анаэробные окислители метана», Микробные сообщества, использующие углеводороды и липиды: члены, метагеномика и экофизиология, Справочник по углеводородной и липидной микробиологии, Springer International Publishing, стр. 1–21, Дои:10.1007/978-3-319-60063-5_7-1, ISBN 9783319600635
- ^ «Исследование обнаружило неожиданный источник выбросов метана в Арктике». НАСА. 22 апреля 2012 г.
- ^ МГЭИК Пятый оценочный отчет, Таблица 8.7, гл. 8, стр. 8–58 (PDF; 8,0 МБ)
- ^ Shindell, D.T .; Faluvegi, G .; Koch, D. M .; Schmidt, G.A .; Унгер, Н .; Бауэр, С. Э. (2009). «Улучшенная атрибуция воздействия климата на выбросы». Наука. 326 (5953): 716–718. Bibcode:2009Sci ... 326..716S. Дои:10.1126 / science.1174760. PMID 19900930. S2CID 30881469.
- ^ Нисбет, Э. (5 февраля 2019 г.). «Очень сильный рост содержания метана в атмосфере за 4 года 2014–2017 гг .: последствия для Парижского соглашения». Глобальные биогеохимические циклы. 33 (3): 318–342. Bibcode:2019GBioC..33..318N. Дои:10.1029 / 2018GB006009.
- ^ Маккай, Робин (2 февраля 2017 г.). «Резкое повышение уровня метана угрожает мировым климатическим целям». Наблюдатель. ISSN 0029-7712. Получено 14 июля, 2019.
- ^ Челси Харви Выбросы метана от нефти и газа могут быть значительно занижены; Оценки выбросов метана из природных источников были слишком завышены, что перекладывает бремя на деятельность человека. Новости E&E через Scientific American 21 февраля 2020 г.
- ^ Кэррингтон, Дамиан, Первая активная утечка метана с морского дна обнаружена в Антарктиде, The Guardian, 21 июля 2020 г.
- ^ Борманн, Герхард; Торрес, Марта Э. (2006), Шульц, Хорст Д .; Забель, Маттиас (ред.), "Газовые гидраты в морских отложениях", Морская геохимия, Springer Berlin Heidelberg, стр. 481–512, Дои:10.1007/3-540-32144-6_14, ISBN 9783540321446
- ^ Миллер, Дж. Тайлер (2007). Поддержание Земли: комплексный подход. США: Thomson Advantage Books, ISBN 0534496725, п. 160.
- ^ Дин, Дж. Ф. (2018). «Обратная связь метана с глобальной климатической системой в более теплом мире». Обзоры геофизики. 56 (1): 207–250. Bibcode:2018RvGeo..56..207D. Дои:10.1002 / 2017RG000559. HDL:1874/366386.
- ^ Босуэлл, Рэй; Коллетт, Тимоти С. (2011). «Современные перспективы газовых гидратных ресурсов». Energy Environ. Наука. 4 (4): 1206–1215. Дои:10.1039 / c0ee00203h. ISSN 1754-5692.
- ^ а б Руппель и Кесслер (2017). «Взаимодействие изменения климата и гидратов метана». Обзоры геофизики. 55 (1): 126–168. Bibcode:2017RvGeo..55..126R. Дои:10.1002 / 2016RG000534.CS1 maint: использует параметр авторов (связь)
- ^ «В Северном Ледовитом океане обнаружен новый источник метана». Phys.org. 1 мая 2015 г.. Получено 10 апреля, 2019.
- ^ «Выбросы метана с арктического шельфа могут быть намного больше и быстрее, чем предполагалось» (Пресс-релиз). Национальный научный фонд (NSF). 10 марта 2010 г.
- ^ Коннор, Стив (13 декабря 2011 г.). «Огромные метановые« шлейфы »в Северном Ледовитом океане при отступлении морского льда». Независимый.
- ^ «Морской лед в Арктике достигает минимальной протяженности за год и спутниковый рекорд» (Пресс-релиз). Национальный центр данных по снегу и льду (NSIDC). 19 сентября 2012 г.
- ^ «Границы 2018/19: Новые проблемы, вызывающие озабоченность окружающей средой». ООН Окружающая среда. Получено 6 марта, 2019.
- ^ Reuters (18 июня 2019 г.). «Ученые шокированы таянием вечной мерзлоты в Арктике на 70 лет раньше, чем предполагалось». Хранитель. ISSN 0261-3077. Получено 14 июля, 2019.
- ^ а б Зубрин, Р. М .; Muscatello, A.C .; Берггрен, М. (2013). «Интегрированная система производства ракетного топлива Mars in situ». Журнал аэрокосмической техники. 26: 43–56. Дои:10.1061 / (ASCE) AS.1943-5525.0000201.
- ^ «Метановый взрыв». НАСА. 4 мая 2007 г.. Получено 7 июля, 2012.
- ^ Чанг, Кеннет (2 ноября 2012 г.). «Надежда на метан на Марсе угасает». Нью-Йорк Таймс. Получено 3 ноября, 2012.
- ^ Атрея, Сушил К .; Mahaffy, Paul R .; Вонг, Ах-Сан (2007). «Метан и родственные ему микроорганизмы на Марсе: происхождение, потеря, значение для жизни и обитаемости». Планетарная и космическая наука. 55 (3): 358–369. Bibcode:2007P & SS ... 55..358A. Дои:10.1016 / j.pss.2006.02.005.CS1 maint: использует параметр авторов (связь)
- ^ Браун, Дуэйн; Вендел, Джоанна; Стейгервальд, Билл; Джонс, Нэнси; Хорошо, Андрей (7 июня 2018 г.). «Выпуск 18-050 - НАСА обнаружило на Марсе древний органический материал, таинственный метан». НАСА. Получено 7 июня, 2018.
- ^ НАСА (7 июня 2018 г.). "На Марсе обнаружена древняя органика - видео (03:17)". НАСА. Получено 7 июня, 2018.
- ^ Уолл, Майк (7 июня 2018 г.). «Марсоход Curiosity находит на Марсе древние« строительные блоки для жизни »». Space.com. Получено 7 июня, 2018.
- ^ Чанг, Кеннет (7 июня 2018 г.). «Жизнь на Марсе? Последнее открытие марсохода ставит ее« на стол »- идентификация органических молекул в породах на красной планете не обязательно указывает на жизнь там, в прошлом или настоящем, но указывает на то, что некоторые из строительных блоков присутствовали. ". Нью-Йорк Таймс. Получено 8 июня, 2018.
- ^ Воозен, Пол (7 июня 2018 г.). "Марсоход НАСА попадает в органическую почву на Марсе". Наука. Дои:10.1126 / science.aau3992. Получено 7 июня, 2018.
- ^ десять Кейт, Инге Лоэс (8 июня 2018 г.). «Органические молекулы на Марсе». Наука. 360 (6393): 1068–1069. Bibcode:2018Научный ... 360.1068T. Дои:10.1126 / science.aat2662. PMID 29880670. S2CID 46952468.
- ^ Вебстер, Кристофер Р.; и другие. (8 июня 2018 г.). «Фоновые уровни метана в атмосфере Марса сильно зависят от сезона». Наука. 360 (6393): 1093–1096. Bibcode:2018Sci ... 360.1093W. Дои:10.1126 / science.aaq0131. PMID 29880682.
- ^ Eigenbrode, Jennifer L .; и другие. (8 июня 2018 г.). "Органическое вещество сохранилось в аргиллитах возрастом 3 миллиарда лет в кратере Гейла на Марсе". Наука. 360 (6393): 1096–1101. Bibcode:2018Научный ... 360.1096E. Дои:10.1126 / science.aas9185. PMID 29880683.
- ^ Ричардсон, Дерек (27 сентября 2016 г.). «Илон Маск демонстрирует межпланетную транспортную систему». Spaceflight Insider. Получено 3 октября, 2016.
- ^ Oze, C .; Шарма, М. (2005). «Есть оливин, будет газ: серпентинизация и абиогенное производство метана на Марсе». Письма о геофизических исследованиях. 32 (10): L10203. Bibcode:2005GeoRL..3210203O. Дои:10.1029 / 2005GL022691.
- ^ Вольта, Алессандро (1777) Lettere del Signor Don Alessandro Volta ... Sull 'Aria Inflammable Nativa Delle Paludi [Письма синьора дона Алессандро Вольта ... о горючем родном воздухе болот], Милан, Италия: Джузеппе Марелли.
- ^ а б Метан. Книга. Получено 26 января, 2012.
- ^ Видеть:
- А. В. Хофманн (1866 г.) «О действии трихлорида фосфора на соли ароматических моноаминов», Труды Лондонского королевского общества, 15 : 55–62; см. сноску на стр. 57–58.
- Джеймс Майкл Макбрайд (1999) "Разработка систематических названий простых алканов". Доступно на сайте Химический факультет Йельского университета (Нью-Хейвен, Коннектикут). В архиве 16 марта 2012 г. Wayback Machine
- ^ Джаясундара, Сусанта (3 декабря 2014 г.). «Есть ли разница в выражении парниковых газов в виде CH4 кг / га и CH4-C кг / га?». ResearchGate. Получено 26 августа, 2020.
- ^ «Руководство пользователя по оценке выбросов углекислого газа, метана и оксида азота в сельском хозяйстве с использованием инструмента государственной инвентаризации» (PDF). Агентство по охране окружающей среды США. 26 ноября 2019 г.,. Получено 26 августа, 2020.
- ^ «Что означает CH4-C? - Определение CH4-C - CH4-C означает соотношение метан-углерод». acronymsandslang.com. Получено 26 августа, 2020.
- ^ Управление по воздуху и радиации, Агентство по охране окружающей среды США (7 октября 1999 г.). «Выбросы метана в США с 1990 по 2020 годы: инвентаризация, прогнозы и возможности для сокращения (EPA 430-R-99-013)» (PDF). ourenergypolicy.org. Получено 26 августа, 2020.
- ^ Дозольм, Филипп. «Обычные горные аварии». About.com.
- ^ Лоуренс Мессина и Грег Блюстайн (8 апреля 2010 г.). «Представитель ФРС: еще слишком рано для спасения шахты W.Va.». News.yahoo.com. Получено 8 апреля, 2010.
внешняя ссылка
- Метан в Периодическая таблица видео (Ноттингемский университет)
- Международная карта химической безопасности 0291
- Газ (метан) гидраты - новые рубежи - Геологическая служба США
- Лансфорд, Джек Х. (2000). «Каталитическая конверсия метана в более полезные химические вещества и топливо: задача 21 века». Катализ сегодня. 63 (2–4): 165–174. Дои:10.1016 / S0920-5861 (00) 00456-9.
- CDC - Справочник по контролю за метаном в горнодобывающей промышленности













