Plumbane - Plumbane
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Plumbane | |
| Другие имена Плюмбан, тетрагидрид свинца, тетрагидридолид, гидрид свинца (IV) | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
PubChem CID | |
| |
| |
| Свойства | |
| PbH4 | |
| Молярная масса | 211,23 г / моль |
| Точка кипения | -13 ° С (9 ° F, 260 К) |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Plumbane, PbH4, это металл гидрид и группа 14 гидрид состоит из вести и водород.[1] Plumbane не очень хорошо охарактеризован или хорошо известен, и он термодинамически нестабилен в отношении потери атома водорода.[2] Производные свинца включают: тетрафторид свинца, (PbF4), и тетраэтилсвинец, ((CH3CH2)4Pb).
История
До недавнего времени было неизвестно, действительно ли был синтезирован свинец,[3]хотя первые сообщения относятся к 1920-м годам[4] а в 1963 г. Заальфельд и Свек сообщили о наблюдении PbH+
4 методом масс-спектрометрии.[5] Plumbane неоднократно становился предметом Дирак –Хартри – Фок релятивистский расчет исследования, которые исследуют стабильность, геометрию и относительную энергию гидридов формулы MH4 или MH2.[2][6][7]
Свойства
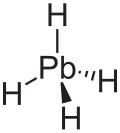
Plumbane - нестабильный бесцветный газ и является наиболее тяжелым гидридом группы IV.[8] Кроме того, у отвеса есть тетраэдрический (Td) структура с равновесным расстоянием между свинцом и водородом 1,73 Å.[9] По весу состав свинца составляет 1,91% водорода и 98,09% свинца. В отвесе формальный состояния окисления водорода и свинца равны -1 и +4 соответственно, поскольку электроотрицательность водорода выше, чем свинца. Устойчивость гидридов металлов с формулой MH4 (M = C – Pb) уменьшается с увеличением атомного номера M.
Подготовка
Ранние исследования PbH4 выявили, что молекула нестабильна по сравнению с более легкими сородичами (силан, немецкий, и Станнане ).[10] Его нельзя получить методами, используемыми для синтеза GeH.4 или SnH4.
В 1999 г. был синтезирован свинец из нитрат свинца (II), Pb (НЕТ3)2, и борогидрид натрия, NaBH4.[11] В 2005 году было сообщено о не возникающем механизме синтеза свинца.[12]
В 2003 году Ван и Эндрюс внимательно изучили препарат PbH.4 от лазерная абляция и дополнительно идентифицировал инфракрасный (ИК) диапазоны.[13]
Конгенеры
Конгенеры из отвеса включают:
использованная литература
- ^ Порритт, К. Дж. (1975). Chem. Инд-Лондон. 9: 398. Отсутствует или пусто
| название =(Помогите) - ^ а б Hein, Thomas A .; Тиль, Уолтер; Ли, Тимоти Дж. (1993). «Ab initio исследование стабильности и колебательных спектров свинца, метилплюмбана и гомологичных соединений». Журнал физической химии. 97 (17): 4381–4385. Дои:10.1021 / j100119a021. HDL:11858 / 00-001M-0000-0028-1862-2.
- ^ Cotton, F. A .; Wilkinson, G .; Мурильо, К. А .; Бохман, М. Продвинутая неорганическая химия. Wiley: Нью-Йорк, 1999.
- ^ Панет, Фриц; Нёрринг, Отто (1920). "Убер Блейвассерстофф". Berichte der Deutschen Chemischen Gesellschaft (серии A и B). 53 (9): 1693–1710. Дои:10.1002 / cber.19200530915.
- ^ Saalfeld, Fred E .; Свец, Гарри Дж. (1963). «Масс-спектры летучих гидридов. I. Моноэлементные гидриды элементов IVB и VB групп». Неорганическая химия. 2: 46–50. Дои:10.1021 / ic50005a014.
- ^ Desclaux, J. P .; Пыкко, П. (1974). "Релятивистские и нерелятивистские расчеты одноцентрового разложения Хартри-Фока для ряда CH4 в PbH4 в сферическом приближении ». Письма по химической физике. 29 (4): 534–539. Bibcode:1974CPL .... 29..534D. Дои:10.1016/0009-2614(74)85085-2.
- ^ Pyykkö, P .; Дескло, Дж. П. (1977). Одноцентровые расчеты Дирака – Фока показывают (114) H4 походить на PbH4". Природа. 266 (5600): 336–337. Bibcode:1977Натура.266..336П. Дои:10.1038 / 266336a0.
- ^ CRC Справочник по химии и физике Интернет-издание.
- ^ Visser, O .; Visscher, L .; Aerts, P. J. C .; Ньивпорт, В. К. (1992). "Релятивистские полностью электронные молекулярные расчеты Хартри-Фока-Дирака- (Брейта) на CH4, SiH4, GeH4, SnH4, PbH4". Теоретика Chimica Acta. 81 (6): 405–416. Дои:10.1007 / BF01134864.
- ^ Малли, Гульзари Л .; Зигерт, Мартин; Тернер, Дэвид П. (2004). "Релятивистские и электронные корреляционные эффекты для молекул тяжелых элементов: Ab initio полностью релятивистские расчеты связанных кластеров для PbH.4". Международный журнал квантовой химии. 99 (6): 940–949. Дои:10.1002 / qua.20142.
- ^ Кривцун, В. М .; Курицын, Ю. А .; Снегирев, Э. П. (1999). «Наблюдение ИК-спектров поглощения нестабильного PbH.4 молекула " (PDF). Опт. Spectrosc. 86 (5): 686–691. Bibcode:1999OptSp..86..686K. Архивировано из оригинал (PDF) на 2016-03-04. Получено 2012-12-31.
- ^ Zou, Y; Джин, FX; Chen, ZJ; Qiu, DR; Ян, ПЙ (2005). «Невозрастающий водородный механизм образования свинца». Гуан Пу Сюэ Ю Гуан Пу Фэнь Си = Гуан Пу. 25 (10): 1720–3. PMID 16395924.
- ^ Ван, Сюэфэн; Эндрюс, Лестер (2003). «Инфракрасные спектры гидридов 14-й группы в твердом водороде: экспериментальное наблюдение PbH.4, Pb2ЧАС2, и Pb2ЧАС4". Журнал Американского химического общества. 125 (21): 6581–6587. Дои:10.1021 / ja029862l. PMID 12785799.







