Сероводород - Hydrogen disulfide
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Дисульфид дигидрогена | |
| Другие имена Сероводород; Персульфид водорода; Сероводород; Тиосульфеновая кислота | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
PubChem CID | |
| |
| |
| Характеристики | |
| ЧАС2S2 | |
| Молярная масса | 66.14 г · моль−1 |
| Внешность | желтая жидкость |
| Плотность | 1,334 г см−3 |
| Температура плавления | -89,6 ° С (-129,3 ° F, 183,6 К) |
| Точка кипения | 70,7 ° С (159,3 ° F, 343,8 К) |
| Основание конъюгата | Дисульфанид HS− 2 |
| Опасности | |
| точка возгорания | легковоспламеняющийся |
| Родственные соединения | |
Родственные соединения | Сероводород Пероксид водорода Диселенид водорода Дителлурид водорода Дихлорид дисеры |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Сероводород это неорганическое соединение с формулой H2S2. Этот халькогенид водорода представляет собой бледно-желтую летучую жидкость с запахом камфоры. Легко разлагается до сероводород (ЧАС2S) и элементаль сера.[1]
Структура
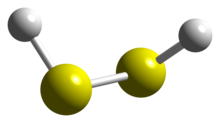
По структуре сероводород аналогичен структуре пероксид водорода, с C2 точечная групповая симметрия. Обе молекулы явно неплоские. Двугранный угол составляет 90,6 ° по сравнению с 111,5 ° в H2О2. Валентный угол H-S-S составляет 92 °, что близко к 90 ° для негибридизированной двухвалентной серы.[1]
Синтез и реакции
Дисульфид водорода можно синтезировать растворением щелочной металл или же щелочноземельный металл полисульфиды в воде. Когда раствор смешивается с концентрированным соляная кислота при -15 ° C желтое масло, состоящее из смеси полисульфаны (ЧАС2Sп) будет собираться ниже водного слоя. Фракционная перегонка этого масла дает сероводород отдельно от любых других полисульфидов (в основном трисульфида).[2][3][4][1]
Дисульфид водорода легко разлагается в условиях окружающей среды до сероводород и сера.[3] В сероорганическая химия, сероводород присоединяется к алкены давать дисульфиды и тиолы.[5]
Квантовое туннелирование и его подавление в дисульфиде дейтерия
В дейтерированный форма сероводорода DSSD, имеет аналогичную геометрию HSSH, но время туннелирования меньше, что делает ее удобным тестовым примером для квантовый эффект Зенона, в котором частое наблюдение квантовой системы подавляет ее нормальную эволюцию. Трост и Хорнбергер[6] вычислили, что, хотя изолированная молекула DSSD будет спонтанно колебаться между левой и правой хиральными формами с периодом 5,6 миллисекунды, присутствие небольшого количества инертного газообразного гелия должно стабилизировать хиральные состояния, фактически столкновения атомов гелия "наблюдаются". "мгновенное хиральность и, таким образом, подавление спонтанной эволюции к другому хиральному состоянию.[7]
Влияние на здоровье
Дисульфид водорода описывается как «имеющий сильный и раздражающий запах», который похож на камфора или же SCl
2, вызывая «слезы и жжение в ноздрях».[3] Если он присутствует в высоких концентрациях, он может вызвать головокружение, дезориентацию и, в конечном итоге, потерю сознания.[8]
Рекомендации
- ^ а б c R. Steudel "Неорганические полисульфаны H2Sп с п > 1 "в Элементарной сере и соединениях с высоким содержанием серы II (Topics in Current Chemistry) 2003, Volume 231, pp 99–125. Дои:10.1007 / b13182
- ^ Де, А. К. (15 января 2001 г.). Учебник неорганической химии. ISBN 978-81-224-1384-7.
- ^ а б c Уолтон и Парсон; Парсонс, Ллевеллин Б. (1921). «Получение и свойства персульфидов водорода». Варенье. Chem. Soc. 43 (12): 2539–48. Дои:10.1021 / ja01445a008.
- ^ Георг Брауэр: Справочник по препаративной неорганической химии Том I, страница 391, Wiley, 1963.
- ^ Опасные реагенты, Братья Робинзоны
- ^ Trost, J .; Хорнбергер, К. (2009). «Парадокс Хунда и столкновительная стабилизация киральных молекул». Phys. Rev. Lett. 103 (2): 023202. arXiv:0811.2140. Bibcode:2009ПхРвЛ.103б3202Т. Дои:10.1103 / PhysRevLett.103.023202. PMID 19659202.
- ^ Месячный расчет разрешает квантовый парадокс 82-летней давности, Physics Today, сентябрь 2009 г., стр. 16
- ^ Стейн, Уилкинсон, Г. (2007). Семинары по общей психиатрии взрослых. Королевский колледж психиатров. ISBN 978-1-904671-44-2.







