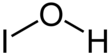
Гипоиодистая кислота - Hypoiodous acid
| |||
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Гипоиодистая кислота | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ЧЭБИ | |||
| ChemSpider | |||
PubChem CID | |||
| UNII | |||
| |||
| |||
| Свойства | |||
| HIO | |||
| Молярная масса | 143,89 г / моль | ||
| Кислотность (пKа) | 10,5 (в воде, оценка) | ||
| Основание конъюгата | Гипойодит | ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Гипоиодистая кислота неорганическое соединение с химическая формула Привет. Образуется, когда водный раствор йод обрабатывается солями ртути или серебра. Он быстро разлагается непропорциональность:[1]
- 5 HIO → HIO3 + 2 я2 + 2 часа2О
Гипойодиты щелочных и щелочно-земельных металлов могут быть получены в холодных разбавленных растворах, если к их соответствующим гидроксидам добавить йод. Гипойодистая кислота представляет собой слабую кислоту с пKа около 11. Сопряженное основание - гипойодит (IO−). Соли этого аниона можно получить, обрабатывая I2 с гидроксидами щелочных металлов. Они быстро становятся непропорциональными по форме йодиды и йодаты.[1]
использованная литература
- ^ а б Холлеман, А.Ф. (2001). Виберг, Нильс (ред.). Неорганическая химия (1-е англ. Ред.). Сан-Диего, Калифорния: Берлин: Academic Press, W. de Gruyter. ISBN 0-12-352651-5.
| Эта неорганический соединение –Связанная статья является заглушка. Вы можете помочь Википедии расширяя это. |