Пирофосфорная кислота - Pyrophosphoric acid
 | |
 | |
| Имена | |
|---|---|
| Имена ИЮПАК Дифосфорная кислота μ-оксидо-бис (дигидроксидооксидофосфор) | |
| Другие имена Дифосфорная кислота | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.017.795 |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| ЧАС4п2О7 | |
| Молярная масса | 177,97 г / моль |
| Температура плавления | 71,5 ° С (160,7 ° F, 344,6 К) |
| Чрезвычайно растворим | |
| Растворимость | Очень растворим в алкоголь, эфир |
| Основание конъюгата | Пирофосфат |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
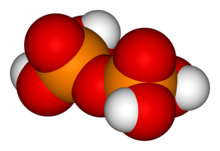
Пирофосфорная кислота, также известный как дифосфорная кислота, представляет собой неорганическое соединение с формулой H4п2О7 или, более описательно, [(HO)2P (O)]2О. Бесцветный и без запаха, растворим в воды, диэтиловый эфир, и этиловый спирт. Безводная кислота кристаллизуется двумя полиморфы, плавящиеся при 54,3 и 71,5 ° C. Соединение не особенно полезно, за исключением того, что оно является компонентом полифосфорной кислоты и сопряженной кислоты пирофосфат-аниона. Анионы, соли, и сложные эфиры пирофосфорной кислоты называются пирофосфаты.
Подготовка
Лучше всего его приготовить ионным обменом из пирофосфата натрия или обработкой пирофосфата свинца сероводород. Это не подготовлено обезвоживание фосфорной кислоты. Вместо этого пирофосфорная кислота производится только как один из продуктов.
Реакции
В расплавленном состоянии пирофосфорная кислота быстро образует равновесную смесь фосфорной кислоты, пирофосфорной кислоты и полифосфорных кислот. Весовой процент пирофосфорной кислоты составляет около 40%, и ее трудно перекристаллизовать из расплава. В водном растворе пирофосфорная кислота, как и все полифосфорные кислоты, гидролизуется и в конечном итоге устанавливается равновесие между фосфорной кислотой, пирофосфорной кислотой и полифосфорными кислотами.[1]
- ЧАС4п2О7 + H2O ⇌ 2H3PO4
Пирофосфорная кислота средней силы неорганический кислота.
Безопасность
Хотя пирофосфорная кислота вызывает коррозию, она не токсична.[2]
История
Название пирофосфорная кислота было дано «мистером Кларком из Глазго» в 1827 году, которому приписывают ее открытие после нагревания до красного каления соли фосфата натрия. Было обнаружено, что фосфорная кислота при нагревании до красного каления образует пирофосфорную кислоту, которая легко превращается в фосфорную кислоту горячей водой.[3]
Смотрите также
- Пирофосфат натрия
- Болезнь отложения дигидрата пирофосфата кальция
- Диметилаллил пирофосфат
- ADP
- АТФ
- Орто кислоты
- трифосфорная кислота
Рекомендации
- ^ Корбридж, Д. (1995). «Глава 3: Фосфаты». Исследования по неорганической химии vol. 20. Elsevier Science B.V., стр. 169–305. Дои:10.1016 / B978-0-444-89307-9.50008-8. ISBN 0-444-89307-5.
- ^ Паспорт безопасности материала: Пирофосфорная кислота MSDS www.sciencelab.com
- ^ Бек, Льюис Калеб (1834). Руководство по химии: краткое изложение современного состояния науки с множеством ссылок на более обширные трактаты, оригинальные статьи и т. Д.. E.W&C Скиннер. п. 160. Получено 30 января, 2015.
