Бромистая кислота - Bromous acid
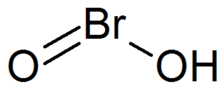 | |
 | |
 | |
| Имена | |
|---|---|
| Имена ИЮПАК гидрокси-λ3-броманон гидроксидооксидобромин бромистая кислота | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
PubChem CID | |
| |
| |
| Характеристики | |
| HBrO2 | |
| Молярная масса | 112,911 г / моль |
| Основание конъюгата | Бромит |
| Родственные соединения | |
Другой анионы | Бромистоводородная кислота; гипобромистая кислота; бромная кислота; пербромовая кислота |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Бромистая кислота это неорганическое соединение с формулой HBrO2. Это нестабильное соединение, хотя соли сопряженного с ним основания - бромитов - были выделены. В кислом растворе бромиты разлагаются до брома.[1]
Открытие
В 1905 году Ричардс А. Х. доказал существование бромистой кислоты посредством серии экспериментов с участием нитрат серебра (AgNO3) и бром.[2] Реакция избытка холодной воды с образованием гипобромистая кислота (HBrO), бромид серебра (AgBr) и азотная кислота (HNO3):
- Br2 + AgNO3 + H2O → HBrO + AgBr + HNO3
Ричардс обнаружил, что эффект добавления избыточного жидкого брома в концентрированный нитрат серебра (AgNO3) привел к другому механизму реакции. Из количества эквивалентных порций кислого брома, образовавшегося в предыдущей реакции, было рассчитано соотношение между кислородом и бромом с точным значением O: Br (0,149975: 0,3745), предполагая, что кислотное соединение содержит два атома кислорода на один атом брома. Таким образом, химическая структура кислотного соединения была рассчитана как HBrO2.[2]
По словам Ричардса, гипобромистая кислота (HBrO) возникает в результате реакции раствора брома и нитрата серебра:[2]
- Br2 + AgNO3 + H2O → HBrO + AgBr + HNO3
- 2 AgNO3 + HBrO + Br2 + H2O → HBrO2 + 2 AgBr + 2 HNO3
Изомерия
Молекула HBrO2 имеет изогнутую структуру с углами ∠ (H − O − Br) 106,1 °. HOBrO также принимает неплоскую конформацию с одной изомерной структурой (2a), имеющей двугранный угол ∠ (H-O-Br-O), равный 74,2 °. Более того, планарные структуры двух других изомеров (2b-СНГ и 2c-транс) являются переходным состоянием для быстрой энантиомеризации.[3]
Другое исследование выявило три изомера: HOOBr, HOBrO и HBr (O) O.[4]
Синтез
Реакция окисления между гипобромистая кислота (HBrO) и хлорноватистая кислота (HClO) можно использовать для производства бромистой кислоты (HBrO2) и соляная кислота (HCl).[5]
- HBrO + HClO → HBrO2 + HCl
Редокс-реакция гипобромистая кислота (HBrO) может образовывать бромистую кислоту (HBrO2) как его продукт:[5]
- HBrO + H2O - 2e− → HBrO2 + 2H+
В реакция диспропорционирования двух эквивалентов гипобромистая кислота (HBrO) приводит к образованию как бромистых кислот (HBrO2) и бромистоводородная кислота (HBr):[5]
- 2 HBrO → HBrO2 + HBr
Реакция перегруппировки, которая возникает в результате син-пропорции бромная кислота (HBrO3) и бромистоводородная кислота (HBr) дает бромистую кислоту (HBrO2):[5]
- 2 HBrO3 + HBr → 3 HBrO2
Бромит натрия
Соли NaBrO2· 3H2O и Ba (BrO2)2·ЧАС2O были кристаллизованы. При обработке этих водных растворов солями Pb2+, Hg2+, а Ag+соответствующие бромиты тяжелых металлов выпадают в осадок в виде твердых веществ.[1]
Реакция Белоусова – Жаботинского
Бромистая кислота является продуктом Реакция Белоусова – Жаботинского образуется в результате комбинации бромата калия, сульфата церия (IV), пропандиовой кислоты и лимонной кислоты в разбавленной серной кислоте. Бромистая кислота представляет собой промежуточную стадию реакции между бромат-ионом (Братан−
3 ) и брома (Br−):[6][7]
- Братан−
3 + 2 руб.− → HBrO2 + HBrO
Другие важные реакции в таких колебательных реакциях:
- HBrO2 + Братан−
3 + H+ → 2 Братан•
2 + H2О - 2 HBrO2 → Братан−
3 + HOBr + H+
Бромиты уменьшают перманганаты к манганаты (VI):[1]
- 2 MnO−
4 + Братан−
2 + ОН− → 2 MnO2−
4 + Братан−
3 + H2О
пKа измерение
Константа кислотной диссоциации бромистой кислоты, Kа = [ЧАС+][Братан−
2]/[HBrO2], определялась разными методами.
Значение pKа для бромистой кислоты оценивалась при исследовании разложения бромитов. В ходе исследования была измерена скорость разложения бромита в зависимости от концентрации ионов водорода и бромита. Экспериментальные данные журнала начальной скорости были нанесены на график в зависимости от pH. Используя этот метод, оценка pKа значение для бромистой кислоты составило 6,25.[8]
Используя другой метод, pKа для бромистой кислоты измеряли на основе начальной скорости реакции между бромитами натрия и йодом калия в диапазоне pH 2,9–8,0, при 25 ° C и ионной силе 0,06 М. Зависимость первого порядка от начальной скорости этого реакция диспропорционирования на [H+] в диапазоне pH 4,5–8,0. Значение константы диссоциации кислоты, измеренное этим методом, составляет Kа = (3.7±0.9)×10−4 M и рKа = 3.43±0.05.[9]
Реактивность
По сравнению с другими кислородно-центрированными окислителями (гипогалитами, анионами пероксидов) и в соответствии с его низкой основностью, бромит является довольно слабым нуклеофилом.[10] Константы скорости бромита по отношению к карбокатионам и акцепторозамещенным олефинам на 1–3 порядка ниже, чем измеренные для гипобромита.
Рекомендации
- ^ а б c Эгон Виберг, Арнольд Фредерик Холлеман (2001) Неорганическая химия, Эльзевьер ISBN 0-12-352651-5
- ^ а б c "Журнал Общества химической промышленности. V.25 1906". HathiTrust. Получено 2017-04-28.
- ^ Глейзер, Райнер; Йост, Мэри (2012-08-16). «Диспропорционирование бромистой кислоты HOBrO прямым переносом O и через ангидриды O (BrO)2 и BrO-BrO2. Неэмпирическое исследование механизма ключевой стадии колебательной реакции Белоусова – Жаботинского ». Журнал физической химии A. 116 (32): 8352–8365. Дои:10.1021 / jp301329g. ISSN 1520-5215. PMID 22871057.
- ^ Соуза, Габриэль Л. К. де; Браун, Алекс (2016-07-01). «Основное и возбужденное состояния HBrO2 [HOOBr, HOBrO и HBr (O) O] и HBrO3 (HOOOBr и HOOBrO) изомеры ». Счета теоретической химии. 135 (7): 178. Дои:10.1007 / s00214-016-1931-8. ISSN 1432-881X.
- ^ а б c d К., Ропп, Р. (1 января 2013 г.). Энциклопедия щелочноземельных соединений. Эльзевир. ISBN 9780444595508. OCLC 964753424.
- ^ Вассалини, Ирэн; Алессандри, Ивано (2015). «Пространственное и временное управление хранением информации в целлюлозе с помощью химически активированных колебаний». Прикладные материалы и интерфейсы ACS. 7 (51): 28708–28713. Дои:10.1021 / acsami.5b11857. PMID 26654462.
- ^ Филд, Ричард Дж .; Корос, Эндре; Нойес, Ричард М. (1972-12-01). «Колебания в химических системах. II. Тщательный анализ временных колебаний в системе бромат-церий-малоновая кислота». Журнал Американского химического общества. 94 (25): 8649–8664. Дои:10.1021 / ja00780a001. ISSN 0002-7863.
- ^ Массаглы, А. (01.01.1970). «Кинетическое исследование разложения бромита - ScienceDirect». Неорганика Chimica Acta. 4: 593–596. Дои:10.1016 / S0020-1693 (00) 93357-7.
- ^ Faria, R. B .; Эпштейн, Ирвинг Р .; Кустин, Кеннет (1 января 1994). «Кинетика диспропорционирования и pKa бромистой кислоты». Журнал физической химии. 98 (4): 1363–1367. Дои:10.1021 / j100055a051. ISSN 0022-3654.
- ^ Майер, Роберт Дж .; Офиал, Армин Р. (22 февраля 2018 г.). «Нуклеофильная активность отбеливающих реагентов». Органические буквы. 20 (10): 2816–2820. Дои:10.1021 / acs.orglett.8b00645. PMID 29741385.
