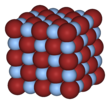
Бромид серебра - Silver bromide
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Бромид серебра (I) | |||
| Другие имена | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.029.160 | ||
| UNII | |||
| |||
| |||
| Характеристики | |||
| AgBr | |||
| Молярная масса | 187,77 г / моль | ||
| Внешность | Бледно-желтое твердое вещество светочувствительный | ||
| Плотность | 6,473 г / см3, твердый | ||
| Температура плавления | 432 ° С (810 ° F, 705 К) | ||
| Точка кипения | 1,502 ° C (2,736 ° F, 1,775 К) (разлагается) | ||
| 0,140 мг / л (20 ° С) | |||
Продукт растворимости (Kзр) | 5.4 × 10 −13 | ||
| Растворимость | не растворим в алкоголь, наиболее кислоты умеренно растворим в аммиак растворим в щелочи цианид решения | ||
| Ширина запрещенной зоны | 2,5 эВ | ||
| Электронная подвижность | 4000 см2/(Против) | ||
| −59.7·10−6 см3/ моль | |||
| 2.253 | |||
| Термохимия | |||
Теплоемкость (C) | 270 Дж / (кг · К) | ||
Стандартный моляр энтропия (S | 107 Дж · моль−1· K−1[1] | ||
Станд. Энтальпия формирование (ΔжЧАС⦵298) | −100 кДж · моль−1[1] | ||
| Родственные соединения | |||
Другой анионы | Фторид серебра (I) Хлорид серебра Йодид серебра | ||
Другой катионы | Бромид меди (I) Бромид ртути (I) | ||
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Бромид серебра (AgBr), мягкая, бледно-желтая, нерастворимая в воде соль, хорошо известная (наряду с другими галогенидами серебра) своими необычными чувствительность к свету. Это свойство позволило галогенидам серебра стать основой современных фотоматериалов.[2] AgBr широко используется в фотопленках и, как полагают некоторые, использовался для изготовления Туринская плащаница.[3] Соль встречается в природе как минерал. бромаргирит.
Подготовка
Хотя соединение можно найти в минеральной форме, AgBr обычно получают по реакции нитрат серебра с бромидом щелочного металла, обычно бромид калия:[2]
- AgNO3(водн.) + KBr (водн.) → AgBr (s) + KNO3(водн.)
Хотя это менее удобно, соль также можно приготовить непосредственно из ее элементов.
Современное приготовление простой светочувствительной поверхности включает формирование эмульсии кристаллов галогенида серебра в желатине, которую затем наносят на пленку или другую основу. Кристаллы образуются путем осаждения в контролируемой среде с образованием мелких однородных кристаллов (обычно <1 мкм в диаметре и содержащих ~ 10 мкм в диаметре).12 Атомы Ag), называемые зернами.[2]
Реакции
Бромид серебра легко реагирует с жидким аммиаком с образованием различных комплексов аммиака, таких как Ag (NH
3)
2Br и Ag (NH
3)
2Br−
2. В целом:[4]
- AgBr + m NH3 + (п - 1) Br−
→ Ag (NH
3)
мBr1-н
п
Бромид серебра реагирует с трифенилфосфин чтобы получить продукт трис (трифенилфосфин):[5]
Физические свойства
Кристальная структура
Все AgF, AgCl и AgBr имеют гранецентрированную кубическую (ГЦК) структуру решетки каменной соли (NaCl) со следующими параметрами решетки:[6]
| Сложный | Кристалл | Структура | Решетка, а / Å | ||||
| AgF | fcc | каменная соль, NaCl | 4.936 | ||||
| AgCl, хлораргирит | fcc | каменная соль, NaCl | 5.5491 | ||||
| AgBr, бромаргирит | fcc | каменная соль, NaCl | 5.7745 | ||||
| |||||||
Более крупные ионы галогенидов расположены в кубической плотной упаковке, в то время как более мелкие ионы серебра заполняют октаэдрические промежутки между ними, образуя 6-координатную структуру, в которой ион серебра Ag+ окружен 6 Br− ионы, и наоборот. Координационная геометрия AgBr в структуре NaCl является неожиданной для Ag (I), который обычно образует линейные, тригональные (3-координированный Ag) или тетраэдрический (4-координированный Ag) комплексы.
В отличие от других галогенидов серебра, иодаргирит (AgI) имеет гексагональную решетчатую структуру цинкита.
Растворимость
Галогениды серебра имеют широкий диапазон растворимости. Растворимость AgF составляет около 6 × 107 раз больше, чем у AgI. Эти различия объясняются относительной сольватация энтальпии галогенид-ионов; энтальпия сольватации фторида аномально велика.[7]
| Сложный | Растворимость (г / 100 г H2O) |
| AgF | 172 |
| AgCl | 0.00019 |
| AgBr | 0.000014 |
| AgI | 0.000003 |
Светочувствительность
Хотя фотографические процессы развивались с середины 1800-х годов, подходящих теоретических объяснений не было до 1938 года, когда была опубликована статья Р.В. Герни и Н.Ф. Мотт.[8] Эта статья вызвала большое количество исследований в области химии и физики твердого тела, а также, в частности, в области фоточувствительности галогенида серебра.[2]
Дальнейшие исследования этого механизма показали, что фотографические свойства галогенидов серебра (в частности, AgBr) являются результатом отклонений от идеальной кристаллической структуры. Такие факторы, как рост кристаллов, примеси и дефекты поверхности, все влияют на концентрацию точечных ионных дефектов и электронных ловушек, которые влияют на чувствительность к свету и позволяют формировать скрытое изображение.[3]
- Дефекты Френкеля и квадрополярная деформация
Основным недостатком галогенидов серебра является Дефект Френкеля, где ионы серебра расположены межузельно (Agя+) в высокой концентрации с соответствующими им отрицательно заряженными вакансиями ионов серебра (Agv−). В чем уникальность AgBr Пары Френкеля заключается в том, что межузельный Agя+ исключительно подвижны, и его концентрация в слое ниже поверхности зерна (называемом слоем пространственного заряда) намного превышает концентрацию в собственном объеме.[3][9] Энергия образования пары Френкеля низкая - 1,16 эВ, а энергия активации миграции необычно мала при 0,05 эВ (по сравнению с NaCl: 2,18 эВ для образования Пара Шоттки и 0,75 эВ для катионной миграции). Такие низкие энергии приводят к большой концентрации дефектов, которая может достигать около 1% вблизи точки плавления.[9]
Низкая энергия активации в бромиде серебра может быть объяснена высокой квадрупольной поляризуемостью ионов серебра; то есть он может легко деформироваться из сферы в эллипсоид. Это свойство, являющееся результатом d9 Электронная конфигурация иона серебра облегчает миграцию как в ионе серебра, так и в вакансиях для иона серебра, что обеспечивает необычно низкую энергию миграции (для Agv−: 0,29–0,33 эВ по сравнению с 0,65 эВ для NaCl).[9]
Исследования показали, что на концентрацию дефектов сильно влияет (до нескольких кратных 10) размер кристаллов. Большинство дефектов, таких как концентрация межузельных ионов серебра и изгибы поверхности, обратно пропорциональны размеру кристалла, хотя вакансионные дефекты прямо пропорциональны. Это явление объясняется изменением равновесия химического состава поверхности и, таким образом, по-разному влияет на концентрацию дефектов.[3]
Концентрацию примесей можно контролировать путем роста кристаллов или прямого добавления примесей в растворы кристаллов. Хотя примеси в решетке бромида серебра необходимы для стимулирования образования дефектов Френкеля, исследования Гамильтона показали, что выше определенной концентрации примесей количество дефектов межузельных ионов серебра и положительных перегибов резко уменьшается на несколько порядков. После этого видны только вакансионные дефекты ионов серебра, которые фактически увеличиваются на несколько порядков.[3]
- Электронные ловушки и дырочные ловушки
Когда свет падает на поверхность зерна галогенида серебра, фотоэлектрон генерируется, когда галогенид теряет свой электрон в зону проводимости:[2][3][10]
- Икс− + hν → X + e−
После выхода электрона он соединится с межузельным атомом Ag.я+ создать атом металла серебра Agя0:[2][3][10]
- е− + Agя+ → Agя0
Из-за дефектов в кристалле электрон может уменьшить свою энергию и попасть в атом.[2] Степень границ зерен и дефектов в кристалле влияет на время жизни фотоэлектрона, где кристаллы с большой концентрацией дефектов будут захватывать электрон намного быстрее, чем более чистый кристалл.[10]
При мобилизации фотоэлектрона также образуется фотоотверстие h •, которое также необходимо нейтрализовать. Однако время жизни фотодыры не коррелирует со временем жизни фотоэлектрона. Эта деталь предполагает другой механизм захвата; Малиновский предполагает, что ловушки дырок могут быть связаны с дефектами из-за примесей.[10] После захвата дырки притягивают подвижные отрицательно заряженные дефекты в решетке: межузельная вакансия серебра Agv−:[10]
- ч • + Agv− ⇌ h.Agv
Формирование h.Agv снижает свою энергию в достаточной степени, чтобы стабилизировать комплекс и уменьшить вероятность выброса дырки обратно в валансную зону (константа равновесия дырочного комплекса внутри кристалла оценивается в 10−4.[10]
Дополнительные исследования по захвату электронов и дырок показали, что примеси также могут быть важной системой захвата. Следовательно, промежуточные ионы серебра не могут быть восстановлены. Следовательно, эти ловушки на самом деле являются механизмами потерь и считаются неэффективными. Например, кислород воздуха может взаимодействовать с фотоэлектронами с образованием O2− виды, которые могут взаимодействовать с дыркой, чтобы обратить комплекс и подвергнуться рекомбинации. Примеси ионов металлов, такие как медь (I), железо (II) и кадмий (II), продемонстрировали захват дырок в бромиде серебра.[3]
- Химия поверхности кристаллов;
Как только дырочные комплексы образуются, они диффундируют к поверхности зерна в результате образовавшегося градиента концентрации. Исследования показали, что время жизни дырок у поверхности зерна намного больше, чем у дырок в объеме, и что эти дырки находятся в равновесии с адсорбированным бромом. Чистый эффект - это равновесный толчок на поверхности для образования большего количества дырок. Следовательно, когда дырочные комплексы достигают поверхности, они диссоциируют:[10]
- h.Agv− → h • + Agv− → Br → ДОЛЯ Br2
Благодаря этому реакционному равновесию дырочные комплексы постоянно расходуются на поверхности, которая действует как сток, пока не будут удалены из кристалла. Этот механизм обеспечивает аналог уменьшения межузельного содержания Agя+ к Agя0, что дает общее уравнение:[10]
- AgBr → Ag + ФРАКЦИЯ Br2
- Формирование скрытого изображения и фотография
Теперь, когда часть теории изложена, можно обсудить реальный механизм фотографического процесса. Подводя итог, можно сказать, что когда фотопленка подвергается воздействию изображения, фотоны, падающие на зерно, производят электроны, которые взаимодействуют с образованием металлического серебра. Больше фотонов, попадающих в конкретное зерно, будет производить большую концентрацию атомов серебра, содержащую от 5 до 50 атомов серебра (из ~ 1012 атомов) в зависимости от чувствительности эмульсии. Теперь пленка имеет градиент концентрации пятнышек атомов серебра, основанный на различной интенсивности света по ее площади, создавая невидимый "скрытое изображение ".[2][10]
Во время этого процесса на поверхности кристалла образуются атомы брома. Для сбора брома слой поверх эмульсии, называемый сенсибилизатором, действует как акцептор брома.[10]
Во время проявления пленки скрытое изображение усиливается добавлением химического вещества, обычно гидрохинон, эта селективность уменьшает те зерна, которые содержат атомы серебра. Этот процесс, чувствительный к температуре и концентрации, полностью восстановит зерна до металлического серебра, усиливая скрытое изображение примерно на 1010 до 1011. Этот шаг демонстрирует преимущество и превосходство галогенидов серебра над другими системами: скрытого изображения, для формирования которого требуется всего миллисекунды и которое является невидимым, достаточно для создания из него полного изображения.[2]
После проявления пленка «фиксируется», при этом оставшиеся соли серебра удаляются, чтобы предотвратить дальнейшее восстановление, оставляя на пленке «негативное» изображение. Используемый агент тиосульфат натрия, и реагирует согласно следующему уравнению:[2]
- AgX (s) + 2 Na2S2О3(водн.) → Na3[Ag (S2О3)2] (водн.) + NaX (водн.)
Неопределенное количество положительных отпечатков может быть получено из негатива, пропуская через него свет и выполняя те же действия, описанные выше.[2]
Свойства полупроводника
Когда бромид серебра нагревается в пределах 100 ° C от его точки плавления, график Аррениуса ионной проводимости показывает, что значение увеличивается и «поворачивается вверх». Другие физические свойства, такие как модули упругости, теплоемкость и запрещенная зона электронов, также увеличиваются, что свидетельствует о приближении кристалла к нестабильности.[9] Такое поведение, типичное для полупроводника, объясняется температурной зависимостью образования дефектов Френкеля, и при нормировке на концентрацию дефектов Френкеля график Аррениуса линеаризуется.[9]
Смотрите также
Рекомендации
- ^ а б Зумдал, Стивен С. (2009). Химические принципы 6-е изд.. Компания Houghton Mifflin. п. A23. ISBN 978-0-618-94690-7.
- ^ а б c d е ж грамм час я j k Гринвуд, Н.Н., Эрншоу, А. (1984). Химия элементов. Нью-Йорк: Permagon Press. С. 1185–87. ISBN 978-0-08-022057-4.CS1 maint: несколько имен: список авторов (связь)
- ^ а б c d е ж грамм час Гамильтон, Дж. Ф. (1974). «Физические свойства микрокристаллов галогенида серебра». Фотографическая наука и инженерия. 18 (5): 493–500.
- ^ Leden, I., Persson, G .; Перссон; Сьёберг; Плотина; Сьёберг; Тофт (1961). «Растворимость хлорида серебра и бромида серебра в водном аммиаке и образование смешанных комплексов галогенида серебра и аммиака». Acta Chem. Сканд. 15: 607–614. Дои:10.3891 / acta.chem.scand.15-0607.CS1 maint: несколько имен: список авторов (связь)
- ^ Энгельгардт, Л. М.; Хили, ПК; Патрик, штат Вирджиния; Уайт, AH (1987). "Аддукты основания Льюиса соединений металлов (I) группы-11. XXX. Комплексы 3: 1 трифенилфосфина с галогенидами серебра (I)". Aust. J. Chem. 40 (11): 1873–1880. Дои:10.1071 / CH9871873.
- ^ Глаус, С., Кальзаферри, Г. (2003). «Зонные структуры галогенидов серебра AgF, AgCl и AgBr: сравнительное исследование». Photochem. Photobiol. Наука. 2 (4): 398–401. Дои:10.1039 / b211678b.
- ^ Лиде, Дэвид Р. (ред.). (2005)Справочник по химии и физике, 86-е издание, The Chemical Rubber Publishing Co., Кливленд.
- ^ Gurney, R.W .; Мотт, Н. Ф. (1938). «Теория фотолиза бромистого серебра и фотографическое скрытое изображение». Proc. Рой. Soc. A164 (917): 151–167. Bibcode:1938RSPSA.164..151G. Дои:10.1098 / rspa.1938.0011.
- ^ а б c d е Слифкин, Л. М. (1989). «Физика дефектов решетки в галогенидах серебра». Дефекты кристаллической решетки и аморфные материалы. 18: 81–96.
- ^ а б c d е ж грамм час я j Малиновский, Дж. (1968). «Роль отверстий в фотографическом процессе». Журнал фотографической науки. 16 (2): 57–62. Дои:10.1080/00223638.1968.11737436.