Перхлорат серебра - Silver perchlorate
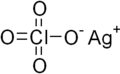 | |
| Имена | |
|---|---|
| Название ИЮПАК Перхлорат серебра (I) | |
| Систематическое название ИЮПАК Хлорат серебра (I) (VII) | |
| Другие имена Хлорная кислота, соль серебра (1+) Аргентный перхлорат | |
| Идентификаторы | |
| |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.029.123 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| AgClO4 | |
| Молярная масса | 207,319 г / моль |
| Внешность | Бесцветный гигроскопичный кристаллы |
| Плотность | 2,806 г / см3 |
| Температура плавления | 486 ° С (907 ° F, 759 К) (разлагается) |
| 557 г / 100 мл (25 ° С) 792,8 г / 100 мл (99 ° С) | |
| Растворимость | растворим в органических растворителях |
| Структура | |
| кубический | |
| Опасности | |
| R-фразы (устарело) | R8 R34 R50 |
| S-фразы (устарело) | S15 S17 S26 S36 / 37/39 S45 |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Перхлорат серебра это химическое соединение с формулой AgClO4. Это белое твердое вещество образует моногидрат и слегка расплывающийся. Это полезный источник Ag+ ион, хотя наличие перхлорат представляет риски. Он используется как катализатор неорганическая химия.
Производство
Перхлорат серебра создается путем нагревания смеси хлорная кислота с нитрат серебра.
Альтернативно, его можно получить реакцией между перхлорат бария и сульфат серебра, или от реакции хлорной кислоты с оксид серебра.
Растворимость
Перхлорат серебра примечателен своей растворимостью в ароматических растворителях, таких как бензол (52,8 г / л) и толуол (1010 г / л).[1] В этих растворителях катион серебра связывается с ареном, что было продемонстрировано обширными кристаллографическими исследованиями кристаллов, полученных из таких растворов.[2][3] Его растворимость в воде чрезвычайно высока, до 500 г на 100 мл воды.
Связанные реагенты
Похожий на нитрат серебра, перхлорат серебра - эффективный реагент для замены галогениды лиганды с перхлоратом, который является слабо или некоординирующий анион. Использование перхлората серебра в химическом синтезе сократилось из-за опасений по поводу взрывоопасности перхлоратных солей. Прочие серебряные реагенты тетрафторборат серебра, и связанные трифторметансульфонат серебра и гексафторфосфат серебра.
Рекомендации
- ^ Ф. Бржезина; Дж. Моллин; Р. Пасторек; З. Шинделарж (1986). Chemické tabulky anorganických sloučenin [Химические таблицы неорганических соединений] (на чешском языке). Прага: СНТЛ.
- ^ Э. А. Холл Гриффит; Э. Л. Амма (1974). "Металлические ионно-ароматические комплексы. XVIII. Получение и молекулярная структура тетрагидрата нафталина-тетракис (перхлората серебра)". Журнал Американского химического общества. 96 (3): 743–749. Дои:10.1021 / ja00810a018.
- ^ Р. К. Макмаллан; Т. Ф. Кетцле; К. Дж. Фритчи-младший (1997). «Низкотемпературное нейтронографическое исследование π-комплекса перхлорат серебра с бензолом». Acta Crystallographica B. 53 (4): 645–653. Дои:10.1107 / S0108768197000712.
| HClO4 | Он | ||||||||||||||||
| LiClO4 | Быть (ClO4)2 | B (ClO 4)− 4 B (ClO4)3 | РОКЛО3 | N (ClO4)3 NH4ClO4 NOClO4 | О | FClO4 | Ne | ||||||||||
| NaClO4 | Mg (ClO4)2 | Al (ClO4)3 | Si | п | S | ClO− 4 ClOClO3 Cl2О7 | Ar | ||||||||||
| KClO4 | Ca (ClO4)2 | Sc (ClO4)3 | Ti (ClO4)4 | VO (ClO4)3 VO2(ClO4) | Cr (ClO4)3 | Mn (ClO4)2 | Fe (ClO4)3 | Co (ClO4)2, Co (ClO4)3 | Ni (ClO4)2 | Cu (ClO4)2 | Zn (ClO4)2 | Ga (ClO4)3 | Ge | В качестве | Se | Br | Kr |
| RbClO4 | Sr (ClO4)2 | Y (ClO4)3 | Zr (ClO4)4 | Nb (ClO4)5 | Пн | Tc | RU | Rh (ClO4)3 | Pd (ClO4)2 | AgClO4 | Cd (ClO4)2 | В (ClO4)3 | Sn (ClO4)4 | Sb | TeO (ClO4)2 | я | Xe |
| CsClO4 | Ba (ClO4)2 | Hf (ClO4)4 | Ta (ClO4)5 | W | Re | Операционные системы | Ir | Pt | Au | Hg2(ClO4)2, Hg (ClO4)2 | Tl (ClO4), Tl (ClO4)3 | Pb (ClO4)2 | Bi (ClO4)3 | По | В | Rn | |
| FrClO4 | Ра | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ц | Og | |
| ↓ | |||||||||||||||||
| Ла | Ce (ClO4)Икс | Pr | Nd | Вечера | Sm (ClO4)3 | Eu (ClO4)3 | Gd (ClO4)3 | Tb (ClO4)3 | Dy (ClO4)3 | Хо (ClO4)3 | Er (ClO4)3 | Tm (ClO4)3 | Yb (ClO4)3 | Лу (ClO4)3 | |||
| Ac | Th (ClO4)4 | Па | UO2(ClO4)2 | Np | Пу | Являюсь | См | Bk | Cf | Es | FM | Мкр | Нет | Lr | |||

