Гептан - Википедия - Heptane
 | |
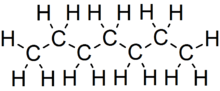 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Гептан[2] | |
| Другие имена Септан[1] | |
| Идентификаторы | |
3D модель (JSmol ) | |
| 1730763 | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| Номер ЕС |
|
| 49760 | |
| MeSH | н-гептан |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1206 |
| |
| |
| Характеристики | |
| C7ЧАС16 | |
| Молярная масса | 100.205 г · моль−1 |
| Внешность | Бесцветная жидкость |
| Запах | Бензин |
| Плотность | 0,6795 г см−3[3] |
| Температура плавления | −90.549[3] ° С (-130,988 ° F, 182,601 К) |
| Точка кипения | 98.38[3] ° С (209,08 ° F, 371,53 К) |
| 0,0003% (20 ° С)[4] | |
| бревно п | 4.274 |
| Давление газа | 5,33 кПа (при 20,0 ° C) |
Закон Генри постоянный (kЧАС) | 12 нмоль Па−1 кг−1 |
| -85.24·10−6 см3/ моль | |
| 1.3855[3] | |
| Вязкость | 0,389 мПа · с[5] |
| 0,0 Д | |
| Термохимия | |
Теплоемкость (C) | 224,64 Дж К−1 моль−1 |
Стандартный моляр энтропия (S | 328,57 Дж К−1 моль−1 |
Станд. Энтальпия формирование (ΔжЧАС⦵298) | −225,2–−223,6 кДж моль−1 |
Станд. Энтальпия горение (ΔcЧАС⦵298) | −4,825–−4,809 МДж моль−1 |
| Опасности | |
| Пиктограммы GHS |     |
| Сигнальное слово GHS | Опасность |
| H225, H304, H315, H336, H410 | |
| P210, P261, P273, P301 + 310, P331 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | -4,0 ° С (24,8 ° F, 269,1 К) |
| 223,0 ° С (433,4 ° F, 496,1 К) | |
| Пределы взрываемости | 1.05–6.7% |
| Смертельная доза или концентрация (LD, LC): | |
LC50 (средняя концентрация ) | 17 986 частей на миллион (мышь, 2 часа)[6] |
LCLo (самый низкий опубликованный ) | 16000 частей на миллион (человек) 15000 частей на миллион (мышь, 30 мин)[6] |
| NIOSH (Пределы воздействия на здоровье в США): | |
PEL (Допустимо) | TWA 500 частей на миллион (2000 мг / м3)[4] |
REL (Рекомендуемые) | TWA 85 частей на миллион (350 мг / м3) C 440 частей на миллион (1800 мг / м3) [15 минут][4] |
IDLH (Непосредственная опасность) | 750 частей на миллион[4] |
| Родственные соединения | |
Родственные алканы | |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Гептан или же п-гептан прямая цепь алкан с химическая формула ЧАС3C (CH2)5CH3 или C7ЧАС16, и является одним из основных компонентов бензин (бензин). При использовании в качестве тестового топливного компонента в антидетонационный тестовые двигатели, 100% гептановое топливо является нулевой точкой октановое число шкала (100 баллов - это 100% изооктан ). Октановое число соответствует антидетонационным свойствам сравниваемой смеси гептана и изооктана, которое выражается как процентное содержание изооктана в гептане и указано на насосах для бензин (бензин) распределяется по всему миру.
Использует
Гептан (и многие его изомеры) широко используется в лаборатории как неполярный растворитель. Как жидкость, идеально подходит для транспортировки и хранения. В тесте жирных пятен гептан используется для растворения масляного пятна, чтобы показать предыдущее присутствие органических соединений на окрашенной бумаге. Это делается путем встряхивания окрашенной бумаги в растворе гептана примерно полминуты.[нужна цитата ]
Водный бром можно отличить от водного йод по его появлению после добыча в гептан. В воде появляются и бром, и йод. коричневый. Однако йод превращается фиолетовый при растворении в гептане, тогда как раствор брома остается коричневым.
Гептан коммерчески доступен в виде смешанных изомеров для использования в красках и покрытиях, так как резиновый клей растворитель "Bestine", уличное печное топливо "Powerfuel" от Primus, в чистом виде. п-гептан для исследований и разработок и фармацевтического производства, а также как второстепенный компонент бензина.
Гептан также используется как средство для удаления клея к коллекционеры марок. С 1974 г. Почтовая служба Соединенных Штатов выпустил самоклеющиеся марки что некоторым коллекционерам трудно отделить от конвертов традиционным методом замачивания в воде. Продукты на основе гептана, такие как Bestine, а также лимонен продукты на основе стали популярными растворителями для более легкого удаления штампов.[7]
Шкала октанового числа
п-Гептан определяется как нулевая точка октановое число шкала. Это более легкий компонент в бензин горит больше взрывоопасно, вызывая двигатель предварительное зажигание (стучать ) в чистом виде, в отличие от октан изомеры, которые горят медленнее и вызывают меньшую детонацию. Первоначально он был выбран в качестве нулевой точки шкалы из-за наличия очень высокой чистоты п-гептан, не смешанный с другими изомерами гептана или других алканов, дистиллированный из смола из Джеффри Пайн и из плодов Pittosporum Resiniferum. Другие источники гептана и октана, полученные из сырая нефть, содержат смесь различных изомеров с сильно различающимися характеристиками и не дают такой точной нулевой точки.
Изомеры и энантиомеры
Гептан имеет девять изомеры, или одиннадцать, если энантиомеры подсчитываются:
- Гептан (п-гептан), H3C – CH2–CH2–CH2–CH2–CH2–CH3,
- 2-метилгексан (изогептан), H3C – CH (CH3) –CH2–CH2–CH2–CH3,
- 3-метилгексан, H3C – CH2–C*H (CH3) –CH2–CH2–CH3 (хиральный ),
- 2,2-диметилпентан (неогептан), H3C – C (CH3)2–CH2–CH2–CH3,
- 2,3-диметилпентан, H3C – CH (CH3) –C*H (CH3) –CH2–CH3 (хиральный ),
- 2,4-диметилпентан, H3C – CH (CH3) –CH2–CH (CH3) –CH3,
- 3,3-диметилпентан, H3C – CH2–C (CH3)2–CH2–CH3,
- 3-этилпентан, H3C – CH2–CH (CH2CH3) –CH2–CH3,
- 2,2,3-триметилбутан, H3C – C (CH3)2–CH (CH3) –CH3, этот изомер также известен как пентаметилэтан и триптан.[8]
Подготовка
Линейный п-гептан можно получить из Джеффри Пайн масло.[9] Шесть разветвленных изомеров без четвертичного углерода могут быть получены путем создания подходящей вторичной или третичной алкоголь посредством Реакция Гриньяра, преобразовав его в алкен к обезвоживание, и гидрогенизация последний.[9] Изомер 2,2-диметилпентана можно получить путем взаимодействия терт-бутилхлорид с п-пропилмагния бромид.[9] Изомер 3,3-диметилпентана можно получить из терт-амилхлорид и этилмагнийбромид.[9]
Риск для здоровья
Эта секция нуждается в расширении. Вы можете помочь добавляя к этому. (Июнь 2015 г.) |
Резкое воздействие паров гептана может вызвать головокружение, ступор, нарушение координации движений, потеря аппетита, тошнота, дерматит, химический пневмонит или потеря сознания, возможная периферическая невропатия.[10]
Рекомендации
- ^ Хофманн, Август Вильгельм Фон (1 января 1867 г.). «I. О действии трихлорида фосфора на соли ароматических монаминов». Труды Лондонского королевского общества. 15: 54–62. Дои:10.1098 / rspl.1866.0018.
- ^ «н-гептан - Резюме соединения». PubChem Compound. США: Национальный центр биотехнологической информации. 16 сентября 2004 г. Идентификационные и связанные записи. Получено 2 января 2012.
- ^ а б c d Хейнс, Уильям М., изд. (2011). CRC Справочник по химии и физике (92-е изд.). Бока-Ратон, Флорида: CRC Press. п. 3.290. ISBN 1439855110.
- ^ а б c d Карманный справочник NIOSH по химической опасности. "#0312". Национальный институт охраны труда и здоровья (NIOSH).
- ^ Dymond, J. H .; Ой, Х.А. (1994). «Вязкость выбранных жидких н-алканов». Журнал физических и химических справочных данных. 23 (1): 41–53. Дои:10.1063/1.555943. ISSN 0047-2689.
- ^ а б «н-гептан». Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ Батлер, Питер. «Это похоже на волшебство: удаление самоклеящихся марок с бумаги» (PDF). Американское филателистическое общество. Получено 15 июн 2020.
- ^ Изомеры. Members.optushome.com.au. Проверено 4 марта 2012.
- ^ а б c d Грэм Эдгар, Джордж Калингерт и Р. Э. Маркер (1929): «Получение и свойства изомерных гептанов. Часть I. Получение». Журнал Американского химического общества, том 51, выпуск 5, страницы 1483–1491. Дои:10.1021 / ja01380a027
- ^ Пэтти, ФА; Янт В.П. (1929). «Интенсивность запаха и симптомы, вызываемые коммерческими парами пропана, бутана, пентана, гексана и гептана». Отчет о расследованиях. Министерство торговли США, Горное управление США. № 2979 (декабрь): 1–10.








