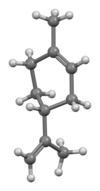
Лимонен - Limonene
| |||
 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC 1-Метил-4- (проп-1-ен-2-ил) циклогекс-1-ен | |||
| Другие имена 1-метил-4- (1-метилэтенил) циклогексен 4-изопропенил-1-метилциклогексен п-Мент-1,8-диен Рацемический: DL-Лимонен; Дипентен | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ |
| ||
| ChemSpider | |||
| ECHA InfoCard | 100.028.848 | ||
| КЕГГ | |||
PubChem CID | |||
| UNII |
| ||
| |||
| |||
| Характеристики | |||
| C10ЧАС16 | |||
| Молярная масса | 136.238 г · моль−1 | ||
| Внешность | от бесцветной до бледно-желтой жидкости | ||
| Запах | апельсин | ||
| Плотность | 0,8411 г / см3 | ||
| Температура плавления | -74,35 ° С (-101,83 ° F, 198,80 К) | ||
| Точка кипения | 176 ° С (349 ° F, 449 К) | ||
| Нерастворимый | |||
| Растворимость | Смешиваемый с бензол, хлороформ, эфир, CS2, и масла растворим в CCl4 | ||
Хиральное вращение ([α]D) | 87–102° | ||
| 1.4727 | |||
| Термохимия | |||
Станд. Энтальпия горение (ΔcЧАС⦵298) | −6,128 МДж моль−1 | ||
| Опасности | |||
| Главный опасности | Сенсибилизатор кожи / Контактный дерматит - После устремления, отек легких, пневмонит, и смерть[1] | ||
| Пиктограммы GHS |     | ||
| Сигнальное слово GHS | Опасность | ||
| H226, H304, H315, H317, H400, H410 | |||
| P210, P233, P240, P241, P242, P243, P261, P264, P272, P273, P280, P301 + 330 + 331, P302 + 352, P303 + 361 + 353, P304 + 340, P312, P333 + 313, P362, P370 + 378, P391, P403 + 233, P235, P405, P501 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 50 ° С (122 ° F, 323 К) | ||
| 237 ° С (459 ° F, 510 К) | |||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Лимонен бесцветная жидкость алифатический углеводород классифицируется как циклический монотерпен, и является основным компонентом в масло из Цитрусовый фрукт пилинги.[1] В D-изомер, чаще встречающийся в природе как ароматизатор апельсинов, является ароматизатором в пищевой промышленности.[1][2] Он также используется в химическом синтезе как предшественник к Carvone и как возобновляемые источники энергии растворитель в чистящие средства.[1] Менее распространенный L-изомер находится в мятные масла и имеет сосновый, скипидар -подобный запах.[1] Соединение является одним из основных летучих монотерпенов, содержащихся в смоле хвойные породы, особенно в Pinaceae, и из апельсиновое масло.
Лимонен получил свое название от Французский лимон ("лимон ").[3] Лимонен - это хиральный молекула, а биологические источники производят одну энантиомер: основной промышленный источник, Цитрусовый фрукт, содержит D-лимонен ((+) - лимонен), который является (р) -энантиомер.[1] Рацемический лимонен известен как дипентен.[4] D-Лимонен коммерчески получают из цитрусовых двумя основными способами: центробежная сепарация или же паровая дистилляция.
Химические реакции
Лимонен - относительно стабильный монотерпен и может перегоняться без разложения, хотя при повышенных температурах трещины формировать изопрен.[5] Легко окисляется во влажном воздухе с образованием карвеол, Carvone, и оксид лимонена.[1][6] Вместе с серой он подвергается дегидрированию до п-Cymene.[7]
Лимонен обычно встречается как D- или же (р)-энантиомер, но рацемизирует до дипентена при 300 ° C. Когда согревается минеральная кислота, лимонен изомеризуется в сопряженный диен α-терпинен (который также можно легко преобразовать в п-цимен ). Доказательства этой изомеризации включают образование Дильс – Альдер аддукты между аддуктами α-терпинена и малеиновый ангидрид.
Возможно избирательно проводить реакцию по одной из двойных связей. Безводный хлористый водород реагирует преимущественно на дизамещенный алкен, тогда как эпоксидирование с mCPBA происходит у тризамещенного алкена.
В другом синтетическом методе Марковникова сложение из трифторуксусная кислота с последующим гидролиз ацетата дает терпинеол.
Биосинтез
В природе лимонен образуется из геранилпирофосфат, через циклизацию Нерил карбокатион или его эквивалент, как показано.[8] Последний шаг включает потерю протона из катиона с образованием алкен.

Наиболее широко применяемое преобразование лимонена - это Carvone. Трехступенчатая реакция начинается с региоселективный добавление нитрозилхлорид через тризамещенную двойную связь. Затем этот вид превращается в оксим с основание, а гидроксиламин удаляется, чтобы дать кетон -содержащий карвон.[2]
В растениях
D-Лимонен является основным компонентом ароматических запахов и смолы характерны для многочисленных хвойных и широколиственных деревьев: клен красный и серебристый (Acer rubrum, Acer saccharinum ), тополя (Populus angustifolia ), осина (Populus grandidentata, Populus tremuloides ) сумах (Rhus glabra ), ель (Picea виды), различные сосны (например, Pinus echinata, Pinus ponderosa ), Пихта Дугласа (Псевдоцуга menziesii ), лиственницы (Ларикс виды), настоящие ели (Abies виды), болиголовы (Цуга виды), каннабис (Каннабис сатива виды),[9] кедры (Cedrus виды), разные Cupressaceae, и куст можжевельника (Можжевельник виды).[1] Способствует возникновению характерного запаха апельсиновая корка, апельсиновый сок и другие цитрусовые фрукты.[1][10] Чтобы оптимизировать извлечение ценных компонентов из отходов кожуры цитрусовых, d-лимонен обычно удаляют.[11]
Безопасность и исследования
D-Лимонен, нанесенный на кожу, может вызвать раздражение от контактный дерматит, но в остальном кажется безопасным для использования человеком.[12][13] Лимонен - это легковоспламеняющийся в виде жидкости или пара, и он токсичен для водная жизнь.[1]
Использует
Лимонен распространен как пищевая добавка и как ароматизатор для косметика товары.[1] Как основной аромат кожуры цитрусовых, D-лимонен используется в производстве продуктов питания и некоторых лекарствах, таких как ароматизатор замаскировать горький вкус алкалоиды, и как аромат в парфюмерия, лосьоны после бритья, средства для ванн и др. личная гигиена товары.[1] D-Лимонен также используется как ботанический инсектицид.[1][14] D-Лимонен используется в органическом гербициде «Мститель».[15] Его добавляют в чистящие средства, такие как средства для мытья рук, чтобы придать лимон или апельсин. аромат (видеть апельсиновое масло ) и за его способность растворять масла.[1] В отличие, L-лимонен имеет сосновый, скипидар -подобный запах.
Лимонен используется как растворитель для очистки, например средство для удаления клея, или удаление масла из деталей машин, поскольку оно произведено из возобновляемых источников (эфирное масло цитрусовых, как побочный продукт апельсиновый сок производство).[11] Он используется как средство для снятия краски а также полезен как ароматная альтернатива скипидар. Лимонен также используется в качестве растворителя в некоторых модель самолета клеи и как компонент некоторых красок. Коммерческие освежители воздуха с пропеллентами, содержащими лимонен, используются филателисты для удаления самоклеящихся почтовых марок с конвертов.[16]
Лимонен также используется как растворитель для изготовления плавленых волокон на основе 3D печать.[17] Принтеры могут печатать на пластике, выбранном для модели, но устанавливать опоры и переплеты из БЕДРА, а полистирол пластик, легко растворимый в лимонене. Поскольку лимонен легко воспламеняется, он также считается биотопливо.[18]
При подготовке ткани за гистология или гистопатология, D-лимонен часто используется как менее токсичный заменитель ксилол при очистке обезвоженных образцов. Очистители - это жидкости, смешиваемые со спиртами (например, этиловый спирт или же изопропанол ) и с расплавленным парафиновая свеча, в который заделаны образцы для облегчения резки шлифов для микроскопия.[19][20][21]
Смотрите также
Рекомендации
- ^ а б c d е ж грамм час я j k л м п "D-Лимонен ». База данных PubChem Compound. Национальный центр биотехнологической информации, Национальная медицинская библиотека США. 2017. Получено 22 декабря 2017.
- ^ а б Фальбуш, Карл-Георг; Хаммершмидт, Франц-Йозеф; Пантен, Йоханнес; Пикенхаген, Вильгельм; Шатковски, Дитмар; Бауэр, Курт; Гарбе, Доротея; Сурбург, Хорст (2003). «Ароматизаторы и ароматизаторы». Энциклопедия промышленной химии Ульмана. Дои:10.1002 / 14356007.a11_141. ISBN 978-3-527-30673-2.
- ^ Словарь Мерриам-Вебстера для слова "лимонен ". Доступ 16 марта 2020 г.
- ^ Симонсен, Дж. Л. (1947). Терпены. 1 (2-е изд.). Издательство Кембриджского университета. OCLC 477048261.[страница нужна ]
- ^ Пакдел, Х. (2001). "Изготовление DL-лимонен путем вакуумного пиролиза изношенных шин ». Журнал аналитического и прикладного пиролиза. 57: 91–107. Дои:10.1016 / S0165-2370 (00) 00136-4.
- ^ Карлберг, Анн-Тереза; Магнуссон, Керстин; Нильссон, Ульрика (1992). «Окисление воздухом D-лимонен (цитрусовый растворитель) создает сильные аллергены ». Контактный дерматит. 26 (5): 332–340. Дои:10.1111 / j.1600-0536.1992.tb00129.x. PMID 1395597.
- ^ Weitkamp, A. W. (1959). "I. Действие серы на терпены. Сульфиды лимонена". Журнал Американского химического общества. 81 (13): 3430–3434. Дои:10.1021 / ja01522a069.
- ^ Mann, J.C .; Hobbs, J. B .; Banthorpe, D. V .; Харборн, Дж. Б. (1994). Натуральные продукты: их химический состав и биологическое значение. Харлоу, Эссекс: Longman Scientific & Technical. стр.308–309. ISBN 0-582-06009-5.
- ^ Бут, Джудит К .; Пейдж, Джонатан Э .; Больманн, Йорг (29 марта 2017 г.). Hamberger, Björn (ред.). "Терпенсинтазы из Каннабис сатива". PLOS ONE. 12 (3): e0173911. Bibcode:2017PLoSO..1273911B. Дои:10.1371 / journal.pone.0173911. ISSN 1932-6203. ЧВК 5371325. PMID 28355238.
- ^ Перес-Качо, Пилар Руис; Роузефф, Рассел Л. (10 июля 2008 г.). «Запах свежевыжатого апельсинового сока: обзор». Критические обзоры в области пищевой науки и питания. 48 (7): 681–695. Дои:10.1080/10408390701638902. ISSN 1040-8398. PMID 18663618. S2CID 32567584.
- ^ а б Шарма, Кавита; Махато, Неелима; Чо, Му Хван; Ли, Ён Рок (2017). «Преобразование отходов цитрусовых в продукты с добавленной стоимостью: экономические и экологически безопасные подходы». Питание. 34: 29–46. Дои:10.1016 / j.nut.2016.09.006. ISSN 0899-9007. PMID 28063510.
- ^ Kim, Y.-W .; Kim, M.-J .; Chung, B.-Y .; Bang Du, Y .; Lim, S.-K .; Choi, S.-M .; Lim, D.-S .; Cho, M.-C .; Юн, К .; Kim, H.-S .; Kim, K.-B .; Kim, Y.-S .; Kwack, S.-J .; Ли, Б.-М. (2013). «Оценка безопасности и оценка рисков D-Лимонен ». Журнал токсикологии и гигиены окружающей среды, часть B. 16 (1): 17–38. Дои:10.1080/10937404.2013.769418. PMID 23573938. S2CID 40274650.
- ^ Деза, Густаво; Гарсиа Браво, Бегонья; Сильвестр, Хуан Ф .; Пастор Ньето, Мария А .; Гонсалес Перес, Рикардо; Герас Мендаса, Фелипе; Меркадер, Педро; Фернандес Редондо, Вирджиния; Никлассон, Бо; Хименес Арнау, Ана М; GEIDAC (2017). «Контактная сенсибилизация к гидропероксидам лимонена и линалоола в Испании: проспективное исследование GEIDAC» (PDF). Контактный дерматит. 76 (2): 74–80. Дои:10.1111 / cod.12714. HDL:10230/33527. PMID 27896835. S2CID 21494625.
- ^ Информационный бюллетень EPA по лимонену, Сентябрь 1994 г.
- ^ Паспорт безопасности материала Avenger http://nebula.wsimg.com/07de45c0af774ba73e06362ad1a56f06?AccessKeyId=C67FD801C8FC93742D64&disposition=0&alloworigin=1
- ^ Батлер, Питер (октябрь 2010 г.). «Это похоже на волшебство. Удаление самоклеящихся марок с бумаги» (PDF). Американский филателист. Американское филателистическое общество. 124 (10): 910–913.
- ^ "С помощью D-Лимонен растворяет опорные конструкции для 3D-печати ». 3D-печать Fargo. 26 апреля 2014 г.. Получено 30 декабря 2015.
- ^ Cyclone Power для демонстрации двигателя внешнего сгорания на мероприятии SAE, Конгресс экологических автомобилей, 20 сентября 2007 г.
- ^ Виннчук, Мария (1994). «Оценка заменителей ксилола для обработки парафиновых тканей». Журнал гистотехнологии (2): 143–149. Дои:10.1179/014788894794710913.
- ^ Карсон, Ф. (1997). Гистотехнология: текст для самообучения. Чикаго, Иллинойс: Пресса ASCP. С. 28–31. ISBN 0-89189-411-X.
- ^ Кирнан, Дж. А. (2008). Гистологические и гистохимические методы. (4-е изд.). Bloxham, Oxon. С. 54, 57. ISBN 978-1-904842-42-2.