Реакция Дильса – Альдера - Diels–Alder reaction
| Реакция Дильса – Альдера | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Названный в честь | Отто Пауль Херманн Дильс Курт Алдер | ||||||||
| Тип реакции | Циклоприсоединение | ||||||||
| Реакция | |||||||||
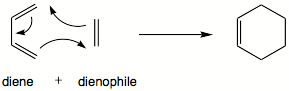
| |||||||||
| Идентификаторы | |||||||||
| Портал органической химии | Дильс-Альдер-реакция | ||||||||
| RSC ID онтологии | RXNO: 0000006 | ||||||||
В органическая химия, то Реакция Дильса – Альдера химическая реакция между сопряженный диен и замененный алкен, обычно называемый диенофил (также пишется диенеофил[1]), чтобы образовать замещенный циклогексен производная. Это прототип перициклическая реакция с согласованный механизм. В частности, он классифицируется как разрешенный по температуре [4 + 2] циклоприсоединение с Символ Вудворда – Гофмана [π4s + π2s]. Впервые он был описан Отто Дильс и Курт Алдер в 1928 году. За открытие этой реакции они были награждены Нобелевская премия по химии в 1950 году. Благодаря одновременному построению двух новых углерод-углеродных связей, реакция Дильса-Альдера обеспечивает надежный способ образования шестичленных колец с хорошим контролем регио- и стереохимических результатов.[2][3] Следовательно, он послужил мощным и широко применяемым инструментом для введения химической сложности в синтез природных продуктов и новых материалов.[4][5] Основная концепция также была применена к π-системам, включающим гетероатомы, такие как карбонилы и имины, которые дают соответствующие гетероциклы; этот вариант известен как гетеро-реакция Дильса – Альдера. Реакция также была обобщена на другие размеры кольца, хотя ни одно из этих обобщений не соответствовало образованию шестичленных колец с точки зрения объема или универсальности. Из-за отрицательных значений ΔЧАС° и ΔS° для типичной реакции Дильса-Альдера микроскопическая обратная реакция реакции Дильса-Альдера становится благоприятной при высоких температурах, хотя это имеет синтетическое значение только для ограниченного диапазона аддуктов Дильса-Альдера, обычно с некоторыми особыми структурными особенностями; эта обратная реакция известна как ретро-реакция Дильса – Альдера.[6]
Механизм
Реакция является примером согласованной перициклической реакции.[7] Считается, что это происходит через одно циклическое переходное состояние,[8] без промежуточных продуктов, образующихся в ходе реакции. Таким образом, реакция Дильса-Альдера регулируется соображениями орбитальной симметрии: она классифицируется как [π4s + π2s] циклоприсоединение, указывающее, что оно проходит через надфасциальный / супрафациальное взаимодействие 4π-электронной системы (диеновая структура) с 2π-электронной системой (диенофильная структура), взаимодействие, которое приводит к переходному состоянию без дополнительного энергетического барьера, обусловленного орбитальной симметрией, и позволяет реакции Дильса-Альдера протекать место с относительной легкостью.[9]
Учет реагентов ' пограничные молекулярные орбитали (FMO) объясняет, почему это так. (Такой же вывод можно сделать из диаграммы орбитальной корреляции или анализа Дьюара-Циммермана.) Для более распространенной реакции Дильса-Альдера «нормального» электронного спроса более важным из двух взаимодействий HOMO / LUMO является взаимодействие между электронами и электронами. богатый диен ψ2 как высшая занятая молекулярная орбиталь (ВЗМО) с π * электронно-дефицитного диенофила в качестве самой низкой незанятой молекулярной орбитали (НСМО). Однако энергетическая щель HOMO – LUMO достаточно близка, чтобы их роли можно было поменять местами, переключая электронные эффекты заместителей на два компонента. В обратная (обратная) реакция Дильса – Альдера электронного спроса электроноакцепторные заместители на диене понижают энергию его пустого ψ3 орбитальные и электронодонорные заместители на диенофиле повышают энергию его заполненной π-орбитали настолько, что взаимодействие между этими двумя орбиталями становится наиболее энергетически значимым стабилизирующим орбитальным взаимодействием. Независимо от того, какая ситуация имеет место, HOMO и LUMO компонентов находятся в фазе, и возникает скрепляющее взаимодействие, как это видно на диаграмме ниже. Поскольку реагенты находятся в основном состоянии, реакция инициируется термически и не требует активации светом.[9]

«Преобладающее мнение»[10][11][12][13] заключается в том, что большинство реакций Дильса-Альдера протекают по согласованному механизму; этот вопрос, однако, был тщательно оспорен. Несмотря на то, что подавляющее большинство реакций Дильса-Альдера демонстрируют стереоспецифическое син-добавление двух компонентов, постулируется бирадикальный интермедиат.[8] (и подтверждено вычислительными данными) на том основании, что наблюдаемая стереоспецифичность не исключает двухэтапного добавления с участием промежуточного продукта, который коллапсирует в продукт быстрее, чем он может вращаться, что позволяет инверсию стереохимии.
При проведении определенных реакций Дильса-Альдера в полярных органических растворителях, таких как диметилформамид и этиленгликоль, наблюдается заметное увеличение скорости.[14] и даже в воде.[15] Например, реакция циклопентадиена и бутенона в воде протекает в 700 раз быстрее по сравнению с 2,2,4-триметилпентаном в качестве растворителя.[15] Было предложено несколько объяснений этого эффекта, например, увеличение эффективной концентрации за счет гидрофобной упаковки.[16] или стабилизация переходного состояния водородными связями.[17]
Геометрия диенового и диенофильного компонентов, каждый, распространяется на стереохимические детали продукта. За межмолекулярный реакции особенно, предпочтительные позиционный а стереохимические отношения заместителей двух компонентов по сравнению друг с другом контролируются электронными эффектами. Однако для внутримолекулярное циклоприсоединение Дильса – Альдера реакции, конформационная устойчивость структуры переходное состояние может иметь подавляющее влияние.
Региоселективность
Теория пограничных молекулярных орбиталей также использовалась для объяснения закономерностей региоселективности, наблюдаемых в реакциях Дильса-Альдера замещенных систем. Расчет энергетических и орбитальных коэффициентов граничных орбиталей компонентов[18] дает картину, которая хорошо согласуется с более прямым анализом резонансных эффектов заместителей, как показано ниже.
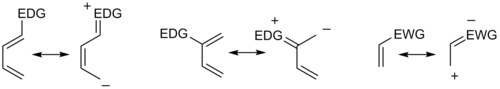
В общем, региоселективность, обнаруженная как для нормальной, так и для обратной реакции Дильса-Альдера с электронной потребностью, соответствует правило орто-пара, названный так потому, что циклогексеновый продукт имеет заместители в положениях, аналогичных положению орто и параграф позиции дизамещенных аренов. Например, в сценарии нормального спроса диен, несущий электронодонорную группу (EDG) в C1, имеет наибольший коэффициент HOMO в C4, в то время как диенофил с электронодонорной группой (EWG) в C1 имеет наибольший коэффициент LUMO при C2. Объединение этих двух коэффициентов дает "орто" произведение, как показано в случае 1 на рисунке ниже. Диен, замещенный у С2, как в случае 2 ниже, имеет самый большой коэффициент ВЗМО у С1, давая "пара" продукт. Подобный анализ для соответствующих сценариев обратного спроса приводит к аналогичным продуктам, как показано в случаях 3 и 4. Изучая канонические мезомерные формы выше, легко убедиться, что эти результаты соответствуют ожиданиям, основанным на рассмотрении электронной плотности и поляризация.

В общем, что касается наиболее энергетически согласованной пары HOMO-LUMO, максимизация энергии взаимодействия путем образования связей между центрами с наибольшими граничными орбитальными коэффициентами позволяет предсказывать основной региоизомер, который будет результатом данной комбинации диен-диенофил.[9] При более сложной обработке три типа заместителей (Z снятие: Понижение HOMO и LUMO (CF3, НЕТ2, CN, C (O) CH3), Икс пожертвование: Поднятие HOMO и LUMO (Me, OMe, NMe2), C сопряжение: Рассматриваются повышение HOMO и понижение LUMO (Ph, винил)), в результате получается 18 возможных комбинаций. Максимизация орбитального взаимодействия правильно предсказывает продукт во всех случаях, для которых доступны экспериментальные данные. Например, в необычных комбинациях, включающих Икс групп как на диене, так и на диенофиле, может быть предпочтительна структура 1,3-замещения, что не объясняется упрощенным аргументом в пользу резонансной структуры.[19] Однако случаи, когда аргумент резонанса и согласование наибольших орбитальных коэффициентов не совпадают, редки.
Стереоспецифичность и стереоселективность
Реакции Дильса-Альдера, как согласованные циклоприсоединения, являются стереоспецифический. Стереохимическая информация о диене и диенофиле сохраняется в продукте в виде син сложение по каждому компоненту. Например, заместители в СНГ (транс, соответственно) отношения на двойной связи диенофила приводят к заместителям, которые СНГ (транс, соответственно) на тех же атомах углерода по отношению к циклогексеновому кольцу. Точно так же СНГ,СНГ- и транс,транс-дезамещенные диены дают СНГ заместители у этих атомов углерода продукта, тогда как СНГ,транс-дизамещенные диены дают транс заместители:[20][21]


Реакции Дильса-Альдера, в которых соседние стереоцентры генерируются на двух концах вновь образованных одинарных связей, подразумевают два различных возможных стереохимических результата. Это стереоселективный ситуация, основанная на взаимной ориентации двух отдельных компонентов, когда они реагируют друг с другом. В контексте реакции Дильса-Альдера переходное состояние, в котором наиболее значимый заместитель (электроноакцепторная и / или сопрягающая группа) диенофила ориентирован в сторону π-системы диена и проскальзывает под ней по мере протекания реакции, является известный как эндо переходное состояние. В альтернативе экзо переходное состояние, он ориентирован от него. (Существует более общее использование терминов эндо и экзо в стереохимической номенклатуре.)
В случаях, когда диенофил имеет один электроноакцепторный / конъюгирующий заместитель или два электроноакцепторных / конъюгированных заместителя СНГ друг к другу, результат часто можно предсказать. В этих сценариях Дильса – Альдера "нормального спроса" эндо переходное состояние обычно является предпочтительным, несмотря на то, что оно часто более стерически перегружено. Это предпочтение известно как Правило ольхи эндо. Как первоначально заявил Альдер, предпочтительным переходным состоянием является состояние с «максимальным накоплением двойных связей». Эндо селективность обычно выше для жестких диенофилов, таких как малеиновый ангидрид и бензохинон; для других, таких как акрилаты и кротонаты, избирательность не очень выражена.[22]
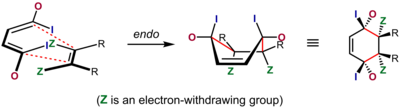
Наиболее широко распространенным объяснением происхождения этого эффекта является благоприятное взаимодействие между π-системами диенофила и диена, взаимодействие, описываемое как вторичный орбитальный эффект, хотя диполярный и ван дер Ваальс привлекательность также может играть роль, и растворитель иногда может существенно повлиять на избирательность.[7][23][24] Объяснение вторичного орбитального перекрытия было впервые предложено Вудвордом и Хоффманном.[25] В этом объяснении орбитали, связанные с группой в конъюгации с двойной связью диенофила, перекрываются с внутренними орбиталями диена, ситуация, которая возможна только для эндо переходное состояние. Хотя в первоначальном объяснении использовалась только орбиталь на атоме α к диенофильной двойной связи, Салем и Хоук впоследствии предположили, что обе орбитали на α- и β-атомах углерода участвуют, когда позволяет молекулярная геометрия.[26]

Часто, как и в случае высокозамещенных диенов, очень объемные диенофилы или обратимые реакции (как и в случае с фуран как диен), стерические эффекты могут отменять нормальные эндо избирательность в пользу экзо изомер.
Диен
В диен компонент реакции Дильса-Альдера может быть как с открытой цепью, так и циклическим, и он может содержать много различных типов заместителей;[7] он должен, однако, существовать в с-СНГ конформация, поскольку это единственный конформер, который может участвовать в реакции. Хотя бутадиены обычно более стабильны в s-транс-конформации, в большинстве случаев разница в энергии невелика (~ 2–5 ккал / моль).[27]
Объемный заместитель в положении C2 или C3 может увеличить скорость реакции за счет дестабилизации s-транс конформация и превращение диена в реакционноспособный s-СНГ конформация. 2-терт-бутил-бута-1,3-диен, например, в 27 раз более реакционноспособен, чем простой бутадиен.[7][28] И наоборот, диен, имеющий объемные заместители как у С2, так и у С3, менее реакционноспособен, потому что стерические взаимодействия между заместителями дестабилизируют s-СНГ конформация.[28]
Диены с объемными концевыми заместителями (C1 и C4) снижают скорость реакции, по-видимому, препятствуя приближению диена и диенофила.[29]
Особенно реакционноспособным диеном является 1-метокси-3-триметилсилоксибута-1,3-диен, иначе известный как Диена Данишефского.[30] Он имеет особую синтетическую полезность в качестве средства получения α, β-ненасыщенных циклогексеноновых систем путем удаления 1-метоксизаместителя после снятия защиты с енолсилилового эфира. Другие синтетически полезные производные диена Данишефского включают 1,3-алкокси-1-триметилсилокси-1,3-бутадиены (диены Брассарда).[31] и 1-диалкиламино-3-триметилсилокси-1,3-бутадиены (Rawal dienes).[32] Повышенная реакционная способность этих и подобных диенов является результатом синергетического вклада донорных групп в C1 и C3, повышая HOMO значительно выше, чем у сопоставимого монозамещенного диена.[4]

Нестабильные (и, следовательно, очень реактивные) диены, из которых, возможно, наиболее синтетически полезны, являются о-хинодиметаны, могут быть созданы на месте.[33] Сильная движущая сила для [4 + 2] циклоприсоединения таких видов является результатом установления (или восстановления) ароматичности. Общие методы создания о-хинодиметаны включают пиролиз бензоциклобутенов[7] или соответствующий сульфон,[4] 1,4-элиминирование орто-бензилсиланов[34] или станнаны,[35][36][37] и восстановление α, α'-орто бензильных дибромидов.[38]

Напротив, стабильные диены довольно инертны и вступают в реакции Дильса – Альдера только при повышенных температурах: например, нафталин может действовать как диен, приводя к аддуктам только с высокореактивными диенофилами, такими как N-фенил-малеимид. Антрацен, будучи менее ароматическим (и, следовательно, более реактивным для синтезов Дильса-Альдера) в своем центральном кольце может образовывать 9,10 аддукт с малеиновый ангидрид при 80 ° C и даже при ацетилен, слабый диенофил, при 250 ° C.[39]
Диенофил
В обычной реакции Дильса-Альдера диенофил имеет электроноакцепторную группу в сочетании с алкеном; в сценарии обратной потребности диенофил конъюгирован с электронодонорной группой.[10] Можно выбрать диенофилы, содержащие «замаскированную функциональность». Диенофил подвергается реакции Дильса-Альдера с диеном, вводя такую функциональность в молекулу продукта. Затем следует серия реакций, чтобы преобразовать функциональность в желаемую группу. Конечный продукт не может быть получен за одну стадию DA, потому что эквивалентный диенофил либо нереактивен, либо недоступен. Примером такого подхода является использование α-хлоракрилонитрила (CH2= CClCN). При взаимодействии с диеном этот диенофил вводит α-хлорнитрильную функциональную группу в молекулу продукта. Это «замаскированная функциональность», которая затем может быть гидролизована с образованием кетона. α-Хлоракрилонитрил диенофил является эквивалентом кетендиенофила (CH2= C = O), что даст тот же продукт за один шаг DA. Проблема в том, что сам кетен не может быть использован в реакциях Дильса-Альдера, потому что он реагирует с диенами нежелательным образом (посредством [2 + 2] циклоприсоединения), и поэтому необходимо использовать подход «замаскированной функциональности».[40] Другими такими функциональными группами являются заместители фосфония (дающие экзоциклические двойные связи после реакции Виттига), различные сульфоксидные и сульфонильные функциональные группы (обе являются эквивалентами ацетилена) и нитрогруппы (эквиваленты кетена).[7]
Варианты классической реакции Дильса – Альдера.
Гетеро-Дильс – Ольха
Реакции Дильса – Альдера с участием хотя бы одного гетероатом также известны и в совокупности называются гетеро-реакциями Дильса – Альдера.[41] Карбонильные группы, например, может успешно реагировать с диенами с образованием дигидропиран кольца, реакция, известная как оксо-реакция Дильса – Альдера, и имины может использоваться либо в качестве диенофила, либо в различных участках диена с образованием различных N-гетероциклические соединения через аза-реакция Дильса – Альдера. Нитрозосоединения (R-N = O) могут реагировать с диенами с образованием оксазины. Хлорсульфонилизоцианат может использоваться в качестве диенофила для приготовления Винс лактам.[7][42]
Активация кислоты Льюиса
Кислоты Льюиса такие как хлорид цинка, трифторид бора, тетрахлорид олова, хлорид алюминия и т. д. могут действовать как катализаторы нормальных реакций Дильса – Альдера путем координации с диенофилом. Комплексный диенофил становится более электрофильным и более реактивным по отношению к диену, увеличивая скорость реакции и часто также улучшая регио- и стереоселективность. Кислотный катализ Льюиса также позволяет реакциям Дильса-Альдера протекать при низких температурах, то есть без термической активации.[7]
Асимметричный Дильс – Ольха
Многие методы были разработаны для воздействия на стереоселективность реакции Дильса – Альдера, такие как использование хиральных вспомогательных веществ, катализ путем хиральные кислоты Льюиса,[43] и катализаторы на малых органических молекулах.[7] Оксазолидиноны Эванса,[44] оксазаборолидины,[45][46][47] бис-оксазолин -медь хелаты,[48] имидазолин катализ,[49] и существует множество других методик проведения диастерео- и энантиоселективных реакций Дильса-Альдера.
Hexadehydro Diels – Alder
в гексадегидро реакция Дильса – Альдера, алкины и diynes используются вместо алкенов и диенов, образуя нестабильные бензин промежуточное соединение, которое затем может улавливаться с образованием ароматического продукта. Эта реакция позволяет образовывать сильно функционализированные ароматические кольца за одну стадию.[50]
Приложения
Ретро-реакция Дильса – Альдера используется в промышленном производстве циклопентадиен. Циклопентадиен является предшественником различных норборнены, которые распространены мономеры. Реакция Дильса – Альдера также используется для получения витамин B6.
История

Работа Дильса и Альдера описана в серии из 28 статей, опубликованных в Юстус Либигс Аннален дер Хеми и Berichte der deutschen chemischen Gesellschaft с 1928 по 1937 год. Первые 19 статей были написаны Дильсом и Олдером, в то время как более поздние статьи были автором Дильса и различных авторов.[52][53]
Первое применение реакции Дильса – Альдера в полном синтезе было проиллюстрировано Р. Б. Вудворд синтез стероидов кортизон и холестерин.[54] Взаимодействие бутадиена с хиноном, указанным ниже, дает кольцам C и D стероидного скелета желаемую региохимию.

Э. Дж. Кори в его оригинальном синтезе 1969 г. простагландины F2α и E2,[55] использовали реакцию Дильса-Альдера на ранней стадии синтеза, чтобы установить относительную стереохимию трех смежных стереоцентров на простагландин-циклопентановом ядре. Для смягчения изомеризации замещенного циклопентадиена через 1,5-гидридный сдвиг было сочтено необходимым поддерживать этот промежуточный продукт ниже 0 ° C до тех пор, пока не произойдет процесс Дильса – Альдера. Таким образом, для протекания реакции требовалась активация сильно кислым тетрафторборатом меди по Льюису. Использование 2-хлоракрилонитрила в качестве диенофила является жизнеспособным синтетический эквивалент для кетена,[10] структура, которая обычно не способствует [2 + 2] циклоприсоединению с образованием димера циклобутанона, а не участвует в реакциях Дильса-Альдера с 1,3-диенами.[56][57] Гидролиз эпимерной смеси аддуктов хлорнитрила позволил получить желаемый бициклогептанон с высоким выходом.

Сэмюэл Дж. Данишефски использовали реакцию Дильса-Альдера для синтеза динатрий префенат,[58] биосинтетический предшественник аминокислот фенилаланина и тирозина, в 1979 году. Эта последовательность примечательна как одна из первых, в которой в полном синтезе был использован 1-метокси-3-силоксибутадиен, так называемый диен Данишефского. Его полезность будет очевидна ниже, а именно, для получения α, β-ненасыщенных циклогексеноновых систем.
В их синтезе 1980 г. Резерпин,[59] Пол Вендер и сотрудники использовали реакцию Дильса-Альдера, чтобы установить цис-декалиновый каркас D и E колец природного продукта. Первоначальная схема Дильса-Альдера между 2-ацетоксиакриловой кислотой и 1,2-дигидропиридин-1-карбоксилатом, показанная ниже, ставит вновь установленную карбоксильную группу в положение для перегруппировки исключительно в цис-конденсированные кольца после преобразования в изохинуклиден, показанный ниже. Цис-слияние позволило установить стереохимию у C17 и C18: сначала путем отщепления ацетатной группы у C18 с образованием кетона, который может модулировать стереохимию метоксигруппы C17, а затем путем восстановления кетона у C18 из экзо-лицо для достижения стереохимии конечного продукта.

В Стивен Ф. Мартин синтез Резерпин,[60] цис-конденсированные кольца D и E также образовывались по реакции Дильса – Альдера. Внутримолекулярное соединение пиранона по Дильсу-Альдеру ниже с последующей экструзией диоксида углерода через ретро [4 + 2] дает бициклический лактам. Эпоксидирование с менее затрудненной α-грани с последующим раскрытием эпоксида на менее затрудненной C18 дало желаемую стереохимию в этих положениях, в то время как цис-синтез достигался с помощью гидрогенизации, опять же, в основном, с менее затрудненной стороны.

Пиранон также использовался в качестве диенофила К. К. Николау группа в полный синтез таксола.[61] Межмолекулярная реакция гидроксипирона и α, β-ненасыщенного сложного эфира, показанная ниже, страдает низким выходом и региоселективностью; однако, когда направлено фенилбороновой кислотой[62] желаемый аддукт может быть получен с выходом 61% после расщепления бороната 2,2-диметил-1,3-пропандиолом. Стереоспецифичность реакции Дильса-Альдера в этом случае позволила определить четыре стереоцентра, которые были перенесены в конечный продукт.

Реакция Дильса – Альдера была ключевым шагом в Амос Смит синтез (-) - фурахиноцина C.[63] Дион 1 был превращен в необходимый диен путем енолизации с использованием двух последовательных силилирований с TMSCl. Циклоприсоединение Дильса – Альдера к бромхинону сопровождалось спонтанным дегидрогалогенирование переформировать ароматическое кольцо. Диен в этом случае примечателен как редкий пример циклического производного диена Данишефского.

Виреш Равал и Сергей Козьмин, в синтезе таберсонина 1998 г.,[64] использовал Дильса-Альдера для установления цис-относительной стереохимии алкалоидного ядра. Превращение цис-альдегида в его соответствующий алкен олефинированием по Виттигу и последующим метатезис замыкающего кольца с Катализатор Шрока дал второе кольцо ядра алкалоида. Диен в этом случае примечателен как пример 1-амино-3-силоксибутадиена, иначе известного как диен Равала.

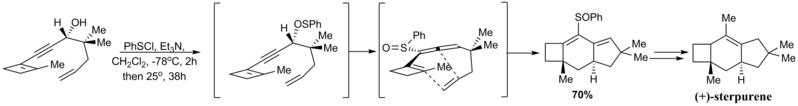
В 1988 г. Уильям Окамура и Ричард Гиббс сообщили об энантиоселективном синтезе (+) - стерпурена[65] это характеризует замечательную внутримолекулярную реакцию аллена Дильса – Альдера. В [2,3] -сигматропная перегруппировка тиофенильной группы с получением сульфоксида, как показано ниже, происходило энантиоспецифично из-за заданной стереохимии пропаргилового спирта. Таким образом, образующийся единичный изомер аллена может привести к появлению диена-диена только на одной стороне образовавшегося «диена».
Эндрю Майерс синтез 2005 года (-) - тетрациклин[66] получили линейное тетрациклическое ядро антибиотика с помощью реакции Дильса-Альдера. При термическом инициировании одновременного открытия бензоциклобутена образуется о-хинодиметан, который взаимодействует межмолекулярно с образованием тетрациклинового скелета; показанный диастереомер затем кристаллизовали из метанола после очистки колоночной хроматографией. Авторы отмечают, что свободная гидроксильная группа диенофила была неотъемлемой частью успеха реакции, поскольку гидроксил-защищенные варианты не реагировали в нескольких различных условиях реакции.

Takemura et al. синтезировал кантарадрин в 1980 году Дильс-Альдером, используя высокое давление.[67]
Синтетические применения реакции Дильса – Альдера были подробно рассмотрены.[68][69][70][71][72]
Смотрите также
- Циклоприсоединение Брэдшера
- Реакция Вагнера-Яурегга
- Реакция Имина Дильса – Альдера
- Реакция Аза-Дильса – Альдера
использованная литература
- ^ Уайтинг, Эндрю; Виндзор, Карл М. (28 мая 1998 г.). «Что заставляет нейтральный имино-диенеофил подвергнуться термической, некаталитической реакции Дильса-Альдера?». Тетраэдр. 54 (22): 6035–6050. Дои:10.1016 / S0040-4020 (98) 00284-1. ISSN 0040-4020.
- ^ Kloetzel, M. C. (1948). «Реакция Дильса – Альдера с малеиновым ангидридом». Органические реакции. 4. С. 1–59. Дои:10.1002 / 0471264180.or004.01. ISBN 978-0471264187.
- ^ Холмс, Х. Л. (1948). «Реакция Дильса-Альдера, этиленовые и ацетиленовые диенофилы». Органические реакции. 4. С. 60–173. Дои:10.1002 / 0471264180.or004.02. ISBN 978-0471264187.
- ^ а б c Nicolaou, K. C .; Снайдер, С. А .; Montagnon, T .; Василикогианнакис, Г. (2002). «Реакция Дильса-Альдера в полном синтезе». Angewandte Chemie International Edition. 41 (10): 1668–1698. Дои:10.1002 / 1521-3773 (20020517) 41:10 <1668 :: AID-ANIE1668> 3.0.CO; 2-Z. PMID 19750686.
- ^ Атилла Тасделен, Мехмет (2011). «Щелкающие реакции Дильса – Альдера: недавние применения в полимерах и материаловедении». Полимерная химия. 2 (10): 2133–2145. Дои:10.1039 / C1PY00041A.CS1 maint: несколько имен: список авторов (ссылка на сайт)
- ^ Цвайфель, Г. С .; Нантц, М. Х. (2007). Современный органический синтез: введение. W.H. Фриман и Ко. ISBN 978-0-7167-7266-8.
- ^ а б c d е ж г час я Кэри, Часть B., стр. 474–526.
- ^ а б Dewar, M. J .; Olivella, S .; Стюарт, Дж. Дж. (1986). «Механизм реакции Дильса-Альдера: реакции бутадиена с этиленом и цианоэтиленами». Журнал Американского химического общества. 108 (19): 5771–5779. Дои:10.1021 / ja00279a018. PMID 22175326.
- ^ а б c Кэри, Часть A., стр. 836–50
- ^ а б c Кэри, Часть A., с. 839
- ^ Gajewski, J. J .; Петерсон, К. Б .; Кагель, Дж. Р. (1987). «Изменение структуры переходного состояния в реакции Дильса-Альдера из-за вторичных кинетических изотопных эффектов дейтерия: реакция почти симметричного диена и диенофила почти синхронна». Журнал Американского химического общества. 109 (18): 5545–5546. Дои:10.1021 / ja00252a052.
- ^ Houk, K. N .; Лин, Ю. Т .; Браун, Ф. К. (1986). «Доказательства согласованного механизма реакции Дильса-Альдера бутадиена с этиленом». Журнал Американского химического общества. 108 (3): 554–556. Дои:10.1021 / ja00263a059. PMID 22175504.
- ^ Goldstein, E .; Beno, B .; Хоук, К. Н. (1996). "Прогнозирование функциональной теории плотности относительных энергий и изотопных эффектов для согласованных и ступенчатых механизмов реакции Дильса-Альдера бутадиена и этилена". Журнал Американского химического общества. 118 (25): 6036–6043. Дои:10.1021 / ja9601494.
- ^ Breslow, R .; Го, Т. (1988). «Реакции Дильса-Альдера в неводных полярных растворителях. Кинетические эффекты хаотропных и антихаотропных агентов и β-циклодекстрина». Журнал Американского химического общества. 110 (17): 5613–5617. Дои:10.1021 / ja00225a003.
- ^ а б Райдаут, Д. С .; Бреслоу, Р. (1980). «Гидрофобное ускорение реакций Дильса-Альдера». Журнал Американского химического общества. 102 (26): 7816–7817. Дои:10.1021 / ja00546a048.
- ^ Breslow, R .; Риццо, К. Дж. (1991). «Хаотропные солевые эффекты в гидрофобно ускоренной реакции Дильса-Альдера». Журнал Американского химического общества. 113 (11): 4340–4341. Дои:10.1021 / ja00011a052.
- ^ Блокзейл, Вильфрид; Энгбертс, Ян Б. Ф. Н. (1992). «Влияние начального и переходного состояний на реакции Дильса – Альдера в воде и смешанных водных растворителях». Журнал Американского химического общества. 114 (13): 5440–5442. Дои:10.1021 / ja00039a074.
- ^ Ashby, E.C .; Chao, L.-C .; Нойман, Х. М. (1973). «Механизмы металлоорганических реакций. XII. Механизм присоединения метилмагнийбромида к бензонитрилу». Журнал Американского химического общества. 95 (15): 4896–4904. Дои:10.1021 / ja00796a022.
- ^ Флеминг, И. (1990). Пограничные орбитальные и органические химические реакции. Чичестер, Великобритания: Wiley. ISBN 978-0471018193.
- ^ Kirmse, W .; Mönch, D. (1991). "Umlagerungen von 1,4,4- и 2,2,5-триметилбицикло [3.2.1] окт-6-ил-катионен". Chemische Berichte. 124 (1): 237–240. Дои:10.1002 / cber.19911240136.
- ^ Bérubé, G .; DesLongchamps, P. (1987). "Stéréosélection acyclique-1,5: Synthèse de la chaîne latérale optique active de la vitamine E". Bulletin de la Société Chimique de France. 1: 103–115.
- ^ Houk, K. N .; Лускус, Л. Дж. (1971). «Влияние стерических взаимодействий на эндостереоселективность». Журнал Американского химического общества. 93 (18): 4606–4607. Дои:10.1021 / ja00747a052.
- ^ Kobuke, Y .; Сугимото, Т .; Furukawa, J .; Фуэно, Т. (1972). «Роль притягивающих взаимодействий в эндо-экзостереоселективности реакций Дильса-Альдера». Журнал Американского химического общества. 94 (10): 3633–3635. Дои:10.1021 / ja00765a066.
- ^ Уильямсон, К. Л .; Сюй, Ю.-Ф. Л. (1970). "Стереохимия реакции Дильса-Альдера. II. Кислотный катализ Льюиса син-анти-изомерии". Журнал Американского химического общества. 92 (25): 7385–7389. Дои:10.1021 / ja00728a022.
- ^ 1917–1979, Вудворд, Р. Б. (Роберт Бернс) (22 октября 2013 г.). Сохранение орбитальной симметрии. Хоффманн, Р. Вайнхайм. ISBN 9781483282046. OCLC 915343522.CS1 maint: числовые имена: список авторов (ссылка на сайт)
- ^ Wannere, Chaitanya S .; Пол, Анкан; Хергес, Райнер; Houk, K. N .; Шефер, Генри Ф .; Шлейер, Пол фон Раге (2007). «Существование вторичных орбитальных взаимодействий». Журнал вычислительной химии. 28 (1): 344–361. Дои:10.1002 / jcc.20532. ISSN 1096-987X. PMID 17109435. S2CID 26096085.
- ^ Кэри, Часть A, стр. 149
- ^ а б Бэкер, Х. Дж. (1939). "Le 2,3-Ditertiobutylbutadiène". Recueil des Travaux Chimiques des Pays-Bas. 58 (7): 643–661. Дои:10.1002 / recl.19390580712.
- ^ Craig, D .; Шипман, Дж. Дж .; Фаулер, Р. Б. (1961). «Скорость реакции малеинового ангидрида с 1,3-диенами в зависимости от конформации диена». Журнал Американского химического общества. 83 (13): 2885–2891. Дои:10.1021 / ja01474a023.
- ^ Данишефский, С .; Китахара, Т. (1974). «Полезный диен для реакции Дильса – Альдера». Журнал Американского химического общества. 96 (25): 7807–7808. Дои:10.1021 / ja00832a031.
- ^ Savard, J .; Брассар, П. (1979). «Региоспецифический синтез хинонов с использованием ацеталей винилкетена, полученных из ненасыщенных сложных эфиров». Буквы Тетраэдра. 20 (51): 4911–4914. Дои:10.1016 / S0040-4039 (01) 86747-2.
- ^ Козьмин, С. А .; Равал, В. Х. (1997). «Получение и реакционная способность Дильса-Альдера 1-амино-3-силокси-1,3-бутадиенов». Журнал органической химии. 62 (16): 5252–5253. Дои:10.1021 / jo970438q.
- ^ Клундт, И. Л. (1970). «Бензоциклобутен и его производные». Химические обзоры. 70 (4): 471–487. Дои:10.1021 / cr60266a002.
- ^ Ито, Й .; Nakatsuka, M .; Саегуса Т. (1982). «Синтезы полициклических кольцевых систем на основе нового поколения о-хинодиметаны ». Журнал Американского химического общества. 104 (26): 7609–7622. Дои:10.1021 / ja00390a036.
- ^ Sano, H .; Ohtsuka, H .; Мигита, Т. (1988). «Удобный метод генерации о-хинодиметанов индуцированным протоном 1,4-элиминированием о- (1-гидроксиалкил) бензилтрибутилстаннаны ». Журнал Американского химического общества. 110 (6): 2014–2015. Дои:10.1021 / ja00214a083.
- ^ Вскоре, H. W. (1993). "Новый метод создания о-хинодиметан путем селен-индуцированной фрагментации о-винилбензилтрибутилстаннан ». Буквы Тетраэдра. 34 (47): 7587–7590. Дои:10.1016 / S0040-4039 (00) 60407-0.
- ^ Вскоре, H. W. (1994). "Генерация α-окси-о-хинодиметаны и реакции циклоприсоединения ». Буквы Тетраэдра. 35 (23): 3975–3978. Дои:10.1016 / S0040-4039 (00) 76717-7.
- ^ Rubottom, G.M .; Уэй, Дж. Э. (1984). "Улучшенный метод приготовления о-Хинодиметаны ». Синтетические коммуникации. 14 (6): 507–514. Дои:10.1080/00397918408059572.
- ^ Маргарета Аврам (1983). Хими органика п. 318-323. Editura Academiei Republicii Socialiste România
- ^ Ranganathan, S .; Ranganathan, D .; Мехротра, А. К. (1977). «Эквиваленты Кетене». Синтез. 1977 (5): 289–296. Дои:10.1055 / с-1977-24362.
- ^ Руш, В. Р. (1991). «Внутримолекулярные реакции Дильса – Альдера». In Trost, B.M .; Флемминг, И. (ред.). Комплексный органический синтез. Vol. 5. С. 513–550. Дои:10.1016 / B978-0-08-052349-1.00131-1. ISBN 978-0-08-052349-1.
- ^ Grieco, P.A .; Ларсен, С. Д. (1990). "Реакции Дильса – Альдера на основе иминиума: N-бензил-2-азанорборен" (PDF). Органический синтез. 68: 206. Дои:10.15227 / orgsyn.068.0206.
- ^ Уайт, Джеймс Д .; Шоу, Субрата (2011). «Цис-2,5-диаминобицикло [2.2.2] октан, новый каркас для асимметричного катализа с помощью комплексов Сален-металл». Орг. Lett. 13 (9): 2488–91. Дои:10.1021 / ol2007378. PMID 21462988.
- ^ Эванс, Д. А .; Chapman, K. T .; Бисаха, Дж. (1988). «Асимметричные реакции циклоприсоединения Дильса – Альдера с хиральными α, β-ненасыщенными N-ацилоксазолидинонами». Журнал Американского химического общества. 110 (4): 1238–1256. Дои:10.1021 / ja00212a037.
- ^ Кори, Э. Дж .; Ло, Т. П. (1991). «Первое применение привлекательных внутримолекулярных взаимодействий для разработки хиральных катализаторов высокоэнантиоселективных реакций Дильса-Альдера». Журнал Американского химического общества. 113 (23): 8966–8967. Дои:10.1021 / ja00023a066.
- ^ Кори, Э. Дж .; Shibata, T .; Ли, Т. В. (2002). «Асимметричные реакции Дильса-Альдера, катализируемые трифликовой кислотой, активированной хиральным оксазаборолидином». Журнал Американского химического общества. 124 (15): 3808–3809. Дои:10.1021 / ja025848x. PMID 11942799.
- ^ Ryu, D. H .; Кори, Э. Дж. (2003). «Трифлимидная активация хирального оксазаборолидина приводит к более общей каталитической системе для энантиоселективного добавления Дильса-Альдера». Журнал Американского химического общества. 125 (21): 6388–6390. Дои:10.1021 / ja035393r. PMID 12785777.
- ^ Johnson, J. S .; Эванс, Д. А. (2000). «Хиральные бис (оксазолин) комплексы меди (II): универсальные катализаторы для энантиоселективного циклоприсоединения, реакций Альдола, Михаэля и карбонилена». Отчеты о химических исследованиях. 33 (6): 325–335. Дои:10.1021 / ar960062n. PMID 10891050.
- ^ Арендт, К. А .; Borths, C.J .; Макмиллан, Д. В. С. (2000). "Новые стратегии органического катализа: первая высокоэнантиоселективная органокаталитическая реакция Дильса-Альдера". Журнал Американского химического общества. 122 (17): 4243–4244. Дои:10.1021 / ja000092s.
- ^ Hoye, T. R .; Baire, B .; Niu, D .; Уиллоуби, П. Х .; Вудс, Б. П. Природа, 2012, 490, 208 [1]
- ^ Бер, Арно (2000). «Металлоорганические соединения и гомогенный катализ». Энциклопедия промышленной химии Ульмана. Дои:10.1002 / 14356007.a18_215. ISBN 978-3527306732.
- ^
- Diels, O .; Алдер, К. (1928). "Synthesen in der hydroaromatischen Reihe, I". Юстус Либигс Аннален дер Хеми. 460: 98–122. Дои:10.1002 / jlac.19284600106.
- Diels, O .; Ольдер, К. (1929). "Synthesen in der hydroaromatischen Reihe, II". Berichte der Deutschen Chemischen Gesellschaft. 62 (3): 554–562. Дои:10.1002 / cber.19290620318.
- Diels, O .; Ольдер, К. (1929). "Synthesen in der hydroaromatischen Reihe, III". Юстус Либигс Аннален дер Хеми. 470: 62–103. Дои:10.1002 / jlac.19294700106.
- Diels, O .; Ольдер, К. (1929). "Synthesen in der hydroaromatischen Reihe, IV". Berichte der Deutschen Chemischen Gesellschaft. 62 (8): 2081–2087. Дои:10.1002 / cber.19290620829.
- Diels, O .; Ольдер, К. (1929). "Synthesen in der hydroaromatischen Reihe, V". Berichte der Deutschen Chemischen Gesellschaft. 62 (8): 2087–2090. Дои:10.1002 / cber.19290620830.
- Diels, O .; Ольдер, К. (1929). "Synthesen in der hydroaromatischen Reihe, VI". Berichte der Deutschen Chemischen Gesellschaft. 62 (8): 2337–2372. Дои:10.1002 / cber.19290620872.
- Diels, O .; Алдер, К. (1930). "Synthesen in der hydroaromatischen Reihe, VII". Юстус Либигс Аннален дер Хеми. 478: 137–154. Дои:10.1002 / jlac.19304780109.
- Diels, O .; Алдер, К. (1931). "Synthesen in der hydroaromatischen Reihe, VIII". Юстус Либигс Аннален дер Хеми. 486: 191–202. Дои:10.1002 / jlac.19314860110.
- Diels, O .; Алдер, К. (1931). "Synthesen in der hydroaromatischen Reihe, IX". Юстус Либигс Аннален дер Хеми. 486: 202–210. Дои:10.1002 / jlac.19314860111.
- Diels, O .; Алдер, К. (1931). "Synthesen in der hydroaromatischen Reihe, X". Юстус Либигс Аннален дер Хеми. 486: 211–225. Дои:10.1002 / jlac.19314860112.
- Diels, O .; Алдер, К. (1931). "Synthesen in der hydroaromatischen Reihe, XI". Юстус Либигс Аннален дер Хеми. 490: 236–242. Дои:10.1002 / jlac.19314900109.
- Diels, O .; Алдер, К. (1931). "Synthesen in der hydroaromatischen Reihe, XII". Юстус Либигс Аннален дер Хеми. 490: 243–257. Дои:10.1002 / jlac.19314900110.
- Diels, O .; Алдер, К. (1931). "Synthesen in der hydroaromatischen Reihe, XIII". Юстус Либигс Аннален дер Хеми. 490: 257–266. Дои:10.1002 / jlac.19314900111.
- Diels, O .; Алдер, К. (1931). "Synthesen in der hydroaromatischen Reihe, XIV". Юстус Либигс Аннален дер Хеми. 490: 267–276. Дои:10.1002 / jlac.19314900112.
- Diels, O .; Алдер, К. (1931). "Synthesen in der hydroaromatischen Reihe, XV". Юстус Либигс Аннален дер Хеми. 490: 277–294. Дои:10.1002 / jlac.19314900113.
- Diels, O .; Алдер, К. (1932). "Synthesen in der hydroaromatischen Reihe, XVI". Юстус Либигс Аннален дер Хеми. 498: 1–15. Дои:10.1002 / jlac.19324980102.
- Diels, O .; Алдер, К. (1932). "Synthesen in der hydroaromatischen Reihe, XVII". Юстус Либигс Аннален дер Хеми. 498: 16–49. Дои:10.1002 / jlac.19324980103.
- Diels, O .; Ольдер, К. (1933). "Synthesen in der hydroaromatischen Reihe, XVIII". Юстус Либигс Аннален дер Хеми. 505: 103–150. Дои:10.1002 / jlac.19335050109.
- Diels, O .; Ольдер, К. (1934). "Synthesen in der hydroaromatischen Reihe, XIX". Юстус Либигс Аннален дер Хеми. 510: 87–128. Дои:10.1002 / jlac.19345100106.
- Diels, O .; Риз, Дж. (1934). "Synthesen in der hydroaromatischen Reihe, XX". Юстус Либигс Аннален дер Хеми. 511: 168–182. Дои:10.1002 / jlac.19345110114.
- Diels, O .; Мейер, Р. (1934). "Synthesen in der hydroaromatischen Reihe, XXI". Юстус Либигс Аннален дер Хеми. 513: 129–145. Дои:10.1002 / jlac.19345130108.
- Diels, O .; Фридрихсен, В. (1934). "Synthesen in der hydroaromatischen Reihe, XXII". Юстус Либигс Аннален дер Хеми. 513: 145–155. Дои:10.1002 / jlac.19345130109.
- Diels, O .; Мёллер, Ф. (1935). "Synthesen in der hydroaromatischen Reihe, XXIII". Юстус Либигс Аннален дер Хеми. 516: 45–61. Дои:10.1002 / jlac.19355160104.
- Diels, O .; Кеч, Х. (1935). "Synthesen in der hydroaromatischen Reihe, XXIV". Юстус Либигс Аннален дер Хеми. 519: 140–146. Дои:10.1002 / jlac.19355190112.
- Diels, O .; Риз, Дж. (1935). "Synthesen in der hydroaromatischen Reihe, XXV". Юстус Либигс Аннален дер Хеми. 519: 147–157. Дои:10.1002 / jlac.19355190113.
- Diels, O .; Хармс, Дж. (1935). "Synthesen in der hydroaromatischen Reihe, XXVI". Юстус Либигс Аннален дер Хеми. 525: 73–94. Дои:10.1002 / jlac.19365250107.
- Diels, O .; Шрам, Х. (1937). "Synthesen in der hydroaromatischen Reihe, XXVII". Юстус Либигс Аннален дер Хеми. 530: 68–86. Дои:10.1002 / jlac.19375300106.
- Diels, O .; Пистор, Х. (1937). "Synthesen in der hydroaromatischen Reihe, XXVIII". Юстус Либигс Аннален дер Хеми. 530: 87–98. Дои:10.1002 / jlac.19375300107.
- ^ "Нобелевская премия по химии 1950 г.". Нобелевский фонд. Получено 19 февраля 2016.
- ^ Woodward, R. B .; Sondheimer, F .; Taub, D .; Heusler, K .; МакЛамор, В. М. (1952). «Полный синтез стероидов». Журнал Американского химического общества. 74 (17): 4223–4251. Дои:10.1021 / ja01137a001.
- ^ Кори, Э. Дж .; Weinshenker, N.M .; Schaaf, T. K .; Хубер, В. (1969). «Стерео-контролируемый синтез простагландинов F-2a и E-2 (dl)». Журнал Американского химического общества. 91 (20): 5675–7. Дои:10.1021 / ja01048a062. PMID 5808505.
- ^ Nicolaou, K. C .; Соренсен, Э. Дж. (1996). Классика в полном синтезе: цели, стратегии, методы. Wiley VCH. ISBN 978-3-527-29231-8.
- ^ De Lucchi, O .; Паскуато, Л. (1988). «Роль функциональных групп серы в активации и направлении олефинов в реакциях циклоприсоединения». Тетраэдр. 44 (22): 6755–6794. Дои:10.1016 / S0040-4020 (01) 86204-9.
- ^ Данишефский, С .; Hirama, M .; Fritsch, N .; Кларди, Дж. (1979). «Синтез динатрия префената и динатрия эпипрефената. Стереохимия префеновой кислоты и наблюдение катализируемой основанием перегруппировки префеновой кислоты в п-гидроксифенилмолочную кислоту». Журнал Американского химического общества. 101 (23): 7013–7018. Дои:10.1021 / ja00517a039.
- ^ Wender, P.A .; Schaus, J.M .; Уайт, А. В. (1980). «Общая методология синтеза цис-гидроизохинолина: синтез резерпина». Журнал Американского химического общества. 102 (19): 6157–6159. Дои:10.1021 / ja00539a038.
- ^ Мартин, С. Ф .; Rueger, H .; Williamson, S.A .; Гжейщак, С. (1987). «Общие стратегии синтеза индольных алкалоидов. Полный синтез (±) -резерпина и (±) -α-йохимбина». Журнал Американского химического общества. 109 (20): 6124–6134. Дои:10.1021 / ja00254a036.
- ^ Nicolaou, K. C .; Ян, З .; Liu, J. J .; Ueno, H .; Nantermet, P. G .; Guy, R.K .; Claiborne, C.F .; Renaud, J .; Couladouros, E.A .; Paulvannan, K .; Соренсен, Э. Дж. (1994). «Полный синтез таксола». Природа. 367 (6464): 630–4. Bibcode:1994Натура.367..630Н. Дои:10.1038 / 367630a0. PMID 7906395. S2CID 4371975.
- ^ Narasaka, K .; Shimada, S .; Osoda, K .; Ивасава, Н. (1991). «Фенилбороновая кислота в качестве матрицы в реакции Дильса-Альдера». Синтез. 1991 (12): 1171–1172. Дои:10.1055 / с-1991-28413.
- ^ Smith, A.B .; Sestelo, J.P .; Дормер, П. Г. (1995). «Полный синтез (-) - фурахиноцина С». Журнал Американского химического общества. 117 (43): 10755–10756. Дои:10.1021 / ja00148a023.
- ^ Козьмин, С. А .; Равал, В. Х. (1998). «Общая стратегия для алкалоидов Aspidosperma: эффективный стереоконтролируемый синтез таберсонина». Журнал Американского химического общества. 120 (51): 13523–13524. Дои:10.1021 / ja983198k.
- ^ Gibbs, R.A .; Окамура, В. Х. (1988). «Короткий энантиоселективный синтез (+) - стерпурена: полный внутримолекулярный перенос центральных хиральных элементов в осевые и центральные». Журнал Американского химического общества. 110 (12): 4062–4063. Дои:10.1021 / ja00220a069.
- ^ Charest, M. G .; Siegel, D. R .; Майерс, А. Г. (2005). «Синтез (-) - тетрациклина». Журнал Американского химического общества. 127 (23): 8292–3. Дои:10.1021 / ja052151d. PMID 15941256.
- ^ Dauben, W. G .; Kessel, C.R .; Такемура, К. Х. (1980). «Простой и эффективный полный синтез кантаридина с помощью реакции Дильса-Альдера при высоком давлении». Журнал Американского химического общества. 102 (22): 6893–6894. Дои:10.1021 / ja00542a060.
- ^ Холмс, Х. Л. (1948). «Реакция Дильса – Альдера, этиленовые и ацетиленовые диенофилы». Органические реакции. 4. С. 60–173. Дои:10.1002 / 0471264180.or004.02. ISBN 978-0471264187.
- ^ Butz, L.W .; Рытина, А. В. (1949). "Хиноны реакции Дильса-Альдера и другие цикленоны". Органические реакции. 5. С. 136–192. Дои:10.1002 / 0471264180.or005.03. ISBN 978-0471264187.
- ^ Kloetzel, M. C. (1948). «Реакция Дильса – Альдера с малеиновым ангидридом». Органические реакции. 4. С. 1–59. Дои:10.1002 / 0471264180.or004.01. ISBN 978-0471264187.
- ^ Heintzelman, G.R .; Meigh, I.R .; Махаджан, Ю. Р .; Вайнреб, С. В. (2005). "Реакции Дильса-Альдера имино диенофилов". Органические реакции. 65. С. 141–599. Дои:10.1002 / 0471264180.or065.02. ISBN 978-0471264187.
- ^ Циганек, Э. (1984). «Внутримолекулярная реакция Дильса-Альдера». Органические реакции. 32. С. 1–374. Дои:10.1002 / 0471264180.or032.01. ISBN 978-0471264187.
Список используемой литературы
- Кэри, Фрэнсис А.; Сандберг, Ричард Дж. (2007). Расширенная органическая химия: Часть B: Реакции и синтез (5-е изд.). Нью-Йорк: Спрингер. ISBN 978-0387683546.
внешняя ссылка
- [2] Английский перевод основополагающей статьи Дильса и Альдера на немецком языке в 1928 году, которая принесла им Нобелевскую премию. Английское название: «Синтезы гидроароматического ряда»; Немецкое название "Synthesen in der hydroaromatischen Reihe".
