Октан - Octane
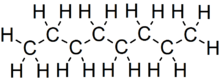 | |
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Октан[1] | |
| Идентификаторы | |
3D модель (JSmol ) | |
| 3DMet | |
| 1696875 | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.003.539 |
| Номер ЕС |
|
| 82412 | |
| КЕГГ | |
| MeSH | октан |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1262 |
| |
| |
| Свойства | |
| C8ЧАС18 | |
| Молярная масса | 114.232 г · моль−1 |
| Внешность | бесцветная жидкость |
| Запах | Как бензин[2] |
| Плотность | 0,703 г см−3 |
| Температура плавления | От -57,1 до -56,6 ° С; От -70,9 до -69,8 ° F; От 216,0 до 216,6 К |
| Точка кипения | От 125,1 до 126,1 ° С; От 257,1 до 258,9 ° F; От 398,2 до 399,2 К |
| 0,007 мг дм−3 (при 20 ° C) | |
| журнал п | 4.783 |
| Давление газа | 1,47 кПа (при 20,0 ° C) |
Закон Генри постоянный (kЧАС) | 29 нмоль Па−1 кг−1 |
| Конъюгированная кислота | Октониум |
| -96.63·10−6 см3/ моль | |
| 1.398 | |
| Вязкость |
|
| Термохимия | |
Теплоемкость (C) | 255,68 Дж К−1 моль−1 |
Стандартный моляр энтропия (S | 361.20 Дж К−1 моль−1 |
Станд. Энтальпия формирование (ΔжЧАС⦵298) | −252,1–−248,5 кДж моль−1 |
Станд. Энтальпия горение (ΔcЧАС⦵298) | −5,53–−5,33 МДж моль−1 |
| Опасности | |
| Пиктограммы GHS |     |
| Сигнальное слово GHS | Опасность |
| H225, H304, H315, H336, H410 | |
| P210, P261, P273, P301 + 310, P331 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | 13,0 ° С (55,4 ° F, 286,1 К) |
| 220,0 ° С (428,0 ° F, 493,1 К) | |
| Пределы взрываемости | 0.96–6.5% |
| Смертельная доза или концентрация (LD, LC): | |
LDLo (самый низкий опубликованный ) | 428 мг / кг (мышь, внутривенно)[4] |
| NIOSH (Пределы воздействия на здоровье в США): | |
PEL (Допустимо) | TWA 500 частей на миллион (2350 мг / м3)[2] |
REL (Рекомендуемые) | TWA 75 частей на миллион (350 мг / м3) C 385 частей на миллион (1800 мг / м3) [15 минут][2] |
IDLH (Непосредственная опасность) | 1000 частей на миллион[2] |
| Родственные соединения | |
Родственные алканы | |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
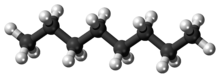
Октан это углеводород и алкан с химическая формула C8ЧАС18, а конденсированная структурная формула CH3(CH2)6CH3. Octane имеет много структурные изомеры которые различаются количеством и расположением разветвлений в углеродной цепи. Один из этих изомеров, 2,2,4-триметилпентан (обычно называемый изооктаном) используется в качестве одного из стандартных значений в октановое число масштаб.
Октан входит в состав бензин (бензин). Как и все низкомолекулярные углеводороды, октан летучий и очень легко воспламеняется.
Использование термина в бензине
«Октан» в просторечии используется как сокращенная форма «октановое число, "особенно в выражении" высокооктановое число "." Октановое число "- это показатель способности топлива сопротивляться стук двигателя при высоком сжатии, что характерно для изомеров с разветвленной цепью октана, особенно изооктана.
Первоначально октановое число было определено путем смешивания топлива только из гептана и 2,2,4-триметилпентана (сильно разветвленный октан) и присвоения антидетонационных характеристик ноль для чистого гептана и 100 для чистого 2,2,4-триметилпентана. Степень защиты от детонации этой смеси будет такой же, как процентное содержание последней в смеси. Различные изомеры октана могут способствовать более низкому или более высокому октановому числу. Например, п-октан (прямая цепь из 8 атомов углерода без разветвления) имеет -20 (отрицательный) Октановый рейтинг исследований, тогда как чистый 2,2,4-триметилпентан имеет рейтинг октанового числа 100. Некоторые виды топлива имеют октановое число выше 100, особенно те, которые содержат метанол или этанол.
Метафорическое использование
Октан стал широко известен в американской поп-культуре в середине и конце 1960-х годов, когда бензин компании хвастались «высоким октановым числом» в рекламе бензина.
Сложное прилагательное «высокооктановое», означающее мощный или динамичный, в переносном смысле записано с 1944 года.[5] К середине 90-х эта фраза широко использовалась как усилитель и нашел свое место в современном английском языке.
Изомеры
Октан имеет 18 структурных изомеров (24 включая стереоизомеры ):
- Октан (п-октан)
- 2-метилгептан
- 3-метилгептан (2 энантиомеры )
- 4-метилгептан
- 3-этилгексан
- 2,2-диметилгексан
- 2,3-диметилгексан (2 энантиомера)
- 2,4-диметилгексан (2 энантиомера)
- 2,5-диметилгексан
- 3,3-диметилгексан
- 3,4-диметилгексан (2 энантиомера + 1 мезосоединение )
- 3-этил-2-метилпентан
- 3-этил-3-метилпентан
- 2,2,3-триметилпентан (2 энантиомера)
- 2,2,4-триметилпентан (изооктан)
- 2,3,3-триметилпентан
- 2,3,4-триметилпентан
- 2,2,3,3-тетраметилбутан
использованная литература
- ^ «октан - Резюме соединения». PubChem Compound. США: Национальный центр биотехнологической информации. 16 сентября 2004 г. Идентификационные и связанные записи. Получено 6 января 2012.
- ^ а б c d Карманный справочник NIOSH по химической опасности. "#0470". Национальный институт охраны труда и здоровья (NIOSH).
- ^ Dymond, J. H .; Ой, Х.А. (1994). «Вязкость выбранной жидкости n-Alkanehhhh s». Журнал физических и химических справочных данных. 23 (1): 41–53. Дои:10.1063/1.555943. ISSN 0047-2689.
- ^ «Октан». Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ Оксфордский словарь английского языка.
внешние ссылки
- Международная карта химической безопасности 0933
- Карманный справочник NIOSH по химической опасности. "#0470". Национальный институт охраны труда и здоровья (NIOSH).
- Фитохимические и этноботанические базы данных доктора Дьюка, Octane, http://www.ars-grin.gov/cgi-bin/duke/chemical.pl?OCTANE[постоянная мертвая ссылка ]








