Паровой риформинг - Steam reforming
Паровой риформинг или паровой риформинг метана это метод производства синтез-газ (водород и монооксид углерода ) по реакции углеводороды с водой. Обычно натуральный газ это сырье. Основное предназначение этой технологии - производство водорода. Реакция представлена этим равновесием:[1]
- CH4 + H2O ⇌ CO + 3 H2
Реакция сильно эндотермический (потребляет тепло, ΔHр= 206 кДж / моль).
Паровой риформинг натуральный газ производит большую часть водорода в мире. Водород используется в промышленный синтез аммиака и другие химические вещества.[2]
Производственная практика
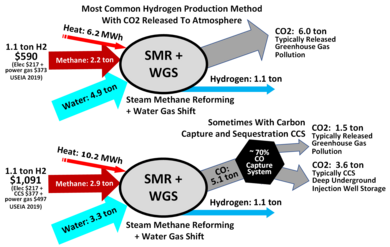
Реакция проводится в реакторе риформинга, где смесь пара и пара под высоким давлением метан вступают в контакт с никель катализатор. Катализаторы с высоким отношение площади поверхности к объему предпочтительны из-за распространение ограничения из-за высоких Рабочая Температура. Примеры катализатор используются колеса со спицами, шестерни и кольца с отверстиями. Кроме того, эти формы имеют низкую падение давления что выгодно для этого приложения.[3]
Через реакция конверсии водяного газа дополнительный водород может быть получен путем обработки монооксида углерода, образующегося при паровом риформинге, водой:
- CO + H2O ⇌ CO2 + H2
Эта реакция мягко говоря экзотермический (выделяет тепло, ΔHр= -41 кДж / моль).
В Соединенные Штаты производит 9—10 миллионов тонн водорода в год, в основном за счет паровой конверсии природного газа.[4] Мировое производство аммиака с использованием водорода, полученного в результате парового риформинга, в 2014 году составило 144 миллиона тонн.[5] Потребление энергии было снижено со 100 ГДж / т аммиака в 1920 году до 27 ГДж к 2019 году.[6]
Эффективность парового риформинга природного газа составляет 65–75%.[7]
Производство H2 и CO из углеводородных газов (например, природного газа) осуществляется двумя хорошо известными установками риформинга «первичный» и «вторичный». Паровой риформинг метана (SMR) и автотермический риформинг (ATR) являются двумя промышленными примерами первичного и вторичного риформинга, соответственно. С другой стороны, в процессе комбинированного риформинга используются как первичные, так и вторичные инструменты для производства синтез-газа, как это обычно практикуется при производстве аммиака. В случае метанола в ATR подается почти чистый кислород (99,5%), а не воздух, поскольку присутствие избыточного азота2 в синтез-газе будет перекрывать сжатие и замедлять производство метанола. Установка риформинга ATR состоит из камеры частичного окисления (POX) (обычно некаталитической среды) и каталитической секции с неподвижным слоем. Каталитический неподвижный слой не только регулирует H2/ CO, но также уничтожает любую возможную сажу и прекурсоры (например, этилен и ацетилен), которые могут образоваться в камере POX. Природный газ (ПГ) частично окисляется в камере сгорания кислородом или воздухом (в качестве окислителя). Отношение пара к углероду (S / C), которое обычно составляет 0,6 в случае с кислородом, было коммерциализировано компанией Haldor-Topose.[8]
Автотермический риформинг
Автотермический риформинг (ATR) использует кислород и диоксид углерода или пар в реакции с метаном с образованием синтез-газ. Реакция протекает в одной камере, где метан частично окисляется. Реакция экзотермична из-за окисления. Когда ATR использует диоксид углерода, H2Соотношение продуцируемого СО: 1: 1; когда ATR использует пар, H2Соотношение продуцируемого газа: CO составляет 2,5: 1.
Реакции можно описать следующими уравнениями с использованием CO2:
- 2 канала4 + O2 + CO2 → 3 H2 + 3 СО + Н2О
И с помощью Steam:
- 4 канала4 + O2 + 2 часа2O → 10 H2 + 4 СО
Температура синтез-газа на выходе составляет 950-1100 ° C, а давление на выходе может достигать 100 ° C. бар.[9]
Основное различие между SMR и ATR заключается в том, что SMR использует только воздух для сгорания в качестве источника тепла для создания пара, в то время как ATR использует очищенный кислород. Преимущество ATR в том, что H2: CO можно варьировать, что может быть полезно при производстве специальных продуктов. Например, производство диметиловый эфир требуется 1: 1 H2: Соотношение CO.
Частичное окисление
Частичное окисление (POX) происходит, когда субстехиометрическая топливно-воздушная смесь частично сгорает в риформинг-установке с образованием синтез-газа, обогащенного водородом. POX обычно намного быстрее парового риформинга и требует меньшего размера реактора. POX производит меньше водорода на единицу входящего топлива, чем паровой риформинг того же топлива.[10]
Паровой риформинг в малых масштабах
Капитальные затраты на установки парового риформинга считаются непомерно высокими для малых и средних предприятий. Затраты на эти сложные объекты не уменьшаются. Обычные установки парового риформинга работают при давлении от 200 до 600 фунтов на квадратный дюйм (14-40 бар) с температурами на выходе в диапазоне от 815 до 925 ° C.
Для двигателей внутреннего сгорания
Факельный газ и вентилируемый Летучие органические соединения являются известными проблемами в морской отрасли и в наземной нефтегазовой отрасли, так как в обоих случаях парниковые газы выбрасываются в атмосферу.[11] При риформинге двигателей внутреннего сгорания используется технология парового риформинга для преобразования отходящих газов в источник энергии.[12]
Риформинг для двигателей внутреннего сгорания основан на паровом риформинге, где неметановые углеводороды (NMHCs ) некачественных газов превращаются в синтез-газ (ЧАС2 + CO) и, наконец, метан (CH4), углекислый газ (CO2) и водород (ЧАС2) - тем самым улучшая качество топливного газа (метановое число).[13]
Для топливных элементов
Существует также интерес к разработке гораздо меньших единиц на основе аналогичной технологии для производства водород как сырье для топливные элементы.[14] Малогабаритные установки парового риформинга на поставку топливные элементы в настоящее время являются предметом исследований и разработок, обычно связанных с реформированием метанол, но рассматриваются и другие виды топлива, такие как пропан, бензин, автогаз, дизельное топливо, и этиловый спирт.[15][16]
Недостатки
Система реформинга с топливными элементами все еще исследуется, но в ближайшем будущем системы будут продолжать работать на существующих видах топлива, таких как природный газ, бензин или дизельное топливо. Тем не менее, ведутся активные дебаты о том, выгодно ли использование этих видов топлива для производства водорода, в то время как глобальное потепление является проблемой. Реформирование ископаемого топлива не устраняет выбросы диоксида углерода в атмосферу, но снижает выбросы диоксида углерода и почти исключает выбросы монооксида углерода по сравнению со сжиганием традиционных видов топлива за счет повышения эффективности и характеристик топливных элементов.[17] Однако, превратив выброс углекислого газа в точечный источник а не распределенный выпуск, улавливание и хранение углерода становится возможным, что предотвратит выброс диоксида углерода в атмосферу, увеличивая при этом стоимость процесса.
Стоимость производства водорода путем реформинга ископаемого топлива зависит от масштаба, в котором это делается, капитальных затрат на установку реформинга и эффективности установки, так что, хотя это может стоить всего несколько долларов за килограмм водорода в промышленных масштабах, он мог бы быть более дорогим при меньшем масштабе, необходимом для топливных элементов.[18]
Проблемы с установками риформинга, поставляющими топливные элементы
Однако с этой технологией связано несколько проблем:
- Реакция риформинга протекает при высоких температурах, что замедляет ее запуск и требует дорогостоящих высокотемпературных материалов.
- Сера соединения в топливе отравляют определенные катализаторы, что затрудняет запуск системы этого типа из обычных бензин. В некоторых новых технологиях эта проблема решена с помощью катализаторов, устойчивых к сере.
- Коксование может быть другой причиной дезактивации катализатора во время парового риформинга. Высокие температуры реакции, низкое отношение водяного пара к углероду (S / C) и сложный характер серосодержащих промышленных углеводородных топлив делают коксование особенно благоприятным. Олефины, обычно этилен, и ароматические углеводороды являются хорошо известными предшественниками углерода, поэтому их образование должно быть уменьшено во время SR. Кроме того, сообщалось, что катализаторы с более низкой кислотностью менее склонны к закоксовыванию из-за подавления реакций дегидрирования. H2S, основной продукт риформинга органической серы, может связываться со всеми катализаторами переходных металлов с образованием связей металл-сера и впоследствии снижать активность катализатора за счет ингибирования хемосорбции реагентов риформинга. Между тем, адсорбированные частицы серы увеличивают кислотность катализатора и, следовательно, косвенно способствуют закоксовыванию. Катализаторы на основе драгоценных металлов, такие как Rh и Pt, имеют более низкую тенденцию к образованию объемных сульфидов, чем другие металлические катализаторы, такие как Ni. Rh и Pt менее подвержены отравлению серой, поскольку только хемосорбируют серу, а не образуют сульфиды металлов.[19]
- Низкая температура полимерный топливный элемент мембраны могут быть отравлены монооксид углерода (CO) производится в реакторе, что делает необходимым включение сложных систем удаления CO. Твердооксидные топливные элементы (ТОТЭ) и топливные элементы с расплавленным карбонатом (MCFC) не имеют этой проблемы, но работают при более высоких температурах, замедляя время запуска и требуя дорогостоящих материалов и громоздкой изоляции.
- В термодинамическая эффективность процесса составляет от 70% до 85% (Основа LHV ) в зависимости от чистоты водородного продукта.
Смотрите также
- Биогаз
- Каталитический риформинг
- Химический риформинг и газификация
- Крекинг (химия)
- Водород
- Щепотка водорода
- Водородные технологии
- Промышленный газ
- Лейн производитель водорода
- Пиролиз метана
- Частичное окисление
- ПРОКС
- Реформированный метанольный топливный элемент
- Цикл риформинга губчатого железа
- Хронология водородных технологий
Рекомендации
- ^ Лю, Кэ; Песня, Чуньшань; Субрамани, Велу, ред. (2009). Технологии производства и очистки водорода и синтез-газа. Дои:10.1002/9780470561256. ISBN 9780470561256.
- ^ Крэбтри, Джордж У.; Dresselhaus, Mildred S .; Бьюкенен, Мишель В. (2004). Водородная экономика (PDF) (Технический отчет).
- ^ Реймерт, Райнер; Маршнер, Фридеманн; Реннер, Ханс-Иоахим; Болл, Уолтер; Supp, Эмиль; Брейк, Мирон; Либнер, Вальдемар; Шауб, Георг (2011). «Добыча газа, 2. Процессы». Энциклопедия промышленной химии Ульмана. Дои:10.1002 / 14356007.o12_o01. ISBN 978-3-527-30673-2.
- ^ «Факт месяца, май 2018: 10 миллионов метрических тонн водорода ежегодно производится в Соединенных Штатах». Energy.gov.
- ^ Азот (фиксированный) - аммиак (PDF) (Отчет). Геологическая служба США. Январь 2016 г.
- ^ Рамсков, Йенс (16 декабря 2019 г.). "Vinder af VIDENSKABENS TOP 5: Водород и метанол uden energifrås". Ingeniøren (на датском).
- ^ «Производство водорода - паровой риформинг метана (SMR)» (PDF), Информационный бюллетень по водороду, заархивировано из оригинал (PDF) 4 февраля 2006 г., получено 28 августа 2014
- ^ Эбрахими, Хади; Бехрузсаранд, Алиреза; Заманиян, Акбар (2010). «Устройство установок первичного и вторичного риформинга для производства синтез-газа». Химико-технические исследования и разработки. 88 (10): 1342–1350. Дои:10.1016 / j.cherd.2010.02.021.
- ^ Топсе ATR
- ^ «Производство водорода: риформинг природного газа».
- ^ «Атмосферные выбросы». Архивировано из оригинал на 26.09.2013.
- ^ «Wärtsilä запускает продукт газового риформинга для преобразования добываемого газа в энергию». Морское понимание. 18 марта 2013. Архивировано с оригинал на 2015-05-11.
- ^ «Способ эксплуатации газомоторной установки и система подачи топлива газового двигателя».
- ^ «Переработчик ископаемого топлива». 2000-10-04.
- ^ Вышинский, Мирослав Л .; Мегаритис, Танос; Лерле, Рой С. (2001). Водород из топливного риформинга выхлопных газов: более экологичные, экономичные и плавные двигатели (PDF) (Технический отчет). Future Power Systems Group, Бирмингемский университет.
- ^ «Реформирование общеупотребительного топлива сегодня». 2000-10-04.
- ^ Реформирование ископаемого топлива без удаления диоксида углерода
- ^ Доти, Ф. Дэвид (2004). «Реалистичный взгляд на прогнозы цен на водород». CiteSeerX 10.1.1.538.3537. Цитировать журнал требует
| журнал =(Помогите)[самостоятельно опубликованный источник? ] - ^ Чжэн, Цинхэ; Янке, Кристиана; Фаррауто, Роберт (2014). «Паровой риформинг серосодержащего додекана на катализаторе Rh – Pt: влияние параметров процесса на стабильность катализатора и структуру кокса». Прикладной катализ B: Окружающая среда. 160-161: 525–533. Дои:10.1016 / j.apcatb.2014.05.044.

