Виниловый спирт - Википедия - Vinyl alcohol
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Этенол | |||
| Другие имена Гидроксиэтен Гидроксиэтилен | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.008.350 | ||
PubChem CID | |||
| |||
| |||
| Характеристики | |||
| C2ЧАС4О | |||
| Молярная масса | 44,053 г / моль | ||
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
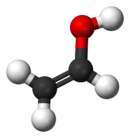
Виниловый спирт, также называемый этенол (Название ИЮПАК), самый простой энол. С формула CЧАС2CHО H, это лабильное соединение, которое превращается в ацетальдегид. Это не предшественник поливиниловый спирт.
Синтез
Виниловый спирт может быть образован пиролитической устранение воды из этиленгликоль при температуре 900 ° С и низком давлении.[1]
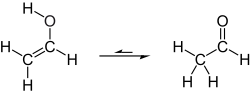
Таутомеризация винилового спирта в ацетальдегид
В обычных условиях виниловый спирт преобразует (таутомеризуется ) в ацетальдегид:
При комнатной температуре ацетальдегид (H3CC (O) H) более устойчив, чем виниловый спирт (H2C = CHOH) на 42,7 кДж / моль:[2]
- ЧАС2С = СНОН → Н3CC (O) H ΔЧАС298, г = -42,7 кДж / моль

Некатализированный кето-енольная таутомерия миграция 1,3-водорода запрещена Правила Вудворда – Хоффмана и поэтому имеет высокий активационный барьер и не является значимым путем при комнатной температуре или около нее. Однако даже следовые количества кислот или оснований (включая воду) могут катализировать реакцию. Даже при строгих мерах предосторожности, направленных на минимизацию посторонних источников влаги или протонов, виниловый спирт можно хранить от нескольких минут до часов, прежде чем он изомеризуется в ацетальдегид. (Угольная кислота является еще одним примером вещества, которое кинетически стабильно в строго чистом виде, но быстро разлагается из-за катализа следами влаги.)
Таутомеризация также может катализироваться с помощью фотохимического процесса. Эти данные свидетельствуют о том, что кето-енольная таутомеризация является жизнеспособным путем в атмосферных и стратосферных условиях, что связано с ролью винилового спирта в производстве органических кислот в атмосфере.[4][5]
Виниловый спирт можно стабилизировать, контролируя концентрацию воды в системе и используя кинетическую благоприятность дейтерий -производится кинетический изотопный эффект (kЧАС+/kD+ = 4.75, kЧАС2О/kD2О = 12). Стабилизация дейтерия может быть достигнута путем гидролиза кетен прекурсор в присутствии небольшого стехиометрического избытка тяжелая вода (D2О). Исследования показывают, что процесс таутомеризации значительно ингибируется при температуре окружающей среды ( kт ≈ 10−6 М / с), а период полураспада формы енола можно легко увеличить до т1/2 = 42 минуты для кинетики гидролиза первого порядка.[6]
Отношение к поли (виниловому спирту)
Из-за нестабильности винилового спирта термопласт поливиниловый спирт (ПВС или ПВС) получают косвенно путем полимеризации винилацетат с последующим гидролиз из сложный эфир связи (Ac = ацетил; HOAc = уксусная кислота):
- п CH2= CHOAc → (CH2-CHOAc)п
- (CH2-CHOAc)п + п ЧАС2O → (CH2-CHOH)п + п HOAc
Как лиганд
Несколько металлические комплексы известны, что содержат виниловый спирт как лиганд. Одним из примеров является Pt (acac) (η2-C2ЧАС3OH) Cl.[7]
Возникновение в межзвездной среде
Виниловый спирт обнаружен в молекулярное облако Стрелец Б.[8] Его стабильность в (разбавленном) межзвездная среда показывает, что его таутомеризации не происходит мономолекулярно.
Смотрите также
Рекомендации
- ^ Клейден, Джонатан; Гривс, Ник; Уоррен, Стюарт. Органическая химия, 2-е издание, с. 456-57. Издательство Оксфордского университета, 2012. ISBN 978-0-19-927029-3.
- ^ Р.Д. Джонсон III. «Стандартная справочная база данных CCCBDB NIST». Получено 2014-08-30.
- ^ Дж. А. Кейт, П. М. Генри (2009). "Механизм реакции Ваккера: рассказ о двух гидроксипалладиях". Энгью. Chem. Int. Эд. 48: 9038–9049. Дои:10.1002 / anie.200902194. PMID 19834921.CS1 maint: использует параметр авторов (связь)
- ^ Heazlewood, B. R .; Maccarone, A.T .; Andrews, D. U .; Осборн, Д. Л .; Harding, L.B .; Klippenstein, S.J .; Jordan, M. J. T .; Kable, S.H. "Около порогового H / D обмен в CD3Фотодиссоциация CHO. Nat. Chem. 2011, 3, 443–448. Дои:10.1038 / nchem.1052
- ^ Эндрюс Д. У., Хизлвуд Б. Р., Маккарон А. Т., Конрой Т., Пейн Р. Дж., Джордан М. Дж. Т., Кейбл С. Х. (2012). «Фото-таутомеризация ацетальдегида в виниловый спирт: потенциальный путь к тропосферным кислотам». Наука. 337: 1203–1206. Дои:10.1126 / science.1220712. PMID 22903524.CS1 maint: несколько имен: список авторов (связь)
- ^ Седерстав, Анна К .; Новак, Брюс М. (1994). «Исследования химии термодинамически нестабильных видов. Прямая полимеризация винилового спирта, энольного таутомера ацетальдегида». Журнал Американского химического общества. 100 (9): 4073–4074. Дои:10.1021 / ja00088a051.
- ^ Коттон Ф. А., Фрэнсис Дж. Н., Френц Б. А., Цуцуи М. (1973). «Структура дигапто (винилового спирта) комплекса платины (II)». Журнал Американского химического общества. 95: 2483–6. Дои:10.1021 / ja00789a011.CS1 maint: несколько имен: список авторов (связь)
- ^ «Ученые тосты за открытие винилового спирта в межзвездном пространстве». Национальная радиоастрономическая обсерватория. 2001-10-01. Получено 2006-12-20.