Двухатомный углерод - Diatomic carbon
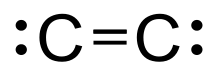 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Двухатомный углерод | |
| Систематическое название ИЮПАК Этендиилиден (заместитель) Дикарбон (C—C) (добавка) | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| 196 | |
PubChem CID | |
| |
| |
| Свойства | |
| C2 | |
| Молярная масса | 24.022 г · моль−1 |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Двухатомный углерод (систематически названный дикарбон и 1λ2, 2λ2-этен), зеленый, газообразный неорганический химический с химическая формула C = C (также пишется [C2] или C2. Он кинетически нестабилен при температуре и давлении окружающей среды, удаляется автополимеризацией. Это происходит в парах углерода, например в электрические дуги; в кометы, звездные атмосферы, а межзвездная среда; и синим углеводород пламя.[1]Двухатомный углерод - вторая простейшая форма углерода после атомарный углерод, и является промежуточным участником генезиса фуллеренов.
Свойства
C2 является компонентом паров углерода. Согласно одной из статей, углеродный пар на 28% состоит из двухатомных атомов.[2] но теоретически это зависит от температуры и давления.
Электромагнитные свойства
Электроны в двухатомном углероде распределяются между атомными орбиталями в соответствии с Принцип Ауфбау для создания уникальных квантовых состояний с соответствующими уровнями энергии. Состояние с самым низким уровнем энергии или основное состояние является синглетным состоянием (1Σ+
г), который систематически называют этен-1,2-диилиденом или дикарбоном (0 •). Существует несколько возбужденных синглетных и триплетных состояний, которые относительно близки по энергии к основному состоянию, которые образуют значительную долю образца дикарбона в условиях окружающей среды. Когда большинство этих возбужденных состояний подвергаются фотохимической релаксации, они излучают в инфракрасной области электромагнитного спектра. Однако одно государство, в частности, излучает в зеленой зоне. Это состояние является триплетным (3Πг), который систематически называют этен-μ, μ-диил-μ-илиденом или дикарбон (2 •). Кроме того, возбужденное состояние несколько дальше по энергии от основного состояния, которое формирует только значительную часть образца дикарбона при среднем ультрафиолетовом облучении. После релаксации это возбужденное состояние флуоресцирует в фиолетовой области и фосфоресцирует в синей области. Это состояние также является синглетным (1Πг), который также называют этен-μ, μ-диил-μ-илиденом или дикарбон (2 •).
государство Возбуждение
энтальпия
(кДж моль−1)Расслабление
переходРасслабление
длина волныРелаксационная EM-область Икс1Σ+
г0 – – – а3Π
ты8.5 а3Π
ты→Икс1Σ+
г14,0 мкм Длинноволновый инфракрасный б3Σ−
г77.0 б3Σ−
г→а3Π
ты1,7 мкм Коротковолновый инфракрасный А1Π
ты100.4 А1Π
ты→Икс1Σ+
г
А1Π
ты→б3Σ−
г1,2 мкм
5,1 мкмБлижний инфракрасный
Средневолновый инфракрасныйB1Σ+
г? B1Σ+
г→А1Π
ты
B1Σ+
г→а3Π
ты?
??
?c3Σ+
ты159.3 c3Σ+
ты→б3Σ−
г
c3Σ+
ты→Икс1Σ+
г
c3Σ+
ты→B1Σ+
г1,5 мкм
751,0 нм
?Коротковолновый инфракрасный
Ближний инфракрасный
?d3Π
г239.5 d3Π
г→а3Π
ты
d3Π
г→c3Σ+
ты
d3Π
г→А1Π
ты518.0 нм
1,5 мкм
860.0 нмЗеленый
Коротковолновый инфракрасный
Ближний инфракрасныйC1Π
г409.9 C1Π
г→А1Π
ты
C1Π
г→а3Π
ты
C1Π
г→c3Σ+
ты386,6 нм
298,0 нм
477,4 нмВиолетта
Средний ультрафиолет
Синий
Молекулярная орбитальная теория показывает, что есть два набора парных электронов в вырожденном пи-связывающем наборе орбиталей. Это дает порядок связи 2, что означает, что должна существовать двойная связь между двумя атомами углерода в C2 молекула.[3] Согласно одному анализу, вместо этого четырехкратная связь существуют,[4] интерпретация, которая была оспорена.[5]
CASSCF расчеты показывают, что четверная связь, основанная на теории молекулярных орбиталей, также является разумной.[3]
Энергии диссоциации связи из B2, С2, и N2 показать увеличение BDE, указывая не замужем, двойной, и тройные облигации соответственно.
В некоторых формах кристаллического углерода, таких как алмаз и графит, седловая точка или «горб» возникает в месте связи в плотности заряда. Триплетное состояние C2 действительно следует этой тенденции. Однако синглетное состояние C2 действует больше как кремний или германий; то есть плотность заряда имеет максимум в месте связи.[6]
Реакции
Двухатомный углерод вступает в реакцию с ацетон и ацетальдегид производить ацетилен двумя разными путями.[2]
- Триплет C2 молекулы будут реагировать по межмолекулярному пути, который, как показано, проявляет бирадикальный характер. Промежуточным звеном для этого пути является этиленовый радикал. Его абстракция коррелирует с энергиями связи.[2]
- Синглетный C2 молекулы будут реагировать по внутримолекулярному, нерадикальному пути, по которому два атома водорода будут отниматься от одной молекулы. Промежуточным звеном для этого пути является синглетный винилиден. Синглетная реакция может происходить через 1,1-диабстракцию или 1,2-диабстракцию. Эта реакция нечувствительна к изотопному замещению. Различные абстракции, возможно, связаны с пространственной ориентацией столкновений, а не с энергиями связи.[2]
- Синглет C2 также будет реагировать с алкены. Ацетилен - основной продукт; однако, похоже, C2 вставит углерод-водородные связи.
- C2 в 2,5 раза чаще вставляется в метильная группа как в метиленовые группы.[7]
История

Свет комет, богатых газом, в основном возникает из-за излучения двухатомного углерода. Примером является С / 2 квартал 2014 г. (Лавджой), где есть несколько строк C2 свет, в основном в видимый спектр[8], формируя Лебединые группы.[9]
Смотрите также
- Ацетилид - родственное химическое вещество с формулой C2−
2
использованная литература
- ^ Хоффманн, Роальд (1995). "Маргиналии: C2 Во всех его обличьях » (PDF). Американский ученый. 83 (4): 309–311. Bibcode:1995AmSci..83..309H. JSTOR 29775475.
- ^ а б c d Скелл, Филип С.; Плонка, Джеймс Х. (1970). «Химия синглета и триплета C2 молекулы. Механизм образования ацетилена из реакции с ацетоном и ацетальдегидом ». Журнал Американского химического общества. 92 (19): 5620–5624. Дои:10.1021 / ja00722a014.
- ^ а б Чжун, Жунлинь; Чжан, Мин; Сюй, Хунлян; Су, Чжунминь (2016). "Скрытая гармония в дикарбоне между теориями VB и MO через ортогональную гибридизацию 3σг и 2σты". Химическая наука. 7 (2): 1028–1032. Дои:10.1039 / c5sc03437j. ЧВК 5954846. PMID 29896370.
- ^ Шайк, Сэсон; Данович, Давид; Ву, Вэй; Су, Пэйфэн; Рзепа, Генри С.; Гиберти, Филипп С. (2012). "Четверное соединение в C2 и аналогичные частицы с восьмью валентными электронами ». Химия природы. 4 (3): 195–200. Bibcode:2012НатЧ ... 4..195С. Дои:10.1038 / nchem.1263. PMID 22354433.
- ^ Грюненберг, Йорг (2012). «Квантовая химия: четырехсвязный углерод». Химия природы. 4 (3): 154–155. Bibcode:2012НатЧ ... 4..154Г. Дои:10.1038 / nchem.1274. PMID 22354425.
- ^ Челиковский, Джеймс Р.; Troullier, N .; Wu, K .; Саад, Ю. (1994). "Метод конечных разностей псевдопотенциалов высшего порядка: приложение к двухатомным молекулам". Физический обзор B. 50 (16): 11356–11364. Bibcode:1994PhRvB..5011355C. Дои:10.1103 / PhysRevB.50.11355. PMID 9975266.
- ^ Скелл, П.С.; Fagone, F.A .; Клабунде, К. Дж. (1972). «Реакция двухатомного углерода с алканами и эфирами / Улавливание алкилкарбенов винилиденом». Журнал Американского химического общества. 94 (22): 7862–7866. Дои:10.1021 / ja00777a032.
- ^ Венкатарамани, Кумар; Гетия, Сатеш; Ганеш, Шашикиран; и другие. (2016). «Оптическая спектроскопия кометы C / 2014 Q2 (Лавджой) из инфракрасной обсерватории Маунт Абу». Ежемесячные уведомления Королевского астрономического общества. 463 (2): 2137–2144. arXiv:1607.06682. Дои:10.1093 / mnras / stw1820.
- ^ Микуз, Герман; Динтиньяна, Боян (1994). «ПЗС-фотометрия комет». International Comet Quarterly. Получено 26 октября, 2006.

