Бутадиен - Butadiene
| |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Бута-1,3-диен[1] | |||
Другие имена
| |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| 605258 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.138 | ||
| Номер ЕС |
| ||
| 25198 | |||
| КЕГГ | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1010 | ||
| |||
| |||
| Характеристики | |||
| C4ЧАС6 | |||
| Молярная масса | 54,0916 г / моль | ||
| Внешность | Бесцветный газ или охлажденная жидкость | ||
| Запах | Слегка ароматный или похожий на бензин | ||
| Плотность |
| ||
| Температура плавления | -108,9 ° С (-164,0 ° F, 164,2 К) | ||
| Точка кипения | -4,4 ° С (24,1 ° F, 268,8 К) | ||
| 1.3 г / л при 5 ℃, 735 мг / л при 20 ℃ | |||
| Растворимость |
| ||
| Давление газа | 2.4 атм (20 ° C)[2] | ||
| 1.4292 | |||
| Вязкость | 0.25 cп при 0 ° C | ||
| Опасности | |||
| Главный опасности | Легковоспламеняющийся, раздражающий, канцероген | ||
| Паспорт безопасности | Видеть: страница данных ECSC 0017 | ||
| Пиктограммы GHS |   | ||
| Сигнальное слово GHS | Опасность | ||
| H220, H340, H350 | |||
| P201, P202, P210, P281, P308 + 313, P377, P381, P403, P405, P501 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | -85 ° C (-121 ° F; 188 K) температура вспышки жидкости[2] | ||
| 420 ° С (788 ° F, 693 К) | |||
| Пределы взрываемости | 2–12% | ||
| Смертельная доза или концентрация (LD, LC): | |||
LD50 (средняя доза ) | 548 мг / кг (крыса, перорально) | ||
LC50 (средняя концентрация ) | |||
LCLo (самый низкий опубликованный ) | 250,000 промилле (кролик, 30 мин)[3] | ||
| NIOSH (Пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 1 промилле ST 5 промилле[2] | ||
REL (Рекомендуемые) | Возможный профессиональный канцероген[2] | ||
IDLH (Непосредственная опасность) | 2000 промилле[2] | ||
| Родственные соединения | |||
| Изопрен Хлоропрен | |||
Родственные соединения | Бутан | ||
| Страница дополнительных данных | |||
| Показатель преломления (п), Диэлектрическая постоянная (εр), так далее. | |||
Термодинамический данные | Фазовое поведение твердое тело – жидкость – газ | ||
| УФ, ИК, ЯМР, РС | |||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
1,3-бутадиен (/ ˌBjuːtəˈdʌɪiːn /)[4] это органическое соединение по формуле (CH2= CH)2. Это бесцветный газ, который легко конденсируется в жидкость. Это важно в промышленном отношении как мономер в производстве синтетическая резина. Молекулу можно рассматривать как объединение двух виниловые группы. Это самый простой сопряженный диен.
Хотя бутадиен ломается быстро попадает в атмосферу, тем не менее, он обнаруживается в атмосферном воздухе в городских и пригородных районах из-за постоянного выброс из автомобили.[5]
Название бутадиен может также относиться к изомер, 1,2-бутадиен, который является накопленный диен со структурой H2С = С = СН-СН3. Этот аллен промышленного значения не имеет.
История
В 1863 г. французский химик Э. Кавенту выделил бутадиен из пиролиз из амиловый спирт.[6] Этот углеводород был идентифицирован как бутадиен в 1886 году, после Генри Эдвард Армстронг выделил его среди продуктов пиролиза нефти.[7] В 1910 году русский химик Сергей Лебедев полимеризовали бутадиен и получили материал с каучукообразными свойствами. Однако этот полимер оказался слишком мягким, чтобы заменить натуральный каучук во многих областях применения, особенно в автомобильных шинах.
Производство бутадиена зародилось в годы, предшествовавшие Второй мировой войне. Многие воюющие страны осознали, что в случае войны они могут быть отрезаны от каучуковых плантаций, контролируемых британская империя, и стремились уменьшить свою зависимость от натурального каучука.[8] В 1929 г. Эдуард Чункер и Уолтер Бок, работаю на IG Farben в Германии изготовлен сополимер стирол и бутадиен, который можно использовать в автомобильных шинах. Быстро последовало мировое производство, при этом бутадиен производился из зерновой спирт в Советском Союзе и США, а также из угля ацетилен в Германии.
Производство
Извлечение из C4 углеводороды
В Соединенных Штатах, Западной Европе и Японии бутадиен производится как побочный продукт паровой крекинг процесс, используемый для производства этилен и другие алкены. При смешивании с паром и кратковременном нагревании до очень высоких температур (часто выше 900 ° C) алифатические углеводороды отдают водород с образованием сложной смеси ненасыщенных углеводородов, включая бутадиен. Количество получаемого бутадиена зависит от углеводородов, используемых в качестве сырья. Световые источники, такие как этан, дайте в первую очередь этилен при крекинге, но более тяжелое сырье способствует образованию более тяжелых олефинов, бутадиена и ароматические углеводороды.
Бутадиен обычно изолирован от других четырехуглеродных углеводороды производится при паровом крекинге экстрактивной перегонкой с использованием полярный апротонный растворитель Такие как ацетонитрил, N-метил-2-пирролидон, фурфурол, или же диметилформамид, из которого затем удаляется дистилляция.[9]
От дегидрирования п-бутан
Бутадиен также может быть получен каталитическим дегидрирование нормального бутана (п-бутан). Первый такой послевоенный коммерческий завод, производящий 65 000 тонны бутадиена в год, начал работу в 1957 г. Хьюстон, Техас.[10] До этого, в 1940-х гг. Компания "Резиновый резерв", входящая в состав правительства США, построила несколько заводов в Боргер, Техас, Толедо, Огайо, и Эль-Сегундо, Калифорния производить синтетический каучук для военных нужд в рамках программы США по синтетическому каучуку.[11] Общая мощность составила 68 тыс. Тонн в год (килограмм метрических тонн в год).
Сегодня бутадиен из п-бутан коммерчески практикуется с использованием Процесс Houdry Catadiene, который был разработан во время Второй мировой войны. Это влечет за собой обработку бутана глинозем и хромия при высоких температурах.[12]
Из этанола
В других частях света, включая Южную Америку, Восточную Европу, Китай и Индию, бутадиен также производится из этиловый спирт. Несмотря на то, что он не может конкурировать с паровым крекингом для производства больших объемов бутадиена, более низкие капитальные затраты делают производство этанола жизнеспособным вариантом для предприятий меньшей мощности. Использовались два процесса.
В одноэтапном процессе, разработанном Сергей Лебедев этанол превращается в бутадиен, водород и воду при 400–450 ° C с помощью любого из множества катализаторов на основе оксидов металлов:[13]
Этот процесс был основой для Советский союз промышленности синтетического каучука во время и после Второй мировой войны, и он оставался в ограниченном использовании в России и других частях Восточной Европы до конца 1970-х годов. В то же время в Бразилии отказались от этого вида производства. По состоянию на 2017 год из этанола промышленным способом бутадиен не производился.
В другом, двухэтапном процессе, разработанном русским химиком-эмигрантом. Иван Остромисленский, этанол окисленный к ацетальдегид, который реагирует с дополнительным этанолом в течение тантал -пористый пористый кремнезем катализатор при 325–350 ° C с получением бутадиена:[13]
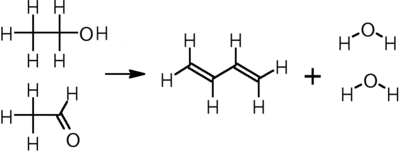 CH3CH2ОН + СН3CHO → CH2= СН-СН = СН2 + 2 часа2О
CH3CH2ОН + СН3CHO → CH2= СН-СН = СН2 + 2 часа2О
Этот процесс был одним из трех, используемых в Соединенных Штатах для производства «правительственного каучука» во время Второй мировой войны, хотя он менее экономичен, чем бутан или бутен для больших объемов. Тем не менее, три завода общей мощностью 200 тыс. Тонн в год.[когда определяется как? ] были построены в США (Институт, Западная Вирджиния, Луисвилл, Кентукки и Кобута, Пенсильвания ) с запуском, завершенным в 1943 году, завод в Луисвилле первоначально производил бутадиен из ацетилена, произведенного на ассоциированном заводе по производству карбида кальция. Этот процесс до сих пор используется в Китае и Индии.
Из бутенов
1,3-Бутадиен также может производиться каталитический дегидрирование нормального бутены. Этот метод также использовался Программа США по синтетическому каучуку (СССРП) во время Вторая Мировая Война. Этот процесс был намного более экономичным, чем спиртовой или н-бутановый путь, но конкурировал с авиационный бензин для доступных молекул бутена (бутенов было много благодаря каталитический крекинг ). СССРП построил несколько заводов в г. Батон-Руж и Лейк Чарльз, Луизиана; Хьюстон, Baytown, и Порт-Нечес, Техас; и Торранс, Калифорния.[11] Общий годовой объем производства составил 275 тыс. Тонн в год.
В 1960-х годах Хьюстон компания, известная как "Петро-Текс", запатентовала процесс производства бутадиена из нормального бутены окислительным дегидрирование с использованием фирменного катализатора. Неясно, применяется ли эта технология в коммерческих целях.[14]
После Второй мировой войны производство бутенов стало основным видом производства в СССР.
Для лабораторного использования
1,3-Бутадиен неудобен для лабораторного использования, потому что это газ. Лабораторные процедуры были оптимизированы для его получения из неосновных прекурсоров. Это может быть произведено ретро-Реакция Дильса-Альдера из циклогексен.[15] Сульфолен является удобным твердым источником 1,3-бутадиена для хранения в лаборатории. Он высвобождает диен и диоксид серы при нагревании.
Использует
Большинство бутадиена полимеризованный производить синтетический каучук. Полибутадиен сам по себе очень мягкий, почти жидкий материал, представляющий коммерческий интерес. В сополимеры приготовлено из бутадиена и стирол и / или акрилонитрил, Такие как акрилонитрилбутадиенстирол (АБС), нитрил-бутадиен (NBR) и стирол-бутадиен (SBR) жесткие и / или эластичные. SBR - это материал, наиболее часто используемый для производства автомобильных шин.[12]
Меньшие количества бутадиена используются для изготовления промежуточного нейлона, адипонитрил, добавлением молекулы цианистый водород к каждой из двойных связей в процессе, называемом гидроцианирование разработан DuPont. Другие синтетические каучуковые материалы, такие как хлоропрен, а растворитель сульфолан также производятся из бутадиена. Бутадиен используется в промышленном производстве 4-винилциклогексен через Дильс Альдер димеризация реакция.[16] Винилциклогексен - обычная примесь, обнаруживаемая в бутадиене при хранении из-за димеризации. Циклооктадиен и циклододекатриен производятся в реакциях димеризации и тримеризации, катализируемых никелем или титаном, соответственно. Бутадиен также полезен в синтезе циклоалканы и циклоалкены, поскольку он реагирует с двойными и тройными углерод-углеродными связями через Реакция Дильса-Альдера.
Строение, экстерьер и стабильность

Самый стабильный конформер 1,3-бутадиена является s-транс конформация, в которой молекула плоская, с двумя парами двойных связей, обращенными в противоположных направлениях. Эта конформация является наиболее стабильной, поскольку перекрытие орбиталей между двойными связями максимально, что обеспечивает максимальное сопряжение, а стерические эффекты минимальны. Условно с-транс конформация считается имеющей C2-C3 двугранный угол 180 °. Напротив, s-СНГ Конформация, в которой двугранный угол равен 0 °, с парой двойных связей, обращенных в одном направлении, примерно на 16,5 кДж / моль (3,9 ккал / моль) выше по энергии из-за стерических затруднений. Эта геометрия является локальным максимумом энергии, поэтому в отличие от с-транс геометрия, это не конформер. В бестактный геометрия, в которой двойные связи s-cis геометрия скручена, чтобы дать двугранный угол около 38 °, это второй конформер, который примерно на 12,0 кДж / моль (2,9 ккал / моль) выше по энергии, чем с-транс конформер. В целом, существует барьер в 24,8 кДж / моль (5,9 ккал / моль) для изомеризации между двумя конформерами.[17] Этот повышенный вращательный барьер и сильное общее предпочтение почти плоской геометрии свидетельствует о делокализованной π-системе и небольшой степени характера частичной двойной связи в одинарной связи C-C в соответствии с теорией резонанса.
Несмотря на высокую энергию s-cis Конформации 1,3-бутадиен должен принять эту конформацию (или очень похожую), прежде чем он сможет участвовать в качестве четырехэлектронного компонента в согласованных реакциях циклоприсоединения, таких как Реакция Дильса-Альдера.
Точно так же совместное экспериментальное и вычислительное исследование показало, что двойная связь s-транс-длина бутадиена составляет 133,8 мкм, а длина этилена - 133,0 мкм. Это было воспринято как свидетельство ослабления и удлинения π-связи в результате делокализации, как показано на резонансных структурах, показанных ниже.[18]
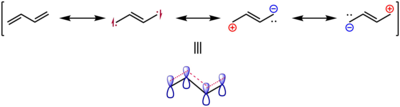
Качественная картина молекулярные орбитали 1,3-бутадиена легко получить, применяя теорию Хюккеля. (Статья о Теория Хюккеля дает вывод для бутадиеновых орбиталей.)
1,3-Бутадиен также термодинамически стабилизирован. В то время как монозамещенная двойная связь выделяет около 30,3 ккал / моль тепла при гидрировании, 1,3-бутадиен выделяет немного меньше (57,1 ккал / моль), чем удвоенная энергия (60,6 ккал / моль), ожидаемая для двух изолированных двойных связей. Это означает, что энергия стабилизации составляет 3,5 ккал / моль.[19] Аналогичным образом, гидрирование концевой двойной связи 1,4-пентадиена высвобождает 30,1 ккал / моль тепла, в то время как гидрирование концевой двойной связи сопряженного (E) -1,3-пентадиен выделяет только 26,5 ккал / моль, что подразумевает очень похожее значение энергии стабилизации в 3,6 ккал / моль.[20] Разницу в ~ 3,5 ккал / моль этих теплот гидрирования можно принять за резонансную энергию сопряженного диена.
Реакции
Промышленное использование иллюстрирует тенденцию бутадиена к полимеризации. Его подверженность реакциям 1,4-присоединения иллюстрируется гидроцианированием. Как и многие диены, он претерпевает катализируемые Pd реакции, протекающие через аллильные комплексы.[21] Это партнер в Реакции Дильса-Альдера, например с малеиновым ангидридом, чтобы дать тетрагидрофталевый ангидрид.[22]
Как и другие диены, бутадиен является лигандом для комплексов низковалентных металлов, например производные Fe (бутадиен) (CO)3 и Мо (бутадиен)3.

Здоровье и безопасность окружающей среды
Бутадиен обладает низкой острой токсичностью. LC50 составляет 12,5-11,5 об.% при вдыхании крысами и мышами.[12]
Длительное воздействие было связано с сердечно-сосудистыми заболеваниями, существует последовательная связь с лейкемией, а также значительная связь с другими видами рака.[24]
1,3-Бутадиен был отнесен к Группе 1 канцероген («канцерогенное для человека») МАИР,[25] и также был внесен в список канцерогенов Агентством по регистрации токсических веществ и Агентством по охране окружающей среды США.[26][27] Американская конференция государственных специалистов по промышленной гигиене (ACGIH) внесла это химическое вещество в список подозреваемых канцерогенов.[27] Совет по защите природных ресурсов (NRDC) перечисляет некоторые группы заболеваний, которые предположительно связаны с этим химическим веществом.[28] Некоторые исследователи пришли к выводу, что это самый мощный канцероген в сигаретный дым, вдвое мощнее, чем занявший второе место акрилонитрил[29]
1,3-Бутадиен также подозревается в человеческом тератоген.[30][31][32] Продолжительное и чрезмерное воздействие может повлиять на многие участки человеческого тела; кровь, мозг, глаза, сердце, почки, легкие, нос и горло - все они реагируют на присутствие избыточного 1,3-бутадиена.[33] Данные на животных показывают, что женщины имеют более высокую чувствительность к возможным канцерогенным эффектам бутадиена по сравнению с мужчинами при воздействии этого химического вещества. Это может быть связано с воздействием рецепторов эстрогена. Хотя эти данные показывают важные последствия для рисков воздействия бутадиена на человека, для окончательной оценки рисков необходимо больше данных. Также отсутствуют данные о воздействии бутадиена на репродуктивную функцию и развитие мышей, но исследования на животных показали, что вдыхание бутадиена во время беременности может увеличить количество врожденных дефектов, а у людей такие же гормональные системы, как и у животных.[34]
1,3-Бутадиен признан высокореактивным летучим органическим соединением (HRVOC) из-за его способности легко образовывать озон, и поэтому выбросы химического вещества строго регулируются TCEQ в части Хьюстон-Бразория-Галвестон Область недостижения озона.[1]
Смотрите также
Рекомендации
- ^ «Переднее дело». Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга). Кембридж: Королевское химическое общество. 2014. с. 374. Дои:10.1039 / 9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ а б c d е Карманный справочник NIOSH по химической опасности. "#0067". Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б «1,3-Бутадиен». Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ https://www.lexico.com/definition/butadiene
- ^ «1,3-Бутадиен». Агентство по охране окружающей среды США Агентство по охране окружающей среды США. Получено 2 сентября 2014.
- ^ Кавенту, Э. (1863). "Ueber eine mit dem zweifach-gebromten Brombutylen isomere Verbindung und über die bromhaltigen Derivate des Brombutylens". Юстус Либигс Аннален дер Хеми. 127: 93–97. Дои:10.1002 / jlac.18631270112.
- ^ Armstrong, H.E .; Миллер, А. К. (1886). «Разложение и генезис углеводородов при высоких температурах. I. Продукты производства газа из нефти». J. Chem. Soc. 49: 74–93. Дои:10.1039 / CT8864900074.
- ^ Простые вещи не спасут Землю, Дж. Роберт Хантер
- ^ Солнце, Г. Wristers, J.P. (1992). Бутадиен. В J.I. Крошвиц (ред.), Энциклопедия химической технологии, 4-е изд., т. 4. С. 663–690. Нью-Йорк: Джон Вили и сыновья.
- ^ Бейчок, М.Р. и Брак, В.Дж., «Первый послевоенный бутадиеновый завод», Нефтепереработчик, Июнь 1957 г.
- ^ а б Герберт, Вернон, «Синтетический каучук: проект, который должен был преуспеть», Greenwood Press, 1985, ISBN 0-313-24634-3
- ^ а б c Я. Груб, Э. Лёзер (2012). «Бутадиен». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a04_431.pub2.CS1 maint: использует параметр авторов (связь)
- ^ а б Киршенбаум, И. (1978). Бутадиен. В М. Грейсоне (ред.), Энциклопедия химической технологии, 3-е изд., т. 4. С. 313–337. Нью-Йорк: Джон Вили и сыновья.
- ^ «БУТАДИЕН ЧЕРЕЗ ОКСИДАТИВНОЕ ДЕГИДРОГЕНЕНИЕ». ResearchGate. Получено 1 июня 2019.
- ^ Э. Б. Хершберг, Джон Р. Рухофф (1937). «1,3-Бутадиен». Орг. Синтезатор. 17: 25. Дои:10.15227 / orgsyn.017.0025.CS1 maint: использует параметр авторов (связь)
- ^ 4-винилциклогексен (PDF). МАИР. ISBN 9789283212607. Получено 19 апреля 2009.
- ^ Феллер, Дэвид; Крейг, Норман К. (26 февраля 2009 г.). «Высокий уровень ab Initio энергии и структур для ротамеров 1,3-бутадиена». Журнал физической химии A. 113 (8): 1601–1607. Bibcode:2009JPCA..113.1601F. Дои:10.1021 / jp8095709. ISSN 1089-5639. PMID 19199679.
- ^ Craig, Norman C .; Гронер, Питер; Маккин, Дональд К. (1 июня 2006 г.). «Равновесные структуры для бутадиена и этилена: убедительные доказательства делокализации Π-электронов в бутадиене». Журнал физической химии A. 110 (23): 7461–7469. Bibcode:2006JPCA..110.7461C. Дои:10.1021 / jp060695b. ISSN 1089-5639. PMID 16759136.
- ^ К., Воллхардт, К. Питер (2007). Органическая химия: структура и функции. Schore, Neil Eric, 1948- (5-е изд.). Нью-Йорк: W.H. Фримен. ISBN 978-0716799498. OCLC 61448218.
- ^ 1937-, Кэри, Фрэнсис А. (2002). Органическая химия (5-е изд.). Лондон: Макгроу-Хилл. ISBN 978-0071151498. OCLC 49907089.CS1 maint: числовые имена: список авторов (связь)
- ^ Дж. Э. Нюстрём, Т. Рейн, Дж. Э. Бэквалл (1989). «1,4-Функционализация 1,3-диенов посредством катализируемого палладием хлорацетоксилирования и аллильного аминирования: 1-ацетокси-4-диэтиламино-2-бутен и 1-ацетокси-4-бензиламино-2-бутен». Орг. Синтезатор. 67: 105. Дои:10.15227 / orgsyn.067.0105.CS1 maint: использует параметр авторов (связь)
- ^ Артур Коуп, Эльберт С. Херрик (1950). «Цис-Δ4-тетрагидрофталевый ангидрид». Орг. Синтезатор. 50: 93. Дои:10.15227 / orgsyn.030.0093.CS1 maint: использует параметр авторов (связь)
- ^ Рейсс, Гвидо Дж. (2010). "Повторное определение (η4-s-цис-1,3-бутадиен) трикарбонилирон (0) ». Acta Crystallographica Раздел E. 66 (11): m1369. Дои:10.1107 / S1600536810039218. ЧВК 3009352. PMID 21588810.
- ^ «Лист НПИ». Архивировано из оригинал 22 декабря 2003 г.. Получено 10 января 2006.
- ^ Гроссе, Янн; Баан, Роберт; Straif, Курт; Секретан, Беатрис; Эль-Гиссасси, Фатиха; Бувар, Вероник; Альтиери, Андреа; Коглиано, Винсент (2008). «Канцерогенность 1,3-бутадиена, этиленоксида, винилхлорида, винилфторида и винилбромида». Ланцет онкологии. 8 (8): 679–680. Дои:10.1016 / S1470-2045 (07) 70235-8. ISSN 1470-2045. PMID 17726789.
- ^ «ATSDR - Токсичные вещества - 1,3-Бутадиен».
- ^ а б Влияние на здоровье https://www.osha.gov/SLTC/butadiene/index.html
- ^ «Группы заболеваний подчеркивают необходимость защиты людей от токсичных химических веществ».
- ^ Фаулз, Дж; Дайбинг, Э (4 сентября 2003 г.). «Применение принципов оценки токсикологического риска к химическим составляющим сигаретного дыма». Институт экологических наук и исследований. 12 (4): 424–430. Дои:10.1136 / tc.12.4.424. ЧВК 1747794. PMID 14660781. Получено 12 октября 2014.
- ^ Ландриган, П.Дж. (1990). «Критическая оценка эпидемиологических исследований канцерогенности 1,3-бутадиена для человека». Перспективы гигиены окружающей среды. 86: 143–147. Дои:10.1289 / ehp.9086143. ЧВК 1567758. PMID 2205484.
- ^ «1,3-Бутадиен КАС № 106-99-0» (PDF). Отчет о канцерогенных веществах (11-е изд.). Архивировано из оригинал (PDF) 8 мая 2009 г.
- ^ Мелник, Рональд Л .; Кон, Майкл С. (1995). «Механистические данные показывают, что 1,3-бутадиен является канцерогеном для человека». Канцерогенез. 16 (2): 157–63. Дои:10.1093 / carcin / 16.2.157. PMID 7859343.
- ^ «Архивная копия». Архивировано из оригинал 3 февраля 2011 г.. Получено 20 августа 2010.CS1 maint: заархивированная копия как заголовок (связь)
- ^ Веб-сайт EPA
внешняя ссылка
- 1,3-бутадиен - Агентство регистрации токсичных веществ и заболеваний
- 1,3-бутадиен - CDC - Карманный справочник NIOSH по химической опасности
- Национальный кадастр загрязнителей - 1,3-бутадиен