Нуклеофил - Википедия - Nucleophile
А нуклеофил это химические вещества который жертвует электронная пара сформировать химическая связь по отношению к реакция. Все молекулы или же ионы со свободной парой электронов или хотя бы одним пи бонд могут действовать как нуклеофилы. Поскольку нуклеофилы отдают электроны, они по определению Базы Льюиса. Нуклеофильный описывает сродство нуклеофила к положительно заряженным атомным ядрам. Нуклеофильность, иногда называемый нуклеофильная сила, относится к нуклеофильному характеру вещества и часто используется для сравнения сродства атомов. Нейтральные нуклеофильные реакции с такими растворителями, как спирты и вода названа сольволиз. Нуклеофилы могут принимать участие в нуклеофильное замещение, в результате чего нуклеофил притягивается к полному или частичному положительному заряду.
История
Условия нуклеофил и электрофил были представлены Кристофер Келк Ингольд в 1933 г.,[1] замена терминов анионоид и катионоид предложенный ранее А. Дж. Лэпворт в 1925 г.[2]
Слово нуклеофил происходит от ядро и греческое слово φιλος, философ ради любви.
Характеристики
В общем, в группе по периодической таблице, чем более основной ион (чем выше pKа конъюгированной кислоты), тем более реакционноспособен он как нуклеофил. В ряду нуклеофилов с одним и тем же атакующим элементом (например, кислородом) порядок нуклеофильности будет соответствовать основности. Сера в целом является лучшим нуклеофилом, чем кислород.
Нуклеофильность
Было разработано множество схем, пытающихся количественно оценить относительную нуклеофильную силу. Следующее эмпирический данные были получены путем измерения скорость реакции для многих реакций с участием многих нуклеофилов и электрофилов. Нуклеофилы, демонстрирующие так называемые альфа-эффект обычно не используются в этом виде лечения.
Уравнение Суэйна – Скотта
Первая такая попытка обнаружена в уравнении Суэйна – Скотта[3][4] выведено в 1953 г .:
Этот отношения свободной энергии связывает псевдопервый порядок константа скорости реакции (в воде при 25 ° C), kреакции, нормированной на скорость реакции, k0стандартной реакции с водой в качестве нуклеофила до нуклеофильной константы п для данного нуклеофила и константы субстрата s которая зависит от чувствительности субстрата к нуклеофильной атаке (определяется как 1 для бромистый метил ).
Эта обработка приводит к следующим значениям для типичных нуклеофильных анионов: ацетат 2.7, хлористый 3.0, азид 4.0, гидроксид 4.2, анилин 4.5, йодид 5.0 и тиосульфат 6.4. Типичные постоянные подложки 0,66 для этилтозилат, 0.77 для β-пропиолактон, 1.00 для 2,3-эпоксипропанол, 0.87 для бензилхлорид и 1,43 для бензоилхлорид.
Уравнение предсказывает, что в нуклеофильное смещение на бензилхлорид, то азид анион реагирует в 3000 раз быстрее, чем вода.
Уравнение Ричи
Уравнение Ричи, полученное в 1972 году, представляет собой еще одно соотношение свободной энергии:[5][6][7]
куда N+ - параметр, зависящий от нуклеофилов и k0 то константа скорости реакции для воды. В этом уравнении параметр, зависящий от подложки, например s в уравнении Суэйна – Скотта отсутствует. Уравнение гласит, что два нуклеофила реагируют с одинаковой относительной реакционной способностью независимо от природы электрофила, что нарушает принцип реактивность – селективность. По этой причине это уравнение также называют постоянная избирательность отношения.
В исходной публикации данные были получены реакциями выбранных нуклеофилов с выбранными электрофильными карбокатионы Такие как тропилий или же диазоний катионы:
или (не отображается) ионы на основе малахитовый зеленый. С тех пор было описано много других типов реакций.
Типичный Ричи N+ значения (в метанол ) составляют: 0,5 для метанол, 5.9 для цианид анион, 7,5 для метоксид анион, 8,5 для азид анион и 10,7 для тиофенол анион. Значения относительной реакционной способности катионов составляют -0,4 для катиона малахитового зеленого, +2,6 для катиона. катион бензолдиазония, и +4,5 для катион тропилия.
Уравнение Майра – Патца
В уравнении Майра – Патца (1994):[8]
В второго порядка константа скорости реакции k при 20 ° C для реакции зависит от параметра нуклеофильности N, параметр электрофильности E, и параметр наклона, зависящий от нуклеофилов s. Постоянная s определяется как 1 с 2-метил-1-пентен как нуклеофил.
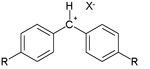
Многие из констант были получены в результате реакции так называемых ионов бензгидрилия как электрофилы:[9]
и разнообразный набор π-нуклеофилов:
 .
.
Типичные значения E составляют +6,2 для R = хлор, +5,90 для R = водород, 0 для R = метокси и −7,02 для R = диметиламин.
Типичные значения N с s в скобках составляют -4,47 (1,32) для электрофильное ароматическое замещение к толуол (1), −0,41 (1,12) для электрофильная добавка до 1-фенил-2-пропена (2) и 0,96 (1) для добавления к 2-метил-1-пентену (3), -0,13 (1,21) для реакции с трифенилаллилсиланом (4), 3,61 (1,11) для реакции с 2-метилфуран (5), +7,48 (0,89) для реакции с изобутенилтрибутилстаннаном (6) и +13,36 (0,81) для реакции с енамин 7.[10]
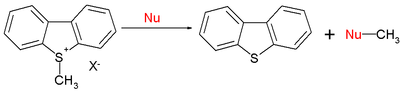
В круг органических реакций также входят: SN2 реакции:[11]
При E = −9,15 для S-метилдибензотиофения ион, типичные значения нуклеофилов N (s) составляют 15,63 (0,64) для пиперидин, 10,49 (0,68) для метоксид, а для воды - 5,20 (0,89). Короче говоря, нуклеофильность по отношению к sp2 или sp3 центры следуют той же схеме.
Единое уравнение
Чтобы объединить описанные выше уравнения, уравнение Майра переписывается как:[11]
с sE параметр наклона, зависящий от электрофилов, и sN параметр наклона, зависящий от нуклеофилов. Это уравнение можно переписать несколькими способами:
- с sE = 1 для карбокатионов это уравнение равно исходному уравнению Майра – Патца 1994 г.,
- с sN = 0,6 для большинства n нуклеофилов уравнение принимает вид
- или исходное уравнение Скотта – Свейна, записанное как:
- с sE = 1 для карбокатионов и sN = 0,6 уравнение принимает следующий вид:
- или исходное уравнение Ричи, записанное как:
Типы
Примерами нуклеофилов являются анионы, такие как Cl−, или соединение с одинокая пара электронов, таких как NH3 (аммиак), PR3.
В приведенном ниже примере кислород гидроксид-иона отдает электронную пару для образования новой химической связи с углерод в конце бромпропан молекула. Связь между углеродом и бром затем проходит гетеролитическое деление, причем атом брома забирает подаренный электрон и становится бромид ион (Br−), так как SN2 реакция происходит атакой сзади. Это означает, что ион гидроксида атакует атом углерода с другой стороны, как раз напротив иона брома. Из-за этой атаки сзади SN2 реакции приводят к инверсии конфигурация электрофила. Если электрофил хиральный, он обычно сохраняет свою хиральность, хотя SN2 продукта абсолютная конфигурация перевернут по сравнению с исходным электрофилом.
An амбидентный нуклеофил это тот, который может атаковать из двух или более мест, в результате чего получается два или более продукта. Например, тиоцианат ион (SCN−) может атаковать либо из S или N. По этой причине SN2 реакция алкилгалогенида с SCN− часто приводит к смеси алкилтиоцианата (R-SCN) и алкила изотиоцианат (R-NCS). Аналогичные соображения применяются в Синтез нитрила Кольбе.
Галогены
В то время как галогены не являются нуклеофильными в их двухатомной форме (например, I2 не является нуклеофилом), их анионы являются хорошими нуклеофилами. В полярных протонных растворителях F− самый слабый нуклеофил, а I− сильнейший; этот порядок обратный в полярных апротонных растворителях.[12]
Углерод
Нуклеофилы углерода часто металлоорганические реагенты такие как найденные в Реакция Гриньяра, Блэз реакция, Реформатская реакция, и Реакция Барбье или реакции с участием литийорганические реагенты и ацетилиды. Эти реагенты часто используются для выполнения нуклеофильные добавки.
Enols также являются углеродными нуклеофилами. Образование енола катализируется кислота или же основание. Энолы амбидент нуклеофилы, но, как правило, нуклеофильные на альфа-углерод атом. Энолы обычно используются в реакции конденсации, в том числе Клейзеновская конденсация и альдольная конденсация реакции.
Кислород
Примеры кислородных нуклеофилов: воды (ЧАС2O), гидроксид анион, спирты, алкоксид анионы, пероксид водорода, и карбоксилат-анионы.Нуклеофильная атака не происходит во время межмолекулярной водородной связи.
Сера
Нуклеофилов серы, сероводород и его соли, тиолы (RSH), тиолат-анионы (RS−), анионы тиолкарбоновых кислот (RC (O) -S−), и анионы дитиокарбонатов (RO-C (S) -S−) и дитиокарбаматы (R2N-C (S) -S−) используются чаще всего.
В целом, сера очень нуклеофильна из-за своего большого размера, что делает его легко поляризуемым, а его неподеленные пары электронов легко доступны.
Азот
Нуклеофилы азота включают: аммиак, азид, амины, нитриты, гидроксиламин, гидразин, карбазид, фенилгидразин, семикарбазид, и амид.
Металлические центры
Хотя металлические центры (например, Li+, Zn2+, Sc3+и т. д.) чаще всего являются катионными и электрофильными (кислота Льюиса) по природе, определенные металлические центры (особенно те, которые находятся в низкой степени окисления и / или несут отрицательный заряд) являются одними из самых сильных зарегистрированных нуклеофилов и иногда называются «сверхнуклеофилами». . " Например, при использовании метилиодида в качестве электрофила сравнения Ph3Sn– примерно на 10000 нуклеофильнее, чем я–, а форма Co (I) витамин B12 (витамин B12 с) составляет около 107 в разы более нуклеофильны.[13] Другие супернуклеофильные центры металлов включают анионы карбонилметалата с низкой степенью окисления (например, CpFe (CO)2–).[14]
Смотрите также
Рекомендации
- ^ Ингольд, К. К. (1933). «266. Значение таутомерии и реакций ароматических соединений в электронной теории органических реакций». Журнал химического общества (возобновлено): 1120. Дои:10.1039 / младший9330001120.
- ^ Лэпворт, А. (1925). «Заменяемость атомов галогена атомами водорода». Природа. 115: 625.
- ^ Количественная корреляция относительных ставок. Сравнение гидроксид-иона с другими нуклеофильными реагентами в отношении алкилгалогенидов, сложных эфиров, эпоксидов и ацилгалогенидов К. Гарднер Суэйн, Карлтон Б. Скотт Варенье. Chem. Soc.; 1953; 75(1); 141-147. Абстрактный
- ^ «Уравнение Суэйна – Скотта». Золотая книга. ИЮПАК. 24 февраля 2014 г.
- ^ Золотая книга определение (Ричи) Связь[постоянная мертвая ссылка ]
- ^ Нуклеофильная реакционная способность по отношению к катионам Calvin D. Ritchie Acc. Chem. Res .; 1972; 5(10); 348-354. Абстрактный
- ^ Катионно-анионные комбинации. XIII. Корреляция реакций нуклеофилов со сложными эфирами Кэлвин Д. Ричи Варенье. Chem. Soc.; 1975; 97(5); 1170–1179.Абстрактный
- ^ Майр, Герберт; Патц, Матиас (1994). «Шкалы нуклеофильности и электрофильности: система для упорядочивания полярных органических и металлоорганических реакций». Angewandte Chemie International Edition на английском языке. 33 (9): 938. Дои:10.1002 / anie.199409381.
- ^ Майр, Герберт; Баг, Торстен; Надо, Маттиас Ф; Геринг, Николь; Иррганг, Бернхард; Янкер, Бриджит; Кемпф, Бернхард; Лоос, Роберт; Офиал, Армин Р; Ременников, Григорий; Шиммель, Хольгер (2001). «Эталонные шкалы для характеристики катионных электрофилов и нейтральных нуклеофилов». Журнал Американского химического общества. 123 (39): 9500–12. Дои:10.1021 / ja010890y. PMID 11572670. S2CID 8392147.
- ^ Интернет-база данных параметров реактивности, поддерживаемая группой Майра, доступна по адресу http://www.cup.uni-muenchen.de/oc/mayr/
- ^ а б Фан, Тхань Бинь; Брейгст, Мартин; Майр, Герберт (2006). «К общей шкале нуклеофильности?». Angewandte Chemie International Edition. 45 (23): 3869–74. CiteSeerX 10.1.1.617.3287. Дои:10.1002 / anie.200600542. PMID 16646102.
- ^ Chem 2401 Дополнительные примечания. Томпсон, Элисон и Пинкок, Джеймс, факультет химии Университета Далхаузи
- ^ Schrauzer, G.N .; Deutsch, E .; Виндгассен, Р. Дж. (Апрель 1968 г.). «Нуклеофильность витамина B (менее 12 с)». Журнал Американского химического общества. 90 (9): 2441–2442. Дои:10.1021 / ja01011a054. ISSN 0002-7863.
- ^ Десси, Раймонд Э .; Pohl, Rudolph L .; Кинг, Р. Брюс (ноябрь 1966 г.). "Металлоорганическая электрохимия. VII. 1 Нуклеофильность металлических и металлоидных анионов, полученных из металлов групп IV, V, VI, VII и VIII". Журнал Американского химического общества. 88 (22): 5121–5124. Дои:10.1021 / ja00974a015. ISSN 0002-7863.





 .
.