Аллиловый спирт - Allyl alcohol
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC Проп-2-ен-1-ол | |
| Другие имена | |
| Идентификаторы | |
3D модель (JSmol ) | |
| 3DMet | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.003.156 |
| Номер ЕС |
|
| КЕГГ | |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1098 |
| |
| |
| Характеристики | |
| C3ЧАС6О | |
| Молярная масса | 58.080 г · моль−1 |
| Внешность | бесцветная жидкость[1] |
| Запах | горчичный[1] |
| Плотность | 0,854 г / мл |
| Температура плавления | −129 ° С |
| Точка кипения | 97 ° С (207 ° F, 370 К) |
| Смешиваемый | |
| Давление газа | 17 мм рт. Ст.[1] |
| Кислотность (пKа) | 15,5 (В2O)[2] |
| -36.70·10−6 см3/ моль | |
| Опасности | |
| Паспорт безопасности | Внешний паспорт безопасности материала |
| Пиктограммы GHS |     |
| Сигнальное слово GHS | Опасность |
| H225, H301, H311, H315, H319, H331, H335, H400 | |
| P210, P233, P240, P241, P242, P243, P261, P264, P270, P271, P273, P280, P301 + 310, P302 + 352, P303 + 361 + 353, P304 + 340, P305 + 351 + 338, P311, P312, P321, P322, P330, P332 + 313, P337 + 313, P361 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | 21 ° С (70 ° F, 294 К) |
| 378 ° С (712 ° F, 651 К) | |
| Пределы взрываемости | 2.5–18.0% |
| Смертельная доза или концентрация (LD, LC): | |
LC50 (средняя концентрация ) | 1000 частей на миллион (млекопитающее, 1 час) 76 частей на миллион (крыса, 8 часов) 207 частей на миллион (мышь, 2 часа) 1000 частей на миллион (кролик, 3,5 часа) 1000 частей на миллион (обезьяна, 4 часа) 1060 частей на миллион (крыса, 1 час) 165 частей на миллион (крыса, 4 часа) 76 частей на миллион (крыса, 8 часов)[3] |
| NIOSH (Пределы воздействия на здоровье в США): | |
PEL (Допустимо) | 2 частей на миллион[1] |
REL (Рекомендуемые) | TWA 2 частей на миллион (5 мг / м3) ST 4 частей на миллион (10 мг / м3) [кожа] [1] |
IDLH (Непосредственная опасность) | 20 частей на миллион[1] |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
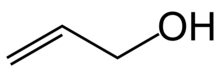
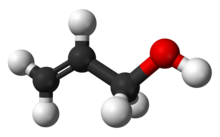
Аллиловый спирт (ИЮПАК имя: проп-2-ен-1-ол) является органическое соединение с структурная формула CH2= CHCH2ОЙ. Как и многие спирты, это водорастворимая бесцветная жидкость. Он более токсичен, чем обычные небольшие спирты. Аллиловый спирт используется в качестве сырья для производства глицерина, но также используется в качестве предшественника многих специализированных соединений, таких как огнестойкие материалы, олифы, и пластификаторы.[4] Аллиловый спирт - самый мелкий представитель аллильный спирты.
Производство
Аллиловый спирт можно получить многими способами. Впервые он был подготовлен в 1856 г. Огюст Кахур и Август Хофманн к гидролиз из аллил йодид.[4] Сегодня аллиловый спирт коммерчески производится Олин и Ракушка корпорации через гидролиз аллилхлорид:
- CH2= CHCH2Cl + NaOH → CH2= CHCH2ОН + NaCl
Аллиловый спирт также можно получить перегруппировкой оксид пропилена, реакция, катализируемая квасцы калия при высокой температуре. Преимущество этого метода по сравнению с аллилхлоридным путем заключается в том, что он не генерирует соли. Также избеганием хлоридсодержащих промежуточных продуктов является «ацетоксилирование» пропилен к аллилацетат:
- CH2= CHCH3 + 1/2 O2 + CH3COOH → CH2= CHCH2OCOCH3 + H2О
Гидролиз этого ацетата дает аллиловый спирт. Альтернативным способом пропилен может быть окислен до акролеин, который на гидрирование дает спирт.
Другие методы
В принципе, аллиловый спирт можно получить дегидрирование из пропанол. В лаборатории он был приготовлен по реакции глицерин с щавелевая или же муравьиная кислота.[5][6] Аллиловые спирты обычно можно получить аллильное окисление из аллил соединения диоксид селена.
Приложения
Аллиловый спирт превращается в основном в глицидол, который является химическим промежуточным продуктом в синтезе глицерин, глицидиловые эфиры, сложные эфиры и амины. Кроме того, из аллилового спирта получают различные полимеризуемые сложные эфиры, например диаллил фталат.[4]
Безопасность
Аллиловый спирт более токсичен, чем родственные спирты. Его пороговое значение (ПДК) составляет 2 ppm. Это слезоточивый.[4]
Классифицируется как чрезвычайно опасное вещество в Соединенных Штатах, как определено в Разделе 302 США Закон о чрезвычайном планировании и праве общества на информацию (42 U.S.C. 11002), и к ним предъявляются строгие требования к отчетности со стороны предприятий, которые производят, хранят или используют его в значительных количествах.[7]
Смотрите также
Рекомендации
- ^ а б c d е ж грамм час Карманный справочник NIOSH по химической опасности. "#0017". Национальный институт охраны труда и здоровья (NIOSH).
- ^ Хейнс, Уильям М., изд. (2016). CRC Справочник по химии и физике (97-е изд.). CRC Press. п. 5–88. ISBN 978-1498754286.
- ^ «Аллиловый спирт». Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б c d Людгер Крэлинг; Юрген Крей; Джеральд Якобсон; Иоганн Гролиг; Леопольд Микше (2002). «Аллильные соединения». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a01_425.
- ^ Оливер Камм; К. С. Марвел (1941). «Аллиловый спирт». Органический синтез.; Коллективный объем, 1, п. 42
- ^ Коэн, Юлий (1900). Практическая органическая химия (2-е изд.). Лондон: Macmillan and Co., Limited. п.96.
Практическая органическая химия Коэн Юлиус.
- ^ «40 C.F.R .: Приложение A к Части 355 - Список особо опасных веществ и их планируемые пороговые количества» (PDF) (1 июля 2008 г. ред.). Государственная типография. Архивировано из оригинал (PDF) 25 февраля 2012 г.. Получено 29 октября, 2011. Цитировать журнал требует
| журнал =(помощь)
внешняя ссылка
- Международная карта химической безопасности 0095
- Карманный справочник NIOSH по химической опасности. "#0017". Национальный институт охраны труда и здоровья (NIOSH).
- Institut national de recherche et de sécurité (2004). "Аллилитный спирт. " Токсикологический журнал № 156. Париж: INRS. (На французском)
- Общественная информация штата Мичиган об аллиловом спирте
- Рекомендации по профессиональному облучению

