Диоксид селена - Selenium dioxide
 | |
 | |
 | |
| Имена | |
|---|---|
| Другие имена Оксид селена (IV) Селеновый ангидрид | |
| Идентификаторы | |
3D модель (JSmol ) |
|
| ChemSpider | |
| ECHA InfoCard | 100.028.358 |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 3283 |
| |
| |
| Свойства | |
| SeO2 | |
| Молярная масса | 110,96 г / моль |
| Внешность | Белые кристаллы, слегка розовеют со следами разложения[1] |
| Запах | гнилой редис |
| Плотность | 3,954 г / см3, твердый |
| Температура плавления | 340 ° C (644 ° F, 613 K) (герметичная трубка) |
| Точка кипения | 350 ° C (662 ° F, 623 K) субл. |
| 38,4 г / 100 мл (20 ° С) 39,5 г / 100 мл (25 ° C) 82,5 г / 100 мл (65 ° С) | |
| Растворимость | растворим в бензол |
| Растворимость в этиловый спирт | 6,7 г / 100 мл (15 ° С) |
| Растворимость в ацетон | 4,4 г / 100 мл (15 ° С) |
| Растворимость в уксусная кислота | 1,11 г / 100 мл (14 ° С) |
| Растворимость в метанол | 10,16 г / 100 мл (12 ° С) |
| Давление газа | 1,65 кПа (70 ° C) |
| Кислотность (пKа) | 2.62; 8.32 |
| −27.2·10−6 см3/ моль | |
| > 1.76 | |
| Структура | |
| см текст | |
| тригональный (Se) | |
| Опасности | |
| Паспорт безопасности | ICSC 0946 |
Классификация ЕС (DSD) (устарело) | Токсичный (Т) Опасно для окружающей среды (N) |
| R-фразы (устарело) | R23 / 25, R33, R50 / 53 |
| S-фразы (устарело) | (S1 / 2), S20 / 21, S28, S45, S60, S61 |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Не воспламеняется |
| Смертельная доза или концентрация (LD, LC): | |
LCLo (самый низкий опубликованный ) | 5890 мг / м3 (кролик, 20 мин) 6590 мг / м3 (коза, 10 мин) 6590 мг / м3 (овца, 10 мин)[2] |
| Родственные соединения | |
Другой анионы | Дисульфид селена |
Другой катионы | Диоксид серы Диоксид теллура |
| Триоксид селена | |
Родственные соединения | Селеновая кислота |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Диоксид селена это химическое соединение с формула SeO2. Это бесцветное твердое вещество - одно из наиболее часто встречающихся соединений селен.
Свойства
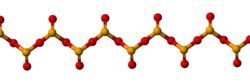
Твердый SeO2 является одномерным полимер, цепочка, состоящая из чередующихся селена и кислород атомы. Каждый атом Se имеет пирамидальную форму и несет концевую оксидную группу. Длина мостиковой связи Se-O составляет 179 пм, а конечное расстояние Se-O составляет 162 пм.[3] Относительная стереохимия при Se чередуется вдоль полимерной цепи (синдиотактический ). В газовой фазе диоксид селена присутствует в виде димеров и других олигомерных частиц, при более высоких температурах он является мономерным.[4] Мономерная форма имеет изогнутую структуру, очень похожую на структуру диоксид серы с длиной облигации 161 пм.[4] Димерная форма была выделена в низкотемпературной матрице аргона, и колебательные спектры показывают, что она имеет форму центросимметричного кресла.[3] Роспуск SeO2 в оксидихлорид селена дать тример [Se (O) O]3.[4] Мономерный SeO2 - полярная молекула с дипольным моментом 2,62 D [5] направлен от середины двух атомов кислорода к атому селена.
Твердое вещество легко возгоняется. При очень низких концентрациях пар имеет отвратительный запах, напоминающий разложившийся хрен. При более высоких концентрациях пар имеет запах, напоминающий соус хрена, и может обжечь нос и горло при вдыхании. В то время как SO2 имеет тенденцию быть молекулярным и SeO2 - одномерная цепь, TeO2 представляет собой сшитый полимер.[3]
SeO2 считается кислотный оксид: растворяется в воде с образованием селеновая кислота.[4] Часто условия селеновая кислота и диоксид селена используются взаимозаменяемо. Он реагирует с основанием с образованием селенит соли содержащий SeO2−
3 анион. Например, реакция с едкий натр производит селенит натрия:
- SeO2 + 2 NaOH → Na2SeO3 + H2О
Подготовка
Диоксид селена получают окислением селен сжиганием на воздухе или реакцией с азотной кислотой или пероксид водорода, но, пожалуй, самый удобный способ приготовления - обезвоживание селеновая кислота.
- 3 Se + 4 HNO3 + H2O → 3 H2SeO3 + 4 НЕТ
- 2 ч2О2 + Se → SeO2 + 2 часа2О
- ЧАС2SeO3 ⇌ SeO2 + H2О
Вхождение
Естественная форма диоксида селена, даунейит, является очень редким минералом. Он встречается только на очень немногих горящих отвалах угля.[6]
Использует
Органический синтез
SeO2 является важным реагентом в органический синтез. Окисление паральдегид (тример ацетальдегида) с SeO2 дает глиоксаль[7] и окисление циклогексанон дает циклогексан-1,2-дион.[8] Исходным материалом селена является уменьшенный к селену и осаждается в виде красного аморфное твердое тело которые можно легко отфильтровать.[8] Такой тип реакции называется Окисление Райли. Он также известен как реагент для «аллильного» окисления,[9] реакция, которая влечет за собой следующее преобразование

В более общем смысле это можно описать как;
- р2C = CR'-CHR "2 + [O] → R2C = CR'-C (OH) R "2
где R, R ', R "могут быть алкил или арил заместители.
Как краситель
Диоксид селена придает красную окраску стекло. Он используется в небольших количествах, чтобы нейтрализовать цвет из-за утюг примесей и так для создания (по-видимому) бесцветного стекла. В больших количествах дает темно-рубиново-красный цвет.
Диоксид селена является активным ингредиентом некоторых воронение решения.
Он также использовался в качестве тонера в фотографическое проявление.
Безопасность
Селен - это существенный элемент, но прием более 5 мг / день приводит к неспецифические симптомы.[10]
использованная литература
- ^ http://www.integrachem.com/msds/S138_26294_101.pdf
- ^ «Соединения селена (как Se)». Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б c Справочник по химии халькогенов: новые перспективы в области серы, селена и теллура, Франческо А. Девилланова, Королевское химическое общество, 2007 г., ISBN 9780854043668
- ^ а б c d Холлеман, Арнольд Фредерик; Виберг, Эгон (2001), Виберг, Нильс (ред.), Неорганическая химия, переведенный Иглсоном, Мэри; Брюэр, Уильям, Сан-Диего / Берлин: Academic Press / De Gruyter, ISBN 0-12-352651-5
- ^ Такео, Харутоши; Хирота, Эйзи; Морино, Йонезо (1972). «Константы потенциала третьего порядка и дипольный момент SeO2 методом микроволновой спектроскопии». Журнал молекулярной спектроскопии. 41 (2): 420–422. Дои:10.1016/0022-2852(72)90216-0. ISSN 0022-2852.
- ^ Финкельман, Роберт Б .; Мроуз, Мэри Э. (1977). "Дауниит, первое подтвержденное природное присутствие SeO2" (PDF). Американский минералог. 62: 316–320.
- ^ Ronzio, A.R .; Во, Т. Д. (1955). «Глиоксаль бисульфит». Органический синтез.CS1 maint: несколько имен: список авторов (ссылка на сайт); Коллективный объем, 3, п. 438
- ^ а б Hach, C. C. Banks, C. V .; Диль, Х. (1963). «1,2-Циклогександион Диоксим». Органический синтез.CS1 maint: несколько имен: список авторов (ссылка на сайт); Коллективный объем, 4, п. 229
- ^ Coxon, J.M .; Dansted, E .; Хартсхорн, М. П. (1988). «Окисление аллила пероксидом водорода – диоксидом селена: транс-пинокарвеол». Органический синтез.CS1 maint: несколько имен: список авторов (ссылка на сайт); Коллективный объем, 6, п. 946
- ^ Бернд Э. Лангнер «Селен и соединения селена» в Энциклопедии промышленной химии Ульмана, 2005, Wiley-VCH, Weinheim. Дои:10.1002 / 14356007.a23_525

