Триоксид хрома - Википедия - Chromium trioxide
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Хром триоксид | |
| Другие имена Хромовый ангидрид, оксид хрома (VI), хромовая кислота (неправильное название) | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.014.189 |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1463 |
| |
| |
| Характеристики | |
| CrО3 | |
| Молярная масса | 99.993 г · моль−1 |
| Внешность | Темно-красное зернистое твердое вещество, расплывающийся |
| Запах | Без запаха |
| Плотность | 2,7 г / см3 (20 ° С)[1] |
| Температура плавления | 197 ° С (387 ° F, 470 К) [1] |
| Точка кипения | 250 ° С (482 ° F, 523 К) разлагается[1] |
| 164,8 г /100 мл (0 ° С) 169 г / 100 мл (25 ° С)[1] 172,6 г / 100 мл (40 ° С) 198,1 г / 100 мл (100 ° С)[2] | |
| Растворимость | Растворим в ЧАС2ТАК4, HNO3, (C2ЧАС5)2О, CH3COOH, ацетон |
| +40·10−6 см3/ моль[1] | |
| Термохимия | |
Стандартный моляр энтропия (S | 73,2 Дж / моль · К[3] |
Станд. Энтальпия формирование (ΔжЧАС⦵298) | -589,3 кДж / моль[4] |
| Опасности | |
| Паспорт безопасности | ICSC 1194 |
| Пиктограммы GHS |      [5] [5] |
| Сигнальное слово GHS | Опасность |
| H271, H300, H301, H302, H303, H304, H305, H310, H311, H312, H313, H314, H315, H316[5] | |
| P201, P220, P260, P273, P280, P284[5] | |
| NFPA 704 (огненный алмаз) | |
| Смертельная доза или концентрация (LD, LC): | |
LD50 (средняя доза ) | 80 мг / кг (крысы, перорально)[6] |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Триоксид хрома (также известен как оксид хрома (VI) или же хромовый ангидрид) является неорганическое соединение с формула CrO3. Это кислый ангидрид из хромовая кислота, и иногда продается под тем же именем.[6]Это соединение темно-фиолетового цвета. твердый в безводных условиях - ярко-оранжевый во влажном состоянии, растворяется в воде при гидролизе. Ежегодно производятся миллионы килограммов, в основном для гальваника.[7] Триоксид хрома - мощный окислитель и канцероген.
Производство, структура и основные реакции
Триоксид хрома образуется при обработке хромат натрия или соответствующий дихромат натрия с серная кислота:[6]
- ЧАС2ТАК4 + Na2Cr2О7 → 2 CrO3 + Na2ТАК4 + H2О
По этому или подобным маршрутам ежегодно производится около 100 000 тонн.[7]
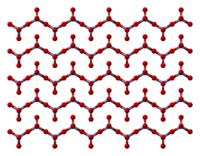
Твердое тело состоит из цепочек тетраэдрически координированных атомов хрома, имеющих общие вершины. Каждый хром Таким образом, центр имеет два общих кислородных центра с соседями. Два атома кислорода не являются общими, что дает общую стехиометрию 1: 3.[8][9]
Структура мономерного CrO3 был рассчитан с использованием теория функционала плотности, и прогнозируется пирамидальный (точечная группа C3в) скорее, чем планарный (точечная группа D3ч).[10]
Триоксид хрома разлагается при температуре выше 197 ° C, выделяя кислород и в конечном итоге давая Cr2О3:
- 4 CrO3 → 2 кр2О3 + 3 O2
Он используется в органический синтез в качестве окислителя, часто в виде раствора в уксусная кислота,[8] или же ацетон в случае Окисление Джонса. В этих окислениях Cr (VI) превращает первичные спирты к соответствующему карбоновые кислоты и вторичные спирты к кетоны. Реакции показаны ниже:
- Первичные спирты в карбоновые кислоты
- 4 CrO3 + 3 РЧ2ОН + 12 Н+ → 3 RCOOH + 4 Cr3+ + 9 часов2О
- Вторичные спирты к кетонам
- 2 CrO3 + 3 р2CHOH + 6 H+ → 3 R2С = O + 2 Cr3+ + 6 часов2О
Приложения
Триоксид хрома в основном используется в хромирование. Обычно его используют с добавками, которые влияют на процесс нанесения покрытия, но не реагируют с триоксидом. Триоксид реагирует с кадмий, цинк, и другие металлы для создания пассивирующих хроматных пленок, стойких к коррозия. Он также используется в производстве синтетические рубины. Раствор хромовой кислоты также используется при нанесении видов анодное покрытие к алюминий, которые в основном используются в аэрокосмической отрасли. На Международной космической станции он используется для контроля роста бактерий в резервуаре для сточных вод. Хромовая кислота /фосфорная кислота решение также является предпочтительным зачистной агент анодных покрытий всех типов.
Безопасность
Триоксид хрома очень токсичен, вызывает коррозию и канцерогенность.[11] Это главный пример шестивалентный хром, экологическая опасность.[12]Родственные производные хрома (III) не особенно опасны; таким образом, восстановители используются для разрушения образцов хрома (VI).
Триоксид хрома, являясь мощным окислителем, воспламеняет такие органические материалы, как спирты при контакте.
Изображений

Концентрированный раствор дихромата калия в воде.

Добавление в раствор серной кислоты.

Кристаллизация триоксида хрома из реакции.
Взаимодействие триоксида хрома и этанола
Рекомендации
- ^ а б c d е Лиде, Дэвид Р., изд. (2009). CRC Справочник по химии и физике (90-е изд.). Бока-Ратон, Флорида: CRC Press. ISBN 978-1-4200-9084-0.
- ^ Зейделл, Атертон; Линке, Уильям Ф. (1919). Растворимость неорганических и органических соединений (2-е изд.). Компания Д. Ван Ностранд. п.250.
- ^ «оксид хрома (VI)». chemister.ru.
- ^ Прадёт, Патнаик (2003). Справочник неорганических химикатов. Компании McGraw-Hill, Inc. ISBN 0-07-049439-8.
- ^ а б c Сигма-Олдрич Ко., Оксид хрома (VI). Проверено 15 июня 2014.
- ^ а б c d «Триоксид хрома». Chemicalland21.com. AroKor Holdings Inc. Получено 2014-06-15.
- ^ а б Гнев, G .; Halstenberg, J .; Hochgeschwender, K .; Scherhag, C .; Korallus, U .; Knopf, H .; Schmidt, P .; Олингер, М. (2000). «Соединения хрома». Энциклопедия промышленной химии Ульмана. Дои:10.1002 / 14356007.a07_067. ISBN 3527306730.
- ^ а б Коттон, Ф. Альберт; Уилкинсон, Джеффри; Мурильо, Карлос А .; Бохманн, Манфред (1999), Продвинутая неорганическая химия (6-е изд.), Нью-Йорк: Wiley-Interscience, ISBN 0-471-19957-5
- ^ Стивенс, Дж. С .; Круикшанк, Д. В. Дж. (1970). «Кристаллическая структура (CrO3)∞". Acta Crystallographica Раздел B. 26 (3): 222. Дои:10.1107 / S0567740870002182.
- ^ Zhai, H.J .; Li, S .; Диксон, Д. А .; Ван, Л. С. (2008). «Исследование электронных и структурных свойств кластеров оксида хрома. (CrO
3)−
п и (CrO3)п (п = 1–5): Фотоэлектронная спектроскопия и функциональные расчеты плотности ». Журнал Американского химического общества. 130 (15): 5167–77. Дои:10.1021 / ja077984d. PMID 18327905. - ^ «Триоксид хрома (MSDS)». Дж. Т. Бейкер. Архивировано из оригинал на 2015-01-12. Получено 2007-09-13.
- ^ Воздействие шестивалентного хрома на окружающую среду вдохновило биографический голливудский фильм 2000 года. Эрин Брокович.









