Хром (III) ацетат - Chromium(III) acetate
 | |
| Имена | |
|---|---|
| Название ИЮПАК Гидрат ацетата хрома (III) | |
| Другие имена хромацетат, триацетат хрома, этаноат хрома (III) | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.012.646 |
PubChem CID | |
| |
| |
| Характеристики | |
| C12ЧАС36ClCr3О22 | |
| Молярная масса | 723.84 г · моль−1 |
| Внешность | твердое вещество от серовато-зеленого до голубовато-зеленого |
| Плотность | 1,662 г / см3 |
| -5104.0·10−6 см3/ моль | |
| Структура | |
| восьмигранный | |
| Родственные соединения | |
Родственные соединения | Ацетат марганца (III) Железо (III) ацетат |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
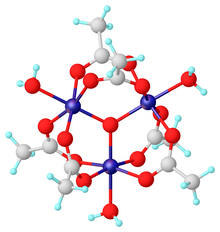
Хром (III) ацетат, широко известный как основной ацетат хрома,[1] описывает семью соли где катион имеет формулу [Cr3О (О2CCH3)6(ОЙ2)3]+. Катион трихрома встречается с различными анионами, такими как хлорид и нитрат. Данные в таблице выше относятся к гексагидрату хлорида [Cr3О (О2CCH3)6(ОЙ2)3] Cl (H2O)6.
Соли основного ацетата хрома давно вызывают интерес из-за его отличительной структуры, которая включает октаэдрические центры Cr (III), тройную мостиковую структуру. оксо лиганд, шесть ацетат лиганды и три акво-лиганды.[1] Такая же структура имеет основной ацетат железа и основной ацетат марганца.[1][2] Существует мало доказательств существования простого ацетата хрома (III), т.е. оксо лиганд.[3] Ацетат хрома (III) представляет собой порошок синего / серо-зеленого цвета, растворимый в воде. Это все еще[2] приготовлен по оригинальной методике 1909 г.[4]

Смотрите также
Рекомендации
- ^ а б c Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ а б Курт Й. Шенк, Ханс У. Гюдель (1982). «Низкотемпературные структурные и спектроскопические свойства [Cr3O (CH3COO)6(ЧАС2O)3] Cl.6H2О ". Неорг. Chem. 21 (6): 2253–2256. Дои:10.1021 / ic00136a025.CS1 maint: использует параметр авторов (связь)
- ^ Эрре, Лилиана Стринна; Мицера, Джованни; Гловяк, Тадеуш; Козловский, Генри (апрель 1997 г.). «Ацетат хрома (III), гидроксид ацетата хрома (III) или µ3-оксоэсакис- (µ2-ацетато-O, O ') - триакватрихром (III) ацетат»? Определение структуры комплексного соединения с помощью аналитических и Спектроскопические методы ». Журнал химического образования. 74 (4): 432. Дои:10.1021 / ed074p432.
- ^ Р. Вайнланд, П. Динкелакер (1909). "Über Salze einer Hexaacetato (formiato) ‐trichrombase. II". Berichte der Deutschen Chemischen Gesellschaft. 42 (3): 2997–3018. Дои:10.1002 / cber.19090420318.CS1 maint: использует параметр авторов (связь)
Ацетилгалогениды и соли ацетат ион | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| AcOH | Он | ||||||||||||||||||
| LiOAc | Быть (OAc)2 BeAcOH | B (OAc)3 | AcOAc ROAc | NH4OAc | AcOOH | FAc | Ne | ||||||||||||
| NaOAc | Mg (OAc)2 | Al (OAc)3 АЛСОЛ Al (OAc)2ОЙ Al2ТАК4(OAc)4 | Si | п | S | ClAc | Ar | ||||||||||||
| KOAc | Ca (OAc)2 | Sc (OAc)3 | Ti (OAc)4 | VO (OAc)3 | Cr (OAc)2 Cr (OAc)3 | Mn (OAc)2 Mn (OAc)3 | Fe (OAc)2 Fe (OAc)3 | Co (OAc)2, Co (OAc)3 | Ni (OAc)2 | Cu (OAc)2 | Zn (OAc)2 | Ga (OAc)3 | Ge | Как (OAc)3 | Se | BrAc | Kr | ||
| RbOAc | Sr (OAc)2 | Y (OAc)3 | Zr (OAc)4 | Nb | Пн (OAc)2 | Tc | Ru (OAc)2 Ru (OAc)3 Ru (OAc)4 | Rh2(OAc)4 | Pd (OAc)2 | AgOAc | CD (OAc)2 | В | Sn (OAc)2 Sn (OAc)4 | Sb (OAc)3 | Te | IAc | Xe | ||
| CsOAc | Ba (OAc)2 | Hf | Та | W | Re | Операционные системы | Ir | Pt (OAc)2 | Au | Hg2(OAc)2, Hg (OAc)2 | TlOAc Tl (OAc)3 | Pb (OAc)2 Pb (OAc)4 | Би (OAc)3 | По | В | Rn | |||
| Пт | Ра | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ц | Og | |||
| ↓ | |||||||||||||||||||
| Ла (OAc)3 | Ce (OAc)Икс | Pr | Nd | Вечера | Sm (OAc)3 | Eu (OAc)3 | Gd (OAc)3 | Tb | Dy (OAc)3 | Хо (OAc)3 | Э | Тм | Yb (OAc)3 | Лу (OAc)3 | |||||
| Ac | Чт | Па | UO2(OAc)2 | Np | Пу | Являюсь | См | Bk | Cf | Es | FM | Мкр | Нет | Lr | |||||
