Сульфат хрома (II) - Chromium(II) sulfate
 | |
| Имена | |
|---|---|
| Название ИЮПАК Сульфат хрома (2+) | |
| Другие имена хромовый сульфат, хромовый сульфат | |
| Идентификаторы | |
| |
| ChemSpider | |
PubChem CID | |
| UNII | |
| |
| Свойства | |
| CrSO4· 5 H2О | |
| Молярная масса | 238,13 (пентагидрат) |
| Внешность | синее твердое вещество (пентагидрат) |
| 21 г / 100 мл (0 ° C, пентагидрат) | |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Сульфат хрома (II) относится к неорганические соединения с химическая формула CrSO4· П H2О. Несколько близкородственных гидратированный соли известны. Пентагидрат представляет собой твердое вещество синего цвета, которое легко растворяется в воде. Растворы хрома (II) легко окисляются воздухом до частиц Cr (III). Растворы Cr (II) используются как специализированные восстановители, имеющие ценность в органический синтез.[1]
Соль получают обработкой металлического хрома водной серной кислотой:[2]
- Cr + H2ТАК4 + 5 часов2O → CrSO4· 5 H2O + H2
Его можно получить в результате реакции сульфат соли и ацетат хрома (II)[3] или, для использования на месте, сокращение сульфат хрома (III) с цинком.[1]
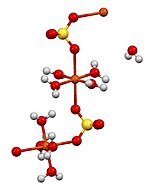
Структура
В водных растворах сульфат хрома (II) образует металлические акво комплексы, предположительно с шестью водными лигандами. Структуры кристаллических солей аналогичны соответствующим гидратам сульфат меди (II): известны пентагидрат, тригидрат, моногидрат и безводные производные сульфата хрома. Во всех этих соединениях центр Cr (II) принимает октаэдрическая координационная геометрия, координируемые с шестью кислородными центрами, образованными комбинацией воды и сульфатных лигандов.[4][5]
использованная литература
- ^ а б A. Zurqiyah и C.E. Castro "Восстановление конъюгированных алкенов сульфатом хрома (II): диэтилсукцинат" Organic Syntheses, Vol. 49, стр.98 (1969).Дои:10.15227 / orgsyn.049.0098
- ^ Справочник по препаративной неорганической химии, 2-е изд. Под редакцией Г. Брауэра, Academic Press, 1963, NY. Vol. 2. п. 1365.
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ Хитчман, Майкл А .; Лихон, Майкл; Макдональд, Робби Дж .; Смит, Питер В .; Незнакомец, Роберт (1987). «Кристаллическая и молекулярная структура пентагидрата сульфата хрома (II), электронные спектры монокристаллов и связывание CrSO4· 5 H2O, пентагидрат сульфата меди и CuSO4· 5 D2О ". Журнал химического общества, Dalton Transactions: 1817–22. Дои:10.1039 / DT9870001817.CS1 maint: использует параметр авторов (ссылка на сайт)
- ^ Dahmen, T .; Glaum, R .; Schmidt, G .; Груэн Р. (1990). «Получение и кристаллическая структура тригидрата сульфата хрома (2+)». Zeitschrift für Anorganische und Allgemeine Chemie. 586: 141–8. Дои:10.1002 / zaac.19905860119.CS1 maint: использует параметр авторов (ссылка на сайт)
| Эта неорганический соединение –Связанная статья является заглушка. Вы можете помочь Википедии расширяя это. |
