Ванадилсульфат - Википедия - Vanadyl sulfate
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Сульфат оксованадия (2+) | |
| Другие имена Основной сульфат ванадия (IV) Сульфат оксида ванадия (IV) Оксисульфат ванадия (IV) | |
| Идентификаторы | |
| |
| ECHA InfoCard | 100.044.214 |
PubChem CID | |
| Номер RTECS |
|
| UNII |
|
| |
| Характеристики | |
| ЧАС10О10SV | |
| Молярная масса | 253.07 г · моль−1 |
| Внешность | Синее твердое вещество |
| Температура плавления | 105 ° С (221 ° F, 378 К) разлагается |
| Растворимый | |
| Опасности | |
| Главный опасности | Раздражающий |
| точка возгорания | Негорючий |
| Родственные соединения | |
Другой анионы | Ванадил хлорид Ванадилнитрат |
Другой катионы | Сульфат ванадия (III) |
Родственные соединения | Ванадил ацетилацетонат |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Ванадил (IV) сульфат описывает коллекцию неорганические соединения ванадия формулы VOSO4(ЧАС2O)Икс где 0 ≤ x ≤ 6. Пентагидрат обычный. Это гигроскопичное твердое вещество синего цвета является одним из наиболее распространенных источников ванадий в лаборатории, что свидетельствует о его высокой стабильности. Он имеет ванадил ион, VO2+, который был назван то «самый стабильный двухатомный ион».[1]
Ванадилсульфат является промежуточным продуктом при экстракции ванадия из нефтяных остатков, одним из коммерческих источников ванадия.[2]
Синтез, структура и реакции
Ванадилсульфат чаще всего получают восстановлением пятиокись ванадия с диоксид серы:
- V2О5 + 7 часов2O + SO2 + H2ТАК4 → 2 [V (O) (H2O)4]ТАК4
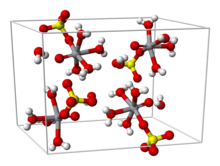
Из водного раствора соль кристаллизуется в виде пентагидрат пятая вода не связана с металлом в твердом теле. Рассматривается как координационный комплекс, ион восьмигранный, с оксо, четырьмя экваториальными водными лигандами и монодентатным сульфатом.[1][3] Тригидрат также исследовали кристаллографией.[4] Гексагидрат существует при температуре ниже 13,6 ° C (286,8 K).[5] Два полиморфы безводного ВОСО4 известны.[6]
Расстояние связи V = O составляет 160вечера, примерно на 50 пм короче, чем V – OH2 облигации. В растворе сульфат-ион быстро диссоциирует.
Широко доступный ванадилсульфат является обычным предшественником других производных ванадила, таких как ванадилацетилацетонат:[7]
- [V (O) (H2O)4]ТАК4 + 2 C5ЧАС8О2 + Na2CO3 → [V (O) (C5ЧАС7О2)2] + Na2ТАК4 + 5 часов2O + CO2
В кислом растворе окисление сульфата ванадила дает производные ванадила (V) желтого цвета. Сокращение, например к цинк, дает производные ванадия (III) и ванадия (II), которые имеют характерный зеленый и фиолетовый цвет соответственно.
Встречаемость в природе
Как и большинство водорастворимых сульфатов, ванадилсульфат редко встречается в природе. Безводная форма - пауфлерит,[8] минерал фумарольный источник. Гидратированные формы, также редкие, включают гексагидрат (станлеит), пентагидраты (минасрагрит, ортоминасрагрит,[9] и анортоминасрагрит) и тригидрат - бобьонесит.[10]
Медицинские исследования
Ванадилсульфат входит в состав пищевых добавок и экспериментальных препаратов. Ванадилсульфат проявляет инсулиноподобные эффекты.[11]
Ванадилсульфат широко изучался в области сахарный диабет исследования как потенциальное средство увеличения инсулин чувствительность. Нет доказательств того, что пероральный прием ванадия улучшает гликемический контроль.[12][13] Лечение ванадием часто приводит к побочным эффектам со стороны желудочно-кишечного тракта, в первую очередь. понос.
Ванадилсульфат также продается как добавка для здоровья, часто для бодибилдинг. Дефицит ванадия приводит к замедлению роста крыс.[14] Его эффективность для бодибилдинга не доказана; некоторые данные свидетельствуют о том, что спортсмены, принимающие его, просто испытывают эффект плацебо.[15]
Рекомендации
- ^ а б Гринвуд, Норман Н.; Эрншоу, Алан (1984). Химия элементов. Оксфорд: Pergamon Press. п. 1157. ISBN 978-0-08-022057-4.
- ^ Гюнтер Бауэр, Фолькер Гютер, Ханс Хесс, Андреас Отто, Оскар Ройдл, Хайнц Роллер, Зигфрид Саттельбергер (2005). «Ванадий и соединения ванадия». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a27_367. ISBN 3527306730.CS1 maint: использует параметр авторов (связь)
- ^ Tachez, M .; Теобальд, Ф. (1980). "Структура пентагидрата сульфата ванадила VO (H2O)5ТАК4 бета (разнообразный орторомбический) ". Acta Crystallographica B. B36: 1757 – p1761. Дои:10.1107 / S0567740880007170.CS1 maint: использует параметр авторов (связь)
- ^ Tachez, M .; Теобальд, Ф. Р. (1980). "Связующий гидроген в кристаллическом тригидрате сульфата ванадила VOSO"4(ЧАС2O)3: Сравнение структурных четвертичных сульфатов ванадил гидрата ». Acta Crystallographica B. 36: 2873–2880. Дои:10.1107 / S056774088001045X.CS1 maint: использует параметр авторов (связь)
- ^ М. Тачез, Ф. Теобальд, Г. Труийо. Кристаллические данные гексагидрата ванадилсульфата VOSO4.6H2O. J. Appl. Cryst. (1976). 9, 246
- ^ Boghosian, S .; Эриксен, К.М .; Fehrmann, R .; Нильсен, К. (1995). «Синтез, переопределение кристаллической структуры и колебательные спектры бета-ВОСО.4". Acta Chemica Scandinavica. 49: 703–708. Дои:10.3891 / acta.chem.scand.49-0703.CS1 maint: использует параметр авторов (связь)Longo, J.M .; Арнотт, Р. Дж. (1970). «Структура и магнитные свойства ВОСО.4". Журнал химии твердого тела. 1 (3–4): 394 – p398. Bibcode:1970JSSCh ... 1..394L. Дои:10.1016/0022-4596(70)90121-0.CS1 maint: использует параметр авторов (связь)
- ^ Bryant, Burl E .; Фернелиус, В. Конард (1957), «Окси (ацетилацетонат) ванадия (IV)», Неорг. Synth., Неорганические синтезы, 5: 113–16, Дои:10.1002 / 9780470132364.ch30, ISBN 9780470132364
- ^ Кривовичев, С.В .; Вергасова, Л. П .; Britvin, S. N .; Филатов, С.К .; Kahlenberg, V .; Ананьев В.В. (1 августа 2007 г.). "Пауфлерит, -ВО (СО4), новый минеральный вид вулкана Толбачик, полуостров Камчатка, Россия ». Канадский минералог. 45 (4): 921–927. Дои:10.2113 / gscanmin.45.4.921.
- ^ Hawthorne, F.C .; Шиндлер, М .; Grice, J.D .; Хейнс, П. (1 октября 2001 г.). «Ортоминасрагрит, V4+O (SO4)(ЧАС2O)5, Новый вид минералов из Темпл-Маунтин, округ Эмери, штат Юта, ОАЭ ". Канадский минералог. 39 (5): 1325–1331. Дои:10.2113 / gscanmin.39.5.1325.
- ^ Шиндлер, М .; Hawthorne, F.C .; Huminicki, D. M.C .; Haynes, P .; Grice, J.D .; Эванс, Х. Т. (1 февраля 2003 г.). «Бобджонесит, V4 + O (So4) (H2O) 3, новый вид минералов из Темпл-Маунтин, округ Эмери, штат Юта, США». Канадский минералог. 41 (1): 83–90. Дои:10.2113 / gscanmin.41.1.83.
- ^ Crans, D. C .; Трухильо, А. М .; Pharazyn, P. S .; Коэн, М. Д. (2011). «Как окружающая среда влияет на активность лекарств: локализация, компартментализация и реакции соединения, повышающего уровень инсулина ванадия, дипиколинатооксованадия (V)». Coord. Chem. Rev. 255 (19–20): 2178–2192. Дои:10.1016 / j.ccr.2011.01.032.
- ^ Ага, Глория Й .; Айзенберг, Дэвид М .; Капчук, Тед Дж .; Филлипс, Рассел С. (2003). «Систематический обзор трав и пищевых добавок для контроля гликемии при диабете». Уход за диабетом. 26 (4): 1277–1294. Дои:10.2337 / diacare.26.4.1277. PMID 12663610.
- ^ Smith, D.M .; Пикеринг, R.M .; Льюит, Г. (31 января 2008 г.). «Систематический обзор пероральных добавок ванадия для контроля гликемии при сахарном диабете 2 типа». QJM. 101 (5): 351–358. Дои:10.1093 / qjmed / hcn003. PMID 18319296.
- ^ Шварц, Клаус; Милн, Дэвид Б. (1971). «Эффекты роста ванадия у крысы». Наука. 174 (4007): 426–428. Bibcode:1971 г. наук ... 174..426С. Дои:10.1126 / science.174.4007.426. JSTOR 1731776. PMID 5112000. S2CID 24362265.
- ^ Talbott, Shawn M .; Хьюз, Керри (2007). "Ванадий". Руководство по диетическим добавкам для медицинского работника. Липпинкотт Уильямс и Уилкинс. С. 419–422. ISBN 978-0-7817-4672-4.
