Оксид рутения (IV) - Ruthenium(IV) oxide
 | |
| Имена | |
|---|---|
| Название ИЮПАК Оксид рутения (IV) | |
| Другие имена Диоксид рутения | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ECHA InfoCard | 100.031.660 |
| Номер ЕС |
|
PubChem CID | |
| |
| |
| Характеристики | |
| RuO2 | |
| Молярная масса | 133,0688 г / моль |
| Внешность | сине-черный твердый |
| Плотность | 6,97 г / см3 |
| Точка кипения | 1200 ° C (2190 ° F, 1470 K) сублимирует |
| нерастворимый | |
| +162.0·10−6 см3/ моль | |
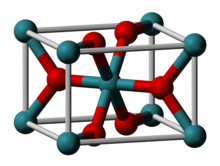
| Структура | |
| Рутил (тетрагональный), tP6 | |
| п42/ммм, № 136 | |
| Октаэдр (RuIV); тригонально планарный (O2−) | |
| Опасности | |
| Паспорт безопасности | Видеть: страница данных |
| точка возгорания | Негорючий |
| Родственные соединения | |
Другой анионы | Дисульфид рутения |
Другой катионы | Оксид осмия (IV) |
| Четырехокись рутения | |
| Страница дополнительных данных | |
| Показатель преломления (п), Диэлектрическая постоянная (εр), так далее. | |
Термодинамический данные | Фазовое поведение твердое тело – жидкость – газ |
| УФ, ИК, ЯМР, РС | |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Оксид рутения (IV) это неорганическое соединение с формулой RUО2. Это черное твердое вещество является наиболее распространенным оксидом рутений. Он широко используется как электрокатализатор для производства хлора, оксидов хлора и O2 катализатор - оксид рутения (IV).[1] Как и многие диоксиды, RuO2 принимает рутил структура.[2][3]
Подготовка
Обычно его получают окислением трихлорид рутения. Практически стехиометрические монокристаллы RuO2 можно получить химический перенос пара, используя O2 в качестве транспортного агента:[4]
- RuO2 + O2 ⇌ RuO4
Фильмы РуО2 может быть подготовлен химическое осаждение из паровой фазы (CVD) из летучих соединений рутения.[5] RuO2 также можно приготовить через гальваника из раствора трихлорида рутения.[6]
Электростатически стабилизированные гидрозоли первичного гидрата диоксида рутения были получены путем использования автокаталитического восстановления четырехокиси рутения в водном растворе. Полученные популяции частиц можно контролировать, чтобы они содержали по существу монодисперсные, однородные сферы с диаметром в диапазоне от 40 до 160 нм.[7]
Использует
Оксид рутения (IV) используется в качестве основного компонента в катализаторе Сумитомо-Дьяконский процесс который производит хлор окислением хлористый водород.[8][9]
RuO2 может использоваться как катализатор во многих других ситуациях. Заслуживают внимания реакции Процесс Фишера-Тропша, Процесс Габера-Боша, и различные проявления топливные элементы.
Потенциальные и нишевые приложения
RuO2 широко используется для покрытия титановых анодов для электролитического производства хлора и для приготовления резисторы или же интегральные схемы.[10][11] Резисторы из оксида рутения могут использоваться в качестве чувствительных термометров в диапазоне температур 0,02
Рекомендации
- ^ Миллс, А. "Гетерогенные окислительно-восстановительные катализаторы выделения кислорода и хлора" Chem. Сот. Rev.,1989, 18, 285-316. Дои:10.1039 / CS9891800285
- ^ Вайкофф, R.W.G .. Кристаллические структуры, Vol. 1. Interscience, John Wiley & Sons: 1963.
- ^ Уэллс, А. Ф. (1975), Структурная неорганическая химия (4-е изд.), Оксфорд: Clarendon Press
- ^ Харальд Шефер, Герд Шнайдерайт, Вильфрид Герхардт "Zur Chemie der Platinmetalle. RuO2 Chemischer Transport, Eigenschaften, thermischer Zerfall" Z. anorg. allg. Chem. 1963, 319, 327-336. Дои:10.1002 / zaac.19633190514
- ^ Pizzini, S .; Buzzancae, G .; Мат. Res. Бык., 1972, 7, 449-462.
- ^ Ли, С. (2003). «Электрохромизм тонких пленок аморфного оксида рутения».. Ионика твердого тела. 165 (1–4): 217–221. Дои:10.1016 / j.ssi.2003.08.035.
- ^ Макмеррей, Х. Н. (1993). «Однородные коллоиды гидрата диоксида рутения, образовавшиеся в результате катализируемого поверхностью восстановления четырехокиси рутения». Журнал физической химии. 97 (30): 8039–8045. Дои:10.1021 / j100132a038.
- ^ Гельмут Фогт, Ян Балей, Джон Э. Беннетт, Питер Винцер, Саид Акбар Шейх, Патрицио Галлоне «Окиси хлора и кислородные кислоты хлора» в Энциклопедии промышленной химии Ульмана 2002, Wiley-VCH. Дои:10.1002 / 14356007.a06_483
- ^ Секи, К; Катал. Surv. Азия, 2010, 14, 168 Дои:10.1007 / s10563-010-9091-7.
- ^ Де Нора, О .; Chem. Англ. Техн., 1970, 42, 222.
- ^ Iles, G.S .; Platinum Met. Ред., 1967,11,126.
- ^ Мэтти, Джонсон. Обзор платиновых металлов. 2002, 46, 3, 105
- ^ Ким, Иль-Хван; Ким, Кван-Бом; Электрохим. Solid-State Lett., 2001, 4, 5, А62-А64
