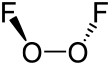Дифторид кислорода - Dioxygen difluoride
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Дифторид кислорода | |||
| Систематическое название ИЮПАК Фтороксигипофторит | |||
Другие имена
| |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| Сокращения | FOOF | ||
| ЧЭБИ | |||
| ChemSpider | |||
| 1570 | |||
PubChem CID | |||
| UNII | |||
| |||
| |||
| Характеристики | |||
| О 2F 2 | |||
| Молярная масса | 69,996 г · моль−1 | ||
| Внешность | оранжевый как твердое вещество красный как жидкость | ||
| Плотность | 1,45 г / см3 (на б.п.) | ||
| Температура плавления | -154 ° С (-245 ° F, 119 К) | ||
| Точка кипения | -57 ° C (-71 ° F, 216 K) экстраполированный | ||
| Растворимость в других растворителях | разлагается | ||
| Термохимия | |||
Теплоемкость (C) | 62,1 Дж / (моль · К) | ||
Стандартный моляр энтропия (S | 277,2 Дж / (моль · К) | ||
Станд. Энтальпия формирование (ΔжЧАС⦵298) | 19,2 кДж / моль | ||
Свободная энергия Гиббса (Δжграмм˚) | 58,2 кДж / моль | ||
| Родственные соединения | |||
Родственные соединения | |||
| Опасности | |||
Классификация ЕС (DSD) (устарело) | |||
| NFPA 704 (огненный алмаз) | |||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Дифторид кислорода это сложный из фтор и кислород с молекулярная формула О
2F
2. Он может существовать в виде твердого вещества оранжевого цвета, которое плавится в красную жидкость при -163 ° C (110 K). Это чрезвычайно сильный окислитель и разлагается превращается в кислород и фтор даже при -160 ° C (113 K) со скоростью 4% в день: таким образом, его время жизни при комнатной температуре чрезвычайно короткое.[1] Дифторид диоксида активно реагирует практически со всеми химическими веществами, с которыми он сталкивается, даже с обычными лед - ведущий к своему звукоподражательный прозвище "FOOF"(игра на его химическом строении и его взрывных тенденциях).
Подготовка
Дифторид диоксида можно получить, подвергая смесь газообразного фтора и кислорода 1: 1 при низком давлении (7-17мм рт. ст. (0.9–2.3 кПа ) оптимально) до электрического разряда 25–30мА при 2,1–2,4кВ.[2]Аналогичный метод был использован для первого синтеза. Отто Рафф в 1933 г.[3] Другой синтез предполагает смешивание О
2 и F
2 в нержавеющая сталь сосуд охлаждали до -196 ° C (77,1 K), а затем подвергали элементы воздействию 3 МэВ тормозное излучение в течение нескольких часов. Третий метод требует нагревания смеси фтора и кислорода до 700 ° C (1292 ° F), а затем быстрого охлаждения с помощью жидкий кислород.[4] Все эти методы включают синтез по уравнению
- О
2 + F
2 → О
2F
2
Это также происходит из термическое разложение из дифторид озона:[5]
- О
3F
2 → О
2F
2 + 1⁄2 О
2
или же
- 2 О
3F
2 → 2 О
2F
2 + О
2
Структура и свойства
В О
2F
2, кислород относится к необычным степень окисления +1. В большинстве других соединений кислород имеет степень окисления -2.
Структура дифторида кислорода напоминает структуру дифторида кислорода. пероксид водорода, ЧАС
2О
2, в своем большом двугранный угол, что приближается к 90 ° и C2 симметрия. Эта геометрия соответствует предсказаниям Теория VSEPR.

Связывание внутри дифторида кислорода было предметом серьезных предположений, особенно из-за очень короткого расстояния O-O и большого расстояния O-F. Длина связи O-O находится в пределах 2 мкм от 120,7 вечера расстояние для двойной связи O = O в дикислород молекула О
2. Для объяснения этого было предложено несколько систем связывания, в том числе O-O тройной связь с одинарными связями O-F, дестабилизированными и удлиненными за счет отталкивания между одинокие пары на атомы фтора и π орбитали связи O-O.[6] Отталкивание с участием неподеленных пар фтора также является причиной длительного и слабого ковалентная связь в молекуле фтора.Вычислительная химия указывает на то, что дифторид кислорода имеет чрезвычайно высокий барьер для вращения 81,17 кДж / моль вокруг связи O-O (в перекиси водорода барьер составляет 29,45 кДж / моль), это близко к энергии диссоциации связи O-F, равной 81,59 кДж / мол.[7]
В 19F ЯМР химический сдвиг дифторида кислорода составляет 865 частей на миллион, что, безусловно, является самым высоким химическим сдвигом, зарегистрированным для ядра фтора, что подчеркивает исключительные электронные свойства этого соединения. Несмотря на его нестабильность, термохимические данные для О
2F
2 были составлены.[8]
Реактивность
Состав легко разлагается на кислород и фтор. Даже при температуре -160 ° C (113 K) 4% разлагается каждый день.[1] этим процессом:
- О
2F
2 → О
2 + F
2
Другое главное свойство этого нестабильного соединения - это его окисляющий мощности, хотя большинство экспериментальных реакций проводилось при температуре около -100 ° C (173 K).[9] Несколько экспериментов с составом привели к серии пожаров и взрывов. Некоторые из соединений, которые вызывали бурную реакцию с О
2F
2 включают этиловый спирт, метан, аммиак, и даже ледяная вода.[9]
С BF
3 и ПФ
5, это дает соответствующее диоксигенил соли:[1][10]
- 2 О
2F
2 + 2 ПФ
5 → 2 [O
2]+
[ПФ
6]−
+ F
2
Использует
В настоящее время соединение не имеет практического применения, но представляет теоретический интерес. Одна лаборатория использовала его для синтеза гексафторид плутония при беспрецедентно низких температурах, что было важно, потому что предыдущие методы приготовления требовали настолько высоких температур, чтобы образовавшийся гексафторид плутония быстро разлагался.[11]
Смотрите также
Рекомендации
- ^ а б c Холлеман, А. Ф .; Виберг, Э. (2001). Неорганическая химия. Академическая пресса. ISBN 978-0-12-352651-9.
- ^ Квасник, В. (1963). «Дифторид кислорода». В Брауэре, Г. (ред.). Справочник по препаративной неорганической химии. 1 (2-е изд.). Нью-Йорк: Academic Press. п. 162.
- ^ Ruff, O .; Mensel, W. (1933). "Neue Sauerstoffluoride: О
2F
2 унд OF ". Zeitschrift für anorganische und allgemeine Chemie. 211 (1–2): 204–208. Дои:10.1002 / zaac.19332110122. - ^ Миллс, Томас (1991). «Прямой синтез жидкофазного дифторида кислорода». Журнал химии фтора. 52 (3): 267–276. Дои:10.1016 / S0022-1139 (00) 80341-3.
- ^ Киршенбаум, А.Д .; Гросс, А. В. (1959). «Фторид озона или триоксигендифторид, О
3F
2". Журнал Американского химического общества. 81 (6): 1277. Дои:10.1021 / ja01515a003. - ^ Бриджман, А. Дж .; Ротери, Дж. (1999). «Склеивание в смеси галогена и перекиси водорода». Журнал химического общества, Dalton Transactions. 1999 (22): 4077–4082. Дои:10.1039 / a904968a.
- ^ Крака, Эльфи; Он, Юань; Кремер, Дитер (2001). «Квантово-химические описания FOOF: нерешенная проблема предсказания его равновесной геометрии». Журнал физической химии A. 105 (13): 3269–3276. Bibcode:2001JPCA..105.3269K. Дои:10.1021 / jp002852r.
- ^ Лайман, Джон Л. (1989). «Термодинамические свойства дифторида кислорода (O2F2) и фторид кислорода (O2F) " (PDF). Американское химическое общество и Американский институт физики Национального института стандартов и технологий.. Получено 5 августа 2013. Цитировать журнал требует
| журнал =(помощь) - ^ а б Streng, А. Г. (1963). «Химические свойства дифторида кислорода». Журнал Американского химического общества. 85 (10): 1380–1385. Дои:10.1021 / ja00893a004.
- ^ Соломон, Ирвин Дж .; Брабец, Роберт I .; Уениши, Рой К .; Кейт, Джеймс Н .; Макдонаф, Джон М. (1964). «Новые диоксигенильные соединения». Неорганическая химия. 3 (3): 457. Дои:10.1021 / ic50013a036.
- ^ Malm, J.G .; Eller, P. G .; Аспри, Л. Б. (1984). «Низкотемпературный синтез гексафторида плутония с использованием дифторида кислорода». Журнал Американского химического общества. 106 (9): 2726–2727. Дои:10.1021 / ja00321a056.
внешняя ссылка
- Перфторпероксид в Linstrom, Peter J .; Маллард, Уильям Г. (ред.); Веб-книга NIST Chemistry, стандартная справочная база данных NIST номер 69, Национальный институт стандартов и технологий, Гейтерсбург (Мэриленд), http://webbook.nist.gov
- Д. Лоу. "Вещи, с которыми я не буду работать: дифторид кислорода". В трубопроводе.