Тетрафторгидразин - Tetrafluorohydrazine
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК 1,1,2,2-тетрафторгидразин | |
| Другие имена тетрафторид диазота, перфторгидразин, ООН 1955 | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.030.091 |
PubChem CID | |
| |
| |
| Характеристики | |
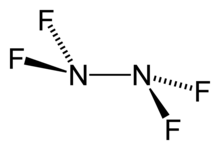
| N2F4 | |
| Молярная масса | 104,01 г моль−1 |
| Температура плавления | -164,5 ° С (-264,1 ° F, 108,6 К) [1] |
| Точка кипения | -73 ° С (-99 ° F, 200 К)[1] |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Тетрафторгидразин или же тетрафторид диазота, N2F4, представляет собой бесцветный реактивный неорганический газ. Это фторированный аналог гидразин. Это очень опасное химическое вещество, которое взрывается в присутствии органический материалы.
Тетрафторгидразин производится из трифторид азота используя утюг катализатор или фторид железа (II). Он используется в некоторых химический синтез, как предшественник или катализатор.
Тетрафторгидразин рассматривался как высокоэнергетическая жидкость. окислитель в некоторых никогда не летающих ракетное горючие формулы в 1959 г.[2]
Характеристики
Тетрафторгидразин находится в равновесии со своим радикальным мономером дифторид азота.[3]
- N2F4 ⇌ 2 НФ2•
При комнатной температуре N2F4 в основном связана только с 0,7% в форме NF2 при давлении 5 мм рт. Когда температура повышается до 225 ° C, он в основном диссоциирует на 99% в виде NF.2.[4]
Энергия, необходимая для разрыва связи N-N в N2F4 составляет 20,8 ккал / моль, с изменением энтропии 38,6 Европа.[4] Для сравнения, энергия диссоциации связи N-N составляет 14,6 ккал / моль в N2О4, 10,2 ккал / моль в N2О2, и 60 ккал / моль в N2ЧАС4. В энтальпия образования из N2F4 (ΔHж) составляет 34,421 кДж / моль.[5]
Рекомендации
- ^ а б Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ Тетрафторгидразин на DTIC.mil, архивировано 12 марта 2007 г.
- ^ Егер, Сюзанна; фон Жуан, Йорн; Келлер-Рудек, Ханнелор; Кошель, Дитер; Кун, Питер; Мерле, Питер; Рупехт, Сигрид; Ванечек, Ганс; Вагнер, Иоахим (1986). Кошель, Дитер; Кун, Питер; Мерле, Питер; Рупрехт, Сигрид; Вагнер, Иоахим (ред.). F Фтор: соединения с кислородом и азотом. Справочник Гмелина по неорганической химии. 4. Берлин: Springer. п. 162. Дои:10.1007/978-3-662-06339-2. ISBN 978-3-662-06341-5. Получено 29 августа 2015.
- ^ а б Бон, Роберт К .; Бауэр, Саймон Харви (февраль 1967). «Электронографическое исследование структур НФ.2 и н2F4". Неорганическая химия. 6 (2): 304–309. Дои:10.1021 / ic50048a024. размеры и углы молекул
- ^ «Азот дифторид NF2(грамм)". www.chem.msu.su.
