Триоксид рения - Rhenium trioxide
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Триоксид рения | |||
| Другие имена Рения | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ECHA InfoCard | 100.013.845 | ||
| Номер ЕС |
| ||
PubChem CID | |||
| UNII | |||
| |||
| |||
| Характеристики | |||
| ReO3 | |||
| Молярная масса | 234,205 г / моль | ||
| Внешность | Темно-красные кристаллы | ||
| Плотность | 6,92 г / см3 | ||
| Температура плавления | 400 ° С (752 ° F, 673 К) (разлагается) | ||
| +16.0·10−6 см3/ моль | |||
| 1.68 | |||
| Структура | |||
| Кубический, cP4 | |||
| пм3м, № 221 | |||
а = 374,8 вечера | |||
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
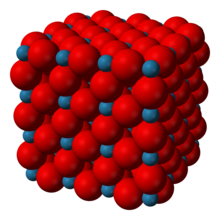

Триоксид рения или же оксид рения (VI) является неорганическое соединение с формулой ReO3. Это красное твердое вещество с металлическим блеском, напоминающее медь по внешнему виду. Это единственная конюшня триоксид элементов группы 7 (Mn, Tc, Re ).
Подготовка и состав
Триоксид рения можно получить путем восстановления оксид рения (VII) с монооксид углерода при 200 ° C или элементарно рений при 400 ° С. [1]
- Re2О7 + CO → 2 ReO3 + CO2
- 3 Re2О7 + Re → 7 ReO3
Re2О7 также можно уменьшить с помощью диоксан.[2]
Триоксид рения кристаллизуется с примитивный кубический ячейка, с параметр решетки из 3,742 Å (374.2 вечера ). Структура РеО3 похож на перовскит (НПА3) без большого катиона A в центре элементарной ячейки. Каждый центр рения окружен октаэдр определяется шестью кислородными центрами. Эти октаэдры имеют общие углы, образуя трехмерную структуру. Координационное число O равно 2, потому что каждый атом кислорода имеет 2 соседних атома Re.[3]
Характеристики
Физические свойства
ReO3 необычно для оксида, потому что он показывает очень низкую удельное сопротивление. Он ведет себя как металл в том, что его удельное сопротивление уменьшается с понижением температуры. В 300 K, его удельное сопротивление 100.0 нОм · м, тогда как при 100 К она уменьшается до 6,0 нОм · м, что в 17 раз меньше, чем при 300 К.[3]
Химические свойства
Триоксид рения не растворяется в воде, а также в разбавленных кислотах и щелочах. Нагрев в основании приводит к непропорциональность давать ReO
2 и ReO−
4, а реакция с кислотой при высокой температуре дает Re
2О
7. В концентрированной азотной кислоте дает перреновая кислота.При нагревании до 400 ° C в вакууме непропорциональность:[2]
- 3 РеО3 → Re2О7 + ReO2
Использует
Катализатор гидрирования
Триоксид рения находит применение в органический синтез как катализатор за восстановление амида.[4]
Рекомендации
- ^ Х. Нечамкин, К. Ф. Хиски, «Рений (VI): оксид (триоксид рения)», неорганический синтез, 1950, том 3, стр. 186-188. Дои:10.1002 / 9780470132340.ch49
- ^ а б G. Glemser "Оксид рения (VI)" Справочник по препаративной неорганической химии, 2-е изд. Под редакцией Г. Брауэра, Academic Press, 1963, NY. Vol. 2. п. 1482.
- ^ а б Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8., п. 1047.
- ^ Нисимура, Шигео (2001). Справочник по гетерогенному каталитическому гидрированию для органического синтеза (1-е изд.). Нью-Йорк: Wiley-Interscience. п. 408. ISBN 9780471396987.


