Перекись - Peroxide
 | |
| Имена | |
|---|---|
| Название ИЮПАК диоксид (2-) | |
| Другие имена # перекись | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| 486 | |
| |
| |
| Характеристики | |
| О2− 2 | |
| Молярная масса | 31.998 г · моль−1 |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
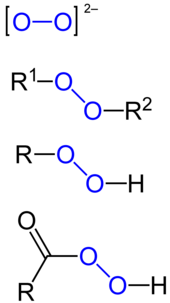
Перекиси представляют собой группу соединений со структурой R − O − O − R.[1] Группа O-O в пероксиде называется пероксидная группа или же пероксогруппа. В отличие от оксидные ионы, то кислород атомы в ионе перекиси есть степень окисления -1.
Самая распространенная перекись - это пероксид водорода (ЧАС2О2), в просторечии известный как «перекись». Он продается в виде раствора в воде при различных концентрациях. Поскольку перекись водорода почти бесцветна, эти растворы тоже. В основном используется как окислитель и отбеливание агент. Однако перекись водорода также вырабатывается в организме человека биохимически, в основном в результате ряда оксидаза ферменты.[2] Концентрированные растворы потенциально опасны при контакте с органическими соединениями.

Помимо перекиси водорода, некоторые другие основные классы перекисей:
- Пероксикислоты, пероксипроизводные многих известных кислот, примерами которых являются пероксимоносерная кислота и перуксусная кислота, и их соли, одним из примеров которых является пероксидисульфат калия.
- Пероксиды основной группы, соединения со связью E − O − O − E (E = элемент основной группы ).
- Пероксиды металлов, примеры являются перекись бария (BaO2) и перекись натрия (Na2О2).
- Органические пероксиды, соединяется со связью C-O-O-C или C-O-O-H. Одним из примеров является терт-бутилгидропероксид.
Рекомендации
- ^ ИЮПАК, Сборник химической терминологии, 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "перекиси ". Дои:10.1351 / goldbook.P04510
- ^ Холливелл, Барри; Клемент, Мари Вероник; Лонг, Ли Хуа (2000). «Перекись водорода в организме человека». Письма FEBS. 486 (1): 10–3. Дои:10.1016 / S0014-5793 (00) 02197-9. PMID 11108833.
