Тетракарбонил никеля - Nickel tetracarbonyl
 | |||
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Тетракарбонилникель | |||
| Другие имена Тетракарбонил никеля Карбонил никеля | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| 6122797 | |||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.033.322 | ||
| Номер ЕС |
| ||
| 3135 | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1259 | ||
| |||
| |||
| Характеристики | |||
| Ni (CO)4 | |||
| Молярная масса | 170,73 г / моль | ||
| Внешность | бесцветная жидкость[1] | ||
| Запах | затхлый[1] как кирпичная пыль | ||
| Плотность | 1,319 г / см3 | ||
| Температура плавления | -17,2 ° С (1,0 ° F, 256,0 К) | ||
| Точка кипения | 43 ° С (109 ° F, 316 К) | ||
| 0,018 г / 100 мл (10 ° С) | |||
| Растворимость | смешивается в большинстве органические растворители растворим в азотная кислота, царская водка | ||
| Давление газа | 315 мм рт. Ст. (20 ° С)[1] | ||
| Вязкость | 3,05 х 10−4 Па с | ||
| Структура | |||
| Тетраэдр | |||
| Тетраэдр | |||
| нуль | |||
| Термохимия | |||
Стандартный моляр энтропия (S | 320 Дж К−1 моль−1 | ||
Станд. Энтальпия формирование (ΔжЧАС⦵298) | −632 кДж / моль | ||
Станд. Энтальпия горение (ΔcЧАС⦵298) | −1180 кДж / моль | ||
| Опасности | |||
| Паспорт безопасности | ICSC 0064 | ||
| Пиктограммы GHS |     | ||
| H225, H300, H310, H330, H351, H360D, H400, H410 | |||
| P201, P202, P210, P233, P240, P241, P242, P243, P260, P271, P273, P280, P281, P284, P303 + 361 + 353, P304 + 340, P308 + 313, P310, P320, P370 + 378, P391, P403 + 233, P403 + 235, P405, P501 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 4 ° С (39 ° F, 277 К) | ||
| 60 ° С (140 ° F, 333 К) | |||
| Пределы взрываемости | 2–34% | ||
| Смертельная доза или концентрация (LD, LC): | |||
LC50 (средняя концентрация ) | 266 частей на миллион (кошка, 30 мин) 35 частей на миллион (кролик, 30 мин) 94 ppm (мышь, 30 мин) 10 частей на миллион (мышь, 10 мин)[2] | ||
LCLo (самый низкий опубликованный ) | 360 ppm (собака, 90 мин) 30 частей на миллион (человек, 30 мин) 42 частей на миллион (кролик, 30 мин) 7 частей на миллион (мышь, 30 мин)[2] | ||
| NIOSH (Пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 0,001 частей на миллион (0,007 мг / м3)[1] | ||
REL (Рекомендуемые) | TWA 0,001 частей на миллион (0,007 мг / м3)[1] | ||
IDLH (Непосредственная опасность) | Ca [2 частей на миллион][1] | ||
| Родственные соединения | |||
Связанный карбонилы металлов | Пентакарбонил железа Дикобальт октакарбонил | ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Карбонил никеля (ИЮПАК имя: тетракарбонилникель) это никелевоорганическое соединение с формула Ni (CO)4. Эта бесцветная жидкость является основным карбонил из никель. Это промежуточное звено в Мондовский процесс для производства очень чистой никель и реагент в металлоорганическая химия, хотя Мондовский процесс вышел из общего использования из-за опасности для здоровья при работе с компаундом. Карбонил никеля - одно из наиболее опасных веществ, встречающихся в химии никеля, из-за его очень высокой токсичности, высокой летучести и быстрого всасывания через кожу.[3]
Структура и склеивание
В тетракарбониле никеля степень окисления для никеля принимается равным нулю. Формула соответствует Правило 18 электронов. Молекула четырехгранный, с четырьмя карбонил (монооксид углерода ) лиганды. Электронная дифракция Были проведены исследования этой молекулы, и расстояния Ni – C и C – O были рассчитаны и составили 1,838 (2) и 1,141 (2) ангстрем соответственно.[4]
Подготовка
Ni (CO)4 был впервые синтезирован в 1890 г. Людвиг Монд путем прямой реакции металлического никеля с CO.[5] Эта новаторская работа предвосхитила существование многих других карбонильных соединений металлов, в том числе соединений V, Cr, Mn, Fe и Co. К концу 19 века она также применялась в промышленности для очистки никеля.[6]
При 323 К (50 ° C; 122 ° F) окись углерода проходит над нечистым никелем. Оптимальная скорость достигается при 130 ° C.[7]
Лабораторные маршруты
Ni (CO)4 не является коммерчески доступным. Его удобно генерировать в лаборатории с помощью карбонилирование коммерчески доступных бис (циклооктадиен) никель (0).[8] Его также можно получить восстановлением аммиачных растворов сульфата никеля с дитионит натрия в атмосфере CO.[9]
Реакции

Термическое декарбонилирование
При умеренном нагреве Ni (CO)4 разлагается до окиси углерода и металлического никеля. В сочетании с легким образованием CO и даже очень нечистого никеля это разложение является основой для Мондовский процесс для очистки никеля или нанесения покрытия на поверхности. Термическое разложение начинается около 180 ° C и увеличивается при повышении температуры.[7]
Реакции с нуклеофилами и восстановителями
Как и другие карбонилы низковалентных металлов, Ni (CO)4 подвержен атаке нуклеофилов. Атака может происходить на никелевом центре, что приводит к вытеснению лигандов CO, или на CO. Таким образом, донорные лиганды, такие как трифенилфосфин реагируют с образованием Ni (CO)3(PPh3) и Ni (CO)2(PPh3)2. Бипиридин и родственные лиганды ведут себя аналогичным образом.[10] Монозамещение тетракарбонила никеля другими лигандами можно использовать для определения Электронный параметр Толмана, мера способности данного лиганда отдавать или снимать электроны.
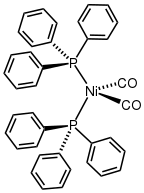 Структура Ni (PPh3)2(CO)2.
Структура Ni (PPh3)2(CO)2.
Лечение с гидроксиды дает кластеры, такие как [Ni5(CO)12]2− и [Ni6(CO)12]2−. Эти соединения также можно получить восстановлением карбонила никеля.
Таким образом, обработка Ni (CO)4 с углеродными нуклеофилами (Nu−) приводит к ацильным производным, таким как [Ni (CO)3C (O) Nu)]−.[11]
Реакции с электрофилами и окислителями
Карбонил никеля может быть окисленный. Хлор окисляет карбонил никеля до NiCl2, выделяя газ CO. Аналогично ведут себя и другие галогены. Эта реакция обеспечивает удобный метод осаждения никелевой части токсичного соединения.
Реакции Ni (CO)4 с алкил- и арилгалогенидами часто приводят к карбонилированным органическим продуктам. Виниловый галогениды, такие как PhCH = CHBr, превращаются в ненасыщенные сложные эфиры после обработки Ni (CO)4 затем метоксид натрия. Такие реакции, вероятно, также протекают через окислительная добавка. Аллильные галогениды образуют соединения π-аллилникеля, такие как (аллил)2Ni2Cl2:[12]
- 2 Ni (CO)4 + 2 ClCH2CH = CH2 → Ni2(μ-Cl)2(η3-C3ЧАС5)2 + 8 СО
Соображения токсикологии и безопасности
Опасности Ni (CO)4 намного больше, чем подразумевается в его содержании CO, отражая эффекты никеля, если он высвобождается в организме. Карбонил никеля может быть смертельным при попадании через кожу или, что более вероятно, при вдыхании из-за его высокой летучести. Его LC50 для 30-минутной экспозиции оценивается в 3промилле, а концентрация, которая является смертельной для человека, составит 30 частей на миллион. Некоторые субъекты, подвергавшиеся воздействию затяжек до 5 частей на миллион, описывали запах как затхлый или сажистый, но, поскольку это соединение чрезвычайно токсично, его запах не обеспечивает надежного предупреждения о потенциально смертельном воздействии.[13]
Пары Ni (CO)4 может самовоспламеняться. Пар разлагается быстро в воздухе, с периодом полураспада около 40 секунд.[14]
Отравление карбонилом никеля характеризуется двухэтапным течением болезни. Первый состоит из головные боли и грудная боль длится несколько часов, обычно после короткой ремиссии. Второй этап - это химический пневмонит который обычно начинается через 16 часов с симптомов кашля, одышки и сильной усталости. Они достигают наибольшей степени тяжести через четыре дня, что может привести к смерти от кардиореспираторной или острая травма почек. Выздоровление часто бывает очень длительным, часто осложняется истощением, депрессия и одышка при напряжении. Постоянное поражение органов дыхания - явление необычное. В канцерогенность Ni (CO)4 является предметом споров, но считается важным.
Классифицируется как чрезвычайно опасное вещество в Соединенных Штатах, как определено в Разделе 302 США Закон о чрезвычайном планировании и праве общества на информацию (42 U.S.C. 11002), и к ним предъявляются строгие требования к отчетности со стороны предприятий, которые производят, хранят или используют его в значительных количествах.[15]
В популярной культуре
«Реквием по живым» (1978), эпизод Куинси, M.E., показывает отравленного умирающего криминального авторитета, который просит доктора Куинси вскрыть его все еще живое тело. Куинси определяет яд - карбонил никеля.
Рекомендации
- ^ а б c d е ж Карманный справочник NIOSH по химической опасности. "#0444". Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б «Карбонил никеля». Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ Индекс Merck (7-е изд.). Merck.
- ^ Hedberg, L .; Иидзима, Т .; Хедберг, К. (1979). "Тетракарбонил никеля, Ni (CO)4. I. Молекулярная структура по данным дифракции электронов в газах. II. Уточнение квадратичного силового поля ». Журнал химической физики. 70 (7): 3224–3229. Дои:10.1063/1.437911.
- ^ Монд, Л.; Langer, C .; Квинке, Ф. (1890). «Действие окиси углерода на никель». J. Chem. Soc. Пер. 57: 749–753. Дои:10.1039 / CT8905700749.
- ^ «Извлечение никеля из руд с помощью процесса Монда». Природа. 59 (1516): 63–64. 1898. Дои:10.1038 / 059063a0.
- ^ а б Lascelles, K .; Morgan, L.G .; Nicholls, D .; Бейерсманн, Д. «Соединения никеля». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a17_235.pub2.
- ^ Веселый, П. У. (1982). «Никель Тетракарбонил». В Abel, Edward W .; Стоун, Ф. Гордон А.; Уилкинсон, Джеффри (ред.). Комплексная металлоорганическая химия. я. Оксфорд: Pergamon Press. ISBN 0-08-025269-9.
- ^ Ф. Зил (1963). «Карбонил никеля». В Г. Брауэре (ред.). Справочник по препаративной неорганической химии. 2 (2-е изд.). Нью-Йорк: Academic Press. С. 1747–1748.
- ^ Elschenbroich, C .; Зальцер, А. (1992). Металлоорганические соединения: краткое введение (2-е изд.). Вайнхайм: Вайли-ВЧ. ISBN 3-527-28165-7.
- ^ Пинхас, А. Р. (2003). «Тетракарбонилникель». Энциклопедия реагентов для органического синтеза, 8 томов. Энциклопедия реагентов для органического синтеза. Джон Вили и сыновья. Дои:10.1002 / 047084289X.rt025m. ISBN 0471936235.
- ^ Semmelhack, M. F .; Хелквист П. М. (1972). «Реакция арилгалогенидов с галогенидами π-аллилникеля: металлилбензол». Органический синтез. 52: 115.; Коллективный объем, 6, п. 722
- ^ Совет по экологическим исследованиям и токсикологии (2008 г.). «Карбонил никеля: рекомендуемые уровни острого воздействия». Рекомендуемые уровни острого воздействия для отдельных переносимых по воздуху химических веществ. 6. Национальная академия прессы. С. 213–259.
- ^ Стедман, Д. Х .; Хикаде, Д. А .; Pearson, R. Jr .; Ялвац, Э. Д. (1980). «Карбонил никеля: разложение на воздухе и связанные с ним кинетические исследования». Наука. 208 (4447): 1029–1031. Дои:10.1126 / science.208.4447.1029. PMID 17779026.
- ^ «40 C.F.R .: Приложение A к Части 355 - Список особо опасных веществ и их планируемые пороговые количества» (PDF) (1 июля 2008 г. ред.). Государственная типография. Архивировано из оригинал (PDF) 25 февраля 2012 г.. Получено 29 октября, 2011. Цитировать журнал требует
| журнал =(помощь)
дальнейшее чтение
- Ши, З. (1991). «Карбонил никеля: токсичность и здоровье человека». Наука об окружающей среде в целом. 148 (2–3): 293–298. Дои:10.1016/0048-9697(94)90406-5. PMID 8029705.
- Сандерман, Ф. В. (1989). «Паломничество в архивы токсикологии никеля». Анналы клинической и лабораторной науки. 19 (1): 1–16. PMID 2644888.
- Армит, Х. В. (1907). «Токсикология карбонила никеля. Часть I». Журнал гигиены. 7 (4): 525–551. Дои:10.1017 / S0022172400033507. ЧВК 2236193. PMID 20474327.
- Армит, Х. У. (1908). «Токсикология карбонила никеля. Часть II». Журнал гигиены. 8 (5): 565–610. Дои:10.1017 / S0022172400015989. ЧВК 2167169. PMID 20474374.
- Barceloux, D.G .; Barceloux, Дональд (1999). «Никель». Клиническая токсикология. 37 (2): 239–258. Дои:10.1081 / CLT-100102423. PMID 10382559.




