Изомераза - Isomerase
Изомеразы являются общим классом ферменты которые превращают молекулу из одного изомер другому. Изомеразы способствуют внутримолекулярным перестройкам, в которых связи разрываются и образуются. Общая форма такой реакции следующая:
А – Б → Б – А
Здесь только один субстрат дает один продукт. У этого продукта такой же молекулярная формула как подложка, но отличается связностью соединений или пространственным расположением. Изомеразы катализируют реакции во многих биологических процессах, например, в гликолиз и углеводный обмен.
Изомеризация
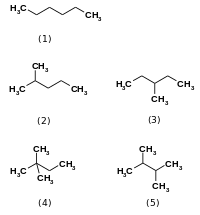

Изомеразы катализировать изменения в пределах одной молекулы.[1] Они превращают один изомер в другой, что означает, что конечный продукт имеет ту же молекулярную формулу, но другую физическую структуру. Изомеры сами по себе существуют во многих разновидностях, но в целом могут быть классифицированы как структурные изомеры или же стереоизомеры. Структурные изомеры имеют разный порядок связей и / или разную связность связей друг с другом, как в случае гексан и его четыре другие изомерные формы (2-метилпентан, 3-метилпентан, 2,2-диметилбутан, и 2,3-диметилбутан ).
Стереоизомеры имеют одинаковое упорядочение отдельных связей и такую же связность, но трехмерное расположение связанных атомов различается. Например, 2-бутен существует в двух изомерных формах: СНГ-2-бутен и транс-2-бутен.[2] Подкатегории изомераз, содержащие рацемазы, эпимеразы и цис-транс-изомеры, являются примерами ферментов, катализирующих взаимное превращение стереоизомеров. Внутримолекулярные лиазы, оксидоредуктазы и трансферазы катализируют взаимопревращение структурных изомеров.
Распространенность каждого изомера в природе частично зависит от энергия изомеризации, разница в энергии между изомерами. Близкие по энергии изомеры могут легко преобразовываться друг в друга, и их часто можно увидеть в сопоставимых пропорциях. Энергия изомеризации, например, для преобразования из стабильного СНГ изомер в менее стабильный транс изомера больше, чем для обратной реакции, что объясняет, почему в отсутствие изомеразы или внешнего источника энергии, такого как ультрафиолетовая радиация данный СНГ изомер обычно присутствует в больших количествах, чем транс изомер. Изомеразы могут увеличивать скорость реакции за счет снижения энергии изомеризации.[3]
Расчет изомеразы кинетика из экспериментальных данных может быть сложнее, чем для других ферментов, потому что использование эксперименты по ингибированию продукта непрактично.[4] То есть изомеризация не необратимая реакция поскольку реакционный сосуд будет содержать один субстрат и один продукт, поэтому типичная упрощенная модель для расчета кинетика реакции не держит. Существуют также практические трудности с определением этап определения ставки при высоких концентрациях при однократной изомеризации. Вместо этого с помощью индикатора можно преодолеть эти технические трудности, если существует две формы несвязанного фермента. Этот метод использует изотопный обмен косвенно измерить взаимопревращение свободного фермента между двумя его формами. Субстрат и продукт с радиоактивной меткой размытый в зависимости от времени. Когда система достигает равновесие добавление немаркированного субстрата нарушает или нарушает баланс. Когда равновесие снова устанавливается, радиоактивно меченные субстрат и продукт отслеживаются для определения энергетической информации.[5]
Самое раннее использование этого метода прояснило кинетику и механизм лежащий в основе действия фосфоглюкомутаза, отдавая предпочтение модели косвенной передачи фосфат с одним средний и прямая передача глюкоза.[6] Затем этот метод был принят для изучения профиля пролин рацемаза и его два состояния: форма, которая изомеризует L-пролин а другой - для D-пролина. При высоких концентрациях было показано, что переходное состояние в этом взаимопревращении ограничение скорости и что эти формы ферментов могут отличаться только протонирование на кислый и базовый группы из активный сайт.[5]
Номенклатура
Обычно «названия изомераз формируются как»субстрат изомераза »(например, еноил-КоА-изомераза ), или как "субстрат тип изомеразы" (Например, фосфоглюкомутаза )."[7]
Классификация
Каждой реакции, катализируемой ферментами, присвоен уникальный классификационный номер. Катализируемые изомеразой реакции имеют свои собственные EC категория: EC 5.[8] Изомеразы подразделяются на шесть подклассов:
Рацемазы, эпимеразы
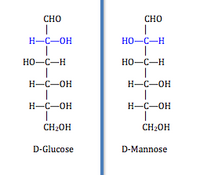
Эта категория (EC 5.1) включает (рацемазы ) и эпимеразы ). Эти изомеразы инвертируют стереохимия в цель хиральный углерод. Рацемазы воздействуют на молекулы с одним хиральным углеродом для инверсии стереохимии, тогда как эпимеразирует целевые молекулы с несколькими хиральными атомами углерода и воздействует на один из них. У молекулы только с одним хиральным углеродом есть два энантиомерный формы, такие как серин имеющий изоформы D-серина и L-серина, различающиеся только абсолютная конфигурация о хиральном углероде. Молекула с несколькими хиральными атомами углерода имеет две формы у каждого хирального углерода. Изомеризация на одном хиральном атоме углерода с несколькими выходами эпимеры, которые отличаются друг от друга по абсолютной конфигурации только одним хиральным атомом углерода.[2] Например, D-глюкоза и D-манноза различаются конфигурацией только у одного хирального углерода. Этот класс далее разбивается на группы, на которые действует фермент:
| Номер ЕС | Описание | Примеры |
|---|---|---|
| EC 5.1.1 | Воздействие на аминокислоты и производные | аланин рацемаза, метионин рацемаза |
| EC 5.1.2 | Воздействие на оксикислоты и производные | лактат рацемаза, тартратная эпимераза |
| EC 5.1.3 | Воздействие на углеводы и производные | рибулозо-фосфат-3-эпимераза, UDP-глюкозо-4-эпимераза |
| 5.1.99 EC | Воздействие на другие соединения | метилмалонил-КоА эпимераза, гидантоин рацемаза |
Цис-транс-изомеразы
В эту категорию (EC 5.2) входят ферменты, катализирующие изомеризацию цис-транс-изомеры. Алкенес и циклоалканы могут иметь цис-транс стереоизомеры. Эти изомеры не отличаются абсолютная конфигурация а скорее положением групп заместителей относительно плоскости отсчета, например, поперек двойной связи или относительно кольцевой структуры. СНГ изомеры имеют группы заместителей на одной стороне и транс изомеры имеют группы на противоположных сторонах.[2]
Эта категория больше не разбивается. Все записи в настоящее время включают:

| Номер ЕС | Примеры |
|---|---|
| EC 5.2.1.1 | Малеат изомераза |
| EC 5.2.1.2 | Малеилацетоацетат изомераза |
| EC 5.2.1.4 | Малеилпируват изомераза |
| EC 5.2.1.5 | Линолеат-изомераза |
| EC 5.2.1.6 | Фурилфурамид изомераза |
| EC 5.2.1.8 | Пептидилпролилизомераза |
| EC 5.2.1.9 | Фарнезол 2-изомераза |
| EC 5.2.1.10 | 2-хлор-4-карбоксиметиленбут-2-ен-1,4-олидизомераза |
| EC 5.2.1.12 | Зета-каротин изомераза |
| EC 5.2.1.13 | Проликопен изомераза |
| EC 5.2.1.14 | Бета-каротин изомераза |
Внутримолекулярные оксидоредуктазы
Эта категория (EC 5.3) включает внутримолекулярный оксидоредуктазы. Эти изомеразы катализируют перенос электроны от одной части молекулы к другой. Другими словами, они катализируют окисление одной части молекулы и одновременное восстановление другой части.[8] Подкатегории этого класса:
| Номер ЕС | Описание | Примеры |
|---|---|---|
| EC 5.3.1 | Взаимопревращение альдозов и кетозов | Триозофосфат изомераза, Рибозо-5-фосфат-изомераза |
| EC 5.3.2 | Взаимопревращение кето- и енольных групп | Фенилпируват таутомераза, Оксалоацетат таутомераза |
| EC 5.3.3 | Транспонирование двойных облигаций C = C | Стероид дельта-изомераза, L-допахром-изомераза |
| EC 5.3.4 | Транспонирование облигаций S-S | Белковая дисульфид-изомераза |
| EC 5.3.99 | Другие внутримолекулярные оксидоредуктазы | Простагландин-D-синтаза, Алленоксидциклаза |
Внутримолекулярные трансферазы
В эту категорию (EC 5.4) входят внутримолекулярные трансферазы (мутазы ). Эти изомеразы катализируют перенос функциональные группы от одной части молекулы к другой.[8] Фосфотрансферазы (EC 5.4.2) были классифицированы как трансферазы (EC 2.7.5) с регенерацией доноров до 1983 года.[9] Этот подкласс можно разбить в зависимости от функциональной группы, которую переносит фермент:

| Номер ЕС | Описание | Примеры |
|---|---|---|
| EC 5.4.1 | Перенос ацильных групп | Лизолецитинацилмутаза, Прекоррин-8Х метилмутаза |
| EC 5.4.2 | Фосфотрансферазы (фосфомутазы) | Фосфоглюкомутаза, Фосфопентомутаза |
| EC 5.4.3 | Перенос аминокислотных групп | Бета-лизин 5,6-аминомутаза, Тирозин-2,3-аминомутаза |
| EC 5.4.4 | Перенос гидроксигрупп | (гидроксиамино) бензолмутаза, Изохоризмат-синтаза |
| 5.4.99 по К.Э. | Перенос других групп | Метиласпартат мутаза, Хоризмат мутаза |
Внутримолекулярные лиазы
В эту категорию (EC 5.5) входят внутримолекулярные лиасы. Эти ферменты катализируют «реакции, в которых группа может рассматриваться как удаленная из одной части молекулы, оставляя двойную связь, оставаясь при этом. ковалентно прикреплен к молекуле ".[8] Некоторые из этих катализируемых реакций включают разрыв кольцевой структуры.
Эта категория больше не разбивается. Все записи в настоящее время включают:
| Номер ЕС | Примеры |
|---|---|
| EC 5.5.1.1 | Муконат циклоизомераза |
| EC 5.5.1.2 | 3-карбокси-цис, цис-муконатциклоизомераза |
| EC 5.5.1.3 | Тетрагидроксиптеридин циклоизомераза |
| EC 5.5.1.4 | Инозитол-3-фосфатсинтаза |
| EC 5.5.1.5 | Карбокси-цис, цис-муконатциклаза |
| EC 5.5.1.6 | Халкон-изомераза |
| EC 5.5.1.7 | Хлормуконат циклоизомераза |
| EC 5.5.1.8 | (+) - борнилдифосфатсинтаза |
| EC 5.5.1.9 | Циклоэукаленол циклоизомераза |
| EC 5.5.1.10 | Альфа-пинен-оксид дециклаза |
| EC 5.5.1.11 | Дихлормуконат циклоизомераза |
| EC 5.5.1.12 | Копалилдифосфатсинтаза |
| EC 5.5.1.13 | Энт-копалилдифосфатсинтаза |
| EC 5.5.1.14 | Син-копалил-дифосфат-синтаза |
| EC 5.5.1.15 | Терпентиенил-дифосфатсинтаза |
| EC 5.5.1.16 | Галимадиенил-дифосфатсинтаза |
| EC 5.5.1.17 | (S) -бета-макрокарпен-синтаза |
| EC 5.5.1.18 | Ликопин-эпсилон-циклаза |
| EC 5.5.1.19 | Ликопин бета-циклаза |
| EC 5.5.1.20 | Просоланапирон-III циклоизомераза |
| EC 5.5.1.n1 | D-рибоза пираназа |
Механизмы изомераз
Расширение и сжатие кольца за счет таутомеров
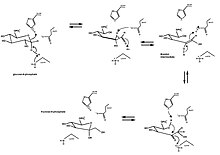
Классическим примером раскрытия и сжатия кольца является изомеризация глюкоза (ан альдегид с шестичленным кольцом) до фруктоза (а кетон с пятичленным кольцом). Превращение D-глюкозо-6-фосфата в D-фруктозо-6-фосфат катализируется глюкозо-6-фосфат изомераза, внутримолекулярный оксидоредуктаза. Общая реакция включает раскрытие кольца с образованием альдозы через кислотно-щелочной катализ и последующее образование промежуточного цис-эндиола. Затем образуется кетоза, и кольцо снова замыкается.
Глюкозо-6-фосфат сначала связывается с активный сайт изомеразы. Изомераза открывает кольцо: ее Его388 остаток протонирует кислород на глюкозном кольце (и тем самым разрыв связи O5-C1) в сочетании с Lys518 депротонирование C1 гидроксил кислород. Кольцо открывается, образуя прямую цепочку. альдоза с кислым протоном C2. Связь C3-C4 вращается и Glu357 (с помощью His388) депронатирует C2 с образованием двойной связи между C1 и C2. А цис-эндиол образуется промежуточный продукт, и кислород C1 протонируется каталитическим остатком, что сопровождается депротонированием кислорода эндиола C2. Прямая цепь кетоза сформирован. Чтобы замкнуть фруктозное кольцо, происходит обратное раскрытие кольца, и кетоза протонируется.[10]
Эпимеризация

Пример эпимеризации находится в цикле Кальвина, когда D-рибулозо-5-фосфат превращается в D-ксилулозо-5-фосфат посредством рибулозо-фосфат-3-эпимераза. Подложка и продукт отличаются только стереохимия на третьем углероде в цепи. Основной механизм включает депротонирование этого третьего углерода с образованием реактивного энолировать средний. Активный центр фермента содержит два Жерех остатки. После связывания субстрата с ферментом первый Asp депротонирует третий углерод с одной стороны молекулы. Это оставляет плоский зр2-гибридизированный средний. Второй Asp расположен на противоположной стороне активной стороны и протонирует молекулу, эффективно добавляя протон с обратной стороны. Эти связанные шаги инвертируют стереохимию у третьего углерода.[11]
Внутримолекулярный перенос

Хоризмат мутаза представляет собой внутримолекулярную трансферазу и катализирует превращение хоризматировать к префенат, используется в качестве прекурсора для L-тирозин и L-фенилаланин у некоторых растений и бактерий. Эта реакция Перестановка Клейзена что может происходить с изомеразой или без нее, хотя скорость увеличивается на 106 складка в присутствии хоризматмутазы. Реакция проходит через стул переходное состояние с подложкой в транс-диаксиальном положении.[12] Экспериментальные данные показывают, что изомераза избирательно связывает переходное состояние кресла, хотя точный механизм катализ не известно. Считается, что это связывание стабилизирует переходное состояние за счет электростатических эффектов, что объясняет резкое увеличение скорости реакции в присутствии мутазы или при добавлении специально размещенного катиона в активном центре.[13]
Внутримолекулярное оксидоредукция

Изопентенил-дифосфат-дельта-изомераза тип I (также известный как изомераза IPP) встречается в холестерин синтез и, в частности, катализирует превращение изопентенил дифосфат (IPP) в диметилаллилдифосфат (DMAPP). В этой реакции изомеризации стабильная двойная углерод-углеродная связь перегруппирована сверху, создавая высокоэффективную электрофильный аллильный изомер. Изомераза IPP катализирует эту реакцию за счет стереоселективный антарафациальный транспозиция одиночного протона. В двойная связь протонируется по C4 с образованием третичного карбокатион промежуточный в C3. Соседний углерод C2 депротонируется с противоположной стороны, образуя двойную связь.[14] Фактически сдвигается двойная связь.
Роль изомеразы в заболеваниях человека
Изомераза играет важную роль в заболеваниях человека. Недостаток этого фермента может вызывать расстройства у человека.
Дефицит фосфогексозоизомеразы
Дефицит фосфогексозоизомеразы (PHI) также известен как дефицит фосфоглюкозоизомеразы или Дефицит глюкозо-6-фосфат изомеразы, и является наследственной недостаточностью ферментов. PHI - вторая по частоте эртоэнзиопатия в гликолиз Помимо дефицит пируваткиназы, и ассоциируется с несфероцитарной гемолитической анемией различной степени тяжести.[15][16] В основе этого заболевания лежит глюкозо-6-фосфатный белок. Этот белок можно найти в секрете некоторых раковых клеток.[17] PHI является результатом димерного фермента, который катализирует обратимое взаимное превращение фруктозо-6-фосфата и глюозо-6-фосфата.[15]
PHI - очень редкое заболевание, на сегодняшний день в литературе зарегистрировано только 50 случаев.[15]
Диагноз ставится на основании клинической картины в сочетании с биохимическими исследованиями, выявляющими дефицит GPI в эритроцитах (от 7 до 60% от нормы) и идентификацией мутации в гене GPI с помощью молекулярного анализа.[15]
Дефицит изомеразы фосфогексозы может привести к состоянию, называемому гемолитический синдром. Как и у человека, гемолитический синдром, который характеризуется уменьшением количества эритроцитов, более низким гематокритом, более низким гемоглобин Более высокое количество ретикулоцитов и концентрация билирубина в плазме, а также повышение соматических показателей печени и селезенки проявлялись исключительно у гомозиготных мутантов.[16]
Дефицит триозофосфат-изомеразы
Заболевание, называемое дефицитом триозофосфат-изомеразы (ДПИ), представляет собой тяжелое аутосомно-рецессивное наследственное мультисистемное заболевание. гликолевый метаболизм.[18] Он характеризуется гемолитической анемией и нейродегенерацией и вызывается анаэробной метаболической дисфункцией. Эта дисфункция является результатом миссенс-мутации, которая влияет на кодируемый белок TPI.[19] Наиболее распространенной мутацией является замена гена Glu104Asp, вызывающего наиболее тяжелые фенотип, и является причиной примерно 80% клинического дефицита ТПИ.[18]
Дефицит ТПИ встречается очень редко, в литературе описано менее 50 случаев.[20] Поскольку это аутосомно-рецессивное наследственное заболевание, дефицит TPI имеет 25% -ный риск рецидива в случае гетерозиготных родителей.[18][20] Это врожденное заболевание, которое чаще всего протекает с гемолитической анемией и проявляется желтухой.[18] Большинство пациентов с TPI по мутации Glu104Asp или гетерозиготными по нулевому аллелю TPI и Glu104Asp имеют ожидаемую продолжительность жизни от младенчества до раннего детства. Пациенты с TPI с другими мутациями обычно демонстрируют более продолжительную продолжительность жизни. На сегодняшний день известно только два случая людей с TPI, живущих в возрасте старше 6 лет. В этих случаях участвуют два брата из Венгрии, один из которых не развил неврологические симптомы до 12 лет, а старший брат не имеет неврологических симптомов и страдает только анемией.[21]
У лиц с TPI очевидные симптомы проявляются в возрасте от 6 до 24 месяцев. Эти симптомы включают: дистонию, тремор, дискинезию, признаки пирамидного тракта, кардиомиопатию и вовлечение спинномозговых мотонейронов.[18] У пациентов также наблюдаются частые бактериальные инфекции дыхательной системы.[18]
ТПИ обнаруживается по недостаточности ферментативной активности и накоплению в эритроцитах дигироксиацетонфосфата (DHAP), который является токсичным субстратом.[18][20] Это можно обнаружить при физическом осмотре и серии лабораторных работ. При обнаружении обычно наблюдаются миопатические изменения в мышцах и хроническая аксональная нейропатия в нервах.[18] Диагноз TPI может быть подтвержден с помощью молекулярной генетики.[18] Анализ ДНК ворсинок хориона или анализ эритроцитов плода может быть использован для выявления TPI при антенатальной диагностике.[18]
Уход для TPI не является конкретным, но варьируется в зависимости от случая. Из-за целого ряда симптомов, вызываемых TPI, может потребоваться группа специалистов для лечения одного человека. Эта команда специалистов будет состоять из педиатров, кардиологов, неврологов и других медицинских работников, которые могут разработать комплексный план действий.[22]
Поддерживающие меры, такие как переливание эритроцитов в случаях тяжелой анемии, также могут быть приняты для лечения TPI. В некоторых случаях удаление селезенки (спленэктомия) может улучшить анемию. Не существует лечения, которое предотвращало бы прогрессирующее неврологическое нарушение или другие негематологические клинические проявления заболевания.[23]
Промышленное применение
Безусловно, наиболее распространенное использование изомераз в промышленности - это сахар изготовление. Глюкозоизомераза (также известная как ксилозоизомераза ) катализирует превращение D-ксилоза и D-глюкоза к D-ксилулоза и D-фруктоза. Как и большинство сахарных изомераз, глюкозоизомераза катализирует взаимное превращение альдозы и кетоз.[24]
Превращение глюкозы во фруктозу - ключевой компонент кукурузный сироп с высоким содержанием фруктозы производство. Изомеризация более специфичен, чем старые химические методы производства фруктозы, что приводит к более высокому урожай фруктозы и нет побочные продукты.[24] Фруктоза, полученная в результате этой реакции изомеризации, чище, без остаточных запахов от загрязняющие вещества. Многие производители кондитерских изделий и газированных напитков предпочитают кукурузный сироп с высоким содержанием фруктозы из-за высокой подслащивающей способности фруктозы (вдвое больше сахарозы.[25]), его относительно невысокая стоимость и неспособность кристаллизоваться. Фруктоза также используется в качестве подсластителя. диабетики.[24] Основные проблемы использования глюкозоизомеразы связаны с ее инактивацией при более высоких температурах и требованием высокого pH (от 7,0 до 9,0) в реакционной среде. Умеренно высокие температуры, выше 70 ° C, увеличивают выход фруктозы по крайней мере наполовину на стадии изомеризации.[26] Фермент требует двухвалентный катион Такие как Co2+ и Mg2+ при пиковой активности производители оплачивают дополнительные расходы. Глюкозоизомераза также имеет гораздо более высокое сродство к ксилозе, чем к глюкозе, что требует тщательно контролируемой среды.[24]
Изомеризация ксилозы в ксилулозу имеет собственное коммерческое применение, поскольку биотопливо увеличилось. Эта реакция часто наблюдается в естественных условиях бактерии которые питаются гниющими растениями. Его наиболее распространенное промышленное использование - производство этиловый спирт, достигнутая ферментация из ксилулоза. Использование гемицеллюлоза как исходный материал очень распространен. Гемицеллюлоза содержит ксилан, который сам состоит из ксилоза в β (1,4) связи.[27] Использование изомеразы глюкозы очень эффективно превращает ксилозу в ксилулозу, на которую затем можно воздействовать путем ферментации. дрожжи. В целом, обширные исследования в области генной инженерии были вложены в оптимизацию изомеразы глюкозы и облегчение ее извлечения из промышленных приложений для повторного использования.
Глюкозоизомераза способна катализировать изомеризацию ряда других сахаров, включая D-рибоза, D-аллозе и я-арабиноза. Наиболее эффективными субстратами являются субстраты, аналогичные глюкозе и ксилозе, имеющие экваториальный гидроксил группы у третьего и четвертого атомов углерода.[28] Текущая модель механизма глюкозоизомеразы - это модель гидридный сдвиг на основе Рентгеновская кристаллография и исследования изотопного обмена.[24]
Мембранно-ассоциированные изомеразы
Некоторые изомеразы связываются с биологические мембраны в качестве белки периферической мембраны или закреплен через один трансмембранная спираль,[29] например изомеразы с тиоредоксиновый домен, и некоторые пролилизомеразы.
Рекомендации
- ^ Номенклатура ферментов, рекомендации Номенклатурного комитета Международного союза биохимиков 1978 г. по номенклатуре и классификации ферментов. Нью-Йорк: Academic Press. 1979 г. ISBN 9780323144605.
- ^ а б c Макнот А.Д. (1997). Сборник химической терминологии (2-е изд.). Оксфорд: Научные публикации Блэквелла. ISBN 978-0-9678550-9-7.
- ^ Whitesell JK, Fox MA (2004). Органическая химия (3-е изд.). Садбери, штат Массачусетс: Джонс и Бартлетт. С. 220–222. ISBN 978-0-7637-2197-8.
- ^ Корниш-Боуден А (2013-02-22). Основы кинетики ферментов (4-е изд.). Вайнхайм: Wiley-VCH. С. 238–241. ISBN 978-3-527-66548-8.
- ^ а б Фишер Л.М., Олбери В.Дж., Ноулз-младший (май 1986 г.). «Энергетика пролинрацемазы: эксперименты по изменению индикаторов с использованием [14C] пролина, которые измеряют скорость взаимного превращения двух форм свободного фермента». Биохимия. 25 (9): 2538–42. Дои:10.1021 / bi00357a038. PMID 3521737.
- ^ Бриттон Х. Г., Кларк Дж. Б. (ноябрь 1968 г.). «Механизм фосфоглюкомутазной реакции. Исследования фосфоглюкомутазы в мышцах кролика с помощью методов флюса». Биохимический журнал. 110 (2): 161–80. Дои:10.1042 / bj1100161. ЧВК 1187194. PMID 5726186.
- ^ Брюс П.Й. (2010). Основная органическая химия (2-е изд.). Река Аппер Сэдл, Нью-Джерси: Prentice Hall. ISBN 978-0-321-59695-6.
- ^ а б c d Уэбб ЕС (1992). Номенклатура ферментов 1992: рекомендации Номенклатурного комитета Международного союза биохимии и молекулярной биологии по номенклатуре и классификации ферментов (6-е изд.). Сан-Диего: Опубликовано для Международного союза биохимии и молекулярной биологии издательством Academic Press. ISBN 978-0-12-227164-9.
- ^ Список ферментов класса 5 - изомеразы (PDF). Номенклатурный комитет Международного союза биохимии и молекулярной биологии (NC-IUBMB). 2010 г.
- ^ Solomons JT, Zimmerly EM, Burns S, Krishnamurthy N, Swan MK, Krings S, Muirhead H, Chirgwin J, Davies C (сентябрь 2004 г.). «Кристаллическая структура мышиной фосфоглюкозоизомеразы с разрешением 1,6А и ее комплекс с глюкозо-6-фосфатом выявляют каталитический механизм раскрытия сахарного кольца». Журнал молекулярной биологии. 342 (3): 847–60. Дои:10.1016 / j.jmb.2004.07.085. PMID 15342241.
- ^ Терада Т., Мукаэ Х., Охаши К., Хосоми С., Мидзогути Т., Уэхара К. (апрель 1985 г.). «Характеристика фермента, который катализирует изомеризацию и эпимеризацию D-эритрозо-4-фосфата». Европейский журнал биохимии / FEBS. 148 (2): 345–51. Дои:10.1111 / j.1432-1033.1985.tb08845.x. PMID 3987693.
- ^ Ошибка T (2012). «Глава 10: Изомеразы». Введение в химию ферментов и коферментов (3-е изд.). Вайли. ISBN 978-1-118-34896-3.
- ^ Каст П., Гризостоми С., Чен И.А., Ли С., Кренгель Ю., Сюэ Ю., Хилверт Д. (ноябрь 2000 г.). «Стратегически расположенный катион имеет решающее значение для эффективного катализа хоризматмутазой». Журнал биологической химии. 275 (47): 36832–8. Дои:10.1074 / jbc.M006351200. PMID 10960481.
- ^ Чжэн В., Сунь Ф., Бартлам М., Ли Х, Ли Р., Рао З. (март 2007 г.). «Кристаллическая структура изопентенилдифосфатизомеразы человека при разрешении 1,7 A показывает ее каталитический механизм в биосинтезе изопреноидов». Журнал молекулярной биологии. 366 (5): 1447–58. Дои:10.1016 / j.jmb.2006.12.055. PMID 17250851.
- ^ а б c d Куглер В., Лакомек М. (март 2000 г.). «Дефицит глюкозо-6-фосфат изомеразы». Лучшие практики и исследования Байера. Клиническая гематология. 13 (1): 89–101. Дои:10.1053 / бэха.1999.0059. PMID 10916680.
- ^ а б Меркл С., Преч В. (1993). «Дефицит глюкозо-6-фосфат-изомеразы, связанный с несфероцитарной гемолитической анемией у мышей: животная модель заболевания человека» (PDF). Кровь. 81 (1): 206–13. PMID 8417789.
- ^ Krone W, Schneider G, Schulz D, Arnold H, Blume KG (1 января 1970 г.). «Выявление дефицита фосфогексозоизомеразы в культурах фибробластов человека». Humangenetik. 10 (3): 224–30. Дои:10.1007 / BF00295784. PMID 5475507.
- ^ а б c d е ж грамм час я j Орош П.Ф. «Дефицит триозофосфат-изомеразы». Orphanet. Получено 14 ноября 2013.
- ^ Селотто А.М., Фрэнк А.С., Сигл Дж.Л., Палладино М.Дж. (ноябрь 2006 г.). Дрозофила модель наследственной гликолитической энзимопатии, вызванной дефицитом триозофосфат изомеразы. Генетика. 174. С. 1237–46. Дои:10.1534 / генетика.106.063206. ЧВК 1667072. PMID 16980388.
- ^ а б c Олах Дж., Орос Ф., Кесеру Г.М., Ковари З., Ковач Дж., Холлан С., Овади Дж. (Апрель 2002 г.). «Дефицит триозофосфатизомеразы: нейродегенеративная болезнь неправильной укладки» (PDF). Сделки Биохимического Общества. 30 (2): 30–8. Дои:10.1042 / bst0300030. PMID 12023819. Архивировано из оригинал (PDF) на 2013-12-03. Получено 2013-11-27.
- ^ Холлан С., Фуджи Х., Хироно А., Хироно К., Карро Х., Мива С., Харшаньи В., Дьоди Е., Инселт-Ковач М. (ноябрь 1993 г.). «Наследственный дефицит триозофосфатизомеразы (ТПИ): два серьезно пострадавших брата, один с неврологическими симптомами, а другой без них». Генетика человека. 92 (5): 486–90. Дои:10.1007 / bf00216456. PMID 8244340.
- ^ «Дефицит триозофосфат-изомеразы». NORD. Получено 14 декабря 2013.
- ^ «Дефицит триозофосфат-изомеразы -ТПИ» (PDF). Получено 26 ноября 2013.
- ^ а б c d е Бхосале С.Х., Рао М.Б., Дешпанде В.В. (июнь 1996 г.). «Молекулярные и промышленные аспекты глюкозоизомеразы». Микробиологические обзоры. 60 (2): 280–300. ЧВК 239444. PMID 8801434.
- ^ Бейкер С (1976). «Чистые сиропы фруктозы». Биохимия процесса. 11: 20–25.
- ^ Антрим Р.Л., Колилла В., Шнайдер Б.Дж. (1979). «Производство глюкозоизомеразы сиропов с высоким содержанием фруктозы». Прикладная биохимия и биоинженерия. 2: 97–155.
- ^ Ван П.Я., Шопсис С., Шнайдер Х. (май 1980 г.). «Ферментация пентозы дрожжами». Сообщения о биохимических и биофизических исследованиях. 94 (1): 248–54. Дои:10.1016 / с0006-291x (80) 80213-0. PMID 6446306.
- ^ Чен В.П. (август – сентябрь 1980 г.). «Глюкозоизомераза». Биохимия процесса. 15: 36–41.
- ^ Надсемейства однопроходных трансмембранных лиаз в База данных мембран
