Ксилозоизомераза - Xylose isomerase
| ксилозоизомераза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Тетрамер D-ксилозоизомеразы из Streptomyces rubiginosus PDB 2glk.[1] Один мономер окрашен вторичной структурой, чтобы подчеркнуть архитектуру цилиндра TIM. | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 5.3.1.5 | ||||||||
| Количество CAS | 9023-82-9 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| БРЕНДА | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | AmiGO / QuickGO | ||||||||
| |||||||||
В энзимология, а ксилозоизомераза (EC 5.3.1.5 ) является фермент который катализирует взаимопревращениеD-ксилоза и D-ксилулоза. Этот фермент принадлежит к семейству изомеразы, особенно те внутримолекулярные оксидоредуктазы взаимопревращение альдозы и кетоз. Изомераза наблюдалась почти у ста видов бактерий. Ксилоза -изомеразы также обычно называют фруктозо-изомеразами из-за их способности взаимно превращать глюкозу и фруктозу. В систематическое название этого класса ферментов является D-ксилоза-альдоз-кетозо-изомераза. Другие широко используемые названия включают D-ксилозоизомеразу, D-ксилозокетоизомеразу и D-ксилозокетол-изомеразу.[2]
История
Деятельность D-ксилоза изомераза впервые был обнаружен Мицухаси и Лампеном в 1953 г. у бактерии Lactobacillus pentosus.[3] Искусственное производство через преобразованный Кишечная палочка также были успешными.[4] В 1957 году активность D-ксилозоизомеразы в превращении D-глюкозы в D-фруктозу была отмечена Куи и Маршаллом.[5] В настоящее время известно, что изомеразы обладают широкой субстратной специфичностью. Большинство пентоз и некоторые гексозы являются субстратами для D-ксилозоизомеразы. Некоторые примеры включают: D-рибозу, L-арабинозу, L-рамозу и D-аллозу.[6]
Превращение глюкозы во фруктозу с помощью ксилозоизомеразы было впервые запатентовано в 1960-х годах, однако этот процесс не был промышленно жизнеспособным, поскольку ферменты были суспендированы в растворе, и переработка фермента была проблематичной.[6] Неподвижная изомераза ксилозы, фиксируемая на твердой поверхности, была впервые разработана Таканаши в Японии.[6] Эти разработки были важны для развития промышленная ферментация процессы, используемые в производстве кукурузный сироп с высоким содержанием фруктозы.[7]:27[8]:808–813
Третичная структура была определена для нескольких изомераз ксилозы из микробов, начиная с середины 1980-х годов (Streptomyces olivochromogenes в 1988 г. Streptomyces violaceoniger в 1988 г. Streptomyces rubiginosus в 1984 г., Артробактер B3728 в 1986 г. Actinoplanes missouriensis в 1992 г. и Clostridium thermosulfurogenes в 1990 г.).[7]:366
Функция
Этот фермент участвует в превращения пентозы и глюкуроната и фруктоза и манноза метаболизм. По данным Международного общества редких сахаров, наиболее биологически доступными сахарами являются: глюкоза, галактоза, манноза, фруктоза, ксилоза, рибоза и L-арабиноза. Двадцать гексоз и девять пентоз, включая ксилулозу, считались «редкими сахарами». Следовательно, D-ксилозоизомераза используется для производства этих редких сахаров, которые имеют очень важное применение в биологии, несмотря на их низкое содержание.[9]
Характеристика
Ксилозоизомераза, которую можно выделить из красного китайского рисового вина, которое содержит бактерии Lactobacillus xylosus.[10] Эта бактерия была ошибочно классифицирована как L. plantarum, который обычно растет на сахаре L-арабиноза и редко выращивались на D-ксилозе. L. xylosus был признан отличным от его способности расти на D-ксилозе.[11]Ксилозоизомераза в L. xylosus имеет молекулярную массу около 183000 дальтон.[12]Оптимальный pH для роста составляет около 7,5 для L. lactis, однако штаммы, такие как L.brevis Фермент ксилоза предпочитает более щелочную среду. В L. lactis штамм стабилен в диапазоне pH от 6,5 до 11,0, а L. brevis Фермент, который менее устойчив к изменениям pH, проявляет активность в диапазоне pH 5,7–7,0.[12] Кей Ю. и Норитака Т. также провели тепловые испытания, и было обнаружено, что изомераза ксилозы является термостойкой примерно до 60 градусов по Цельсию.[12]
Активный сайт и механизм
Ксилозоизомераза имеет структуру, основанную на восьми альфа / бета-цилиндрах, которые создают активный центр, содержащий два двухвалентных иона магния. Ферменты ксилозоизомеразы проявляют ТИМ ствол складка с активным участком в центре ствола и тетрамерный четвертичная структура.[13] Структуры PDB доступны по ссылкам в информационном окне справа. Белок - это тетрамер где парные цилиндры почти соосны, которые образуют две полости, в которых оба двухвалентных металла связаны с одной из двух полостей. Металлы имеют октаэдрическую геометрию. Металлический участок 1 плотно связывает субстрат, в то время как второй участок металла связывает субстрат слабо. Оба имеют общий кислотный остаток глутаминовой кислоты 216 фермента, который связывает два катиона. Две основные аминокислоты окружают отрицательно заряженный лиганды чтобы нейтрализовать их. Вторая полость обращена к металлической полости, и обе полости имеют один и тот же путь доступа. Вторая полость является гидрофобной по своей природе и содержит важный остаток гистидина, который активируется аспартат остаток, который водородная связь к нему. Этот остаток гистидина важен для изомеризация глюкозы.[14]
При изомеризации глюкозы гистидин 53 используется, чтобы катализировать перенос протона от O1 к O5; Схема механизма открывания кольца представлена ниже. Первый металл, упомянутый ранее, координаты к O3 и O4, и используется для стыковки подложки.[14]

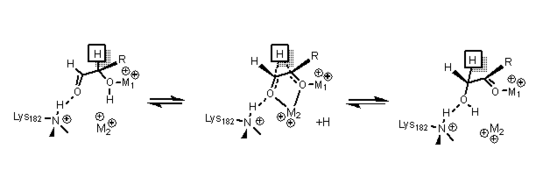
При изомеризации ксилозы кристаллические данные показали, что сахар ксилозы связывается с ферментом в открытой цепи. конформация. Металл 1 связывается с O2 и O4, и после связывания металл 2 связывается с O1 и O2 в переходном состоянии, и эти взаимодействия вместе с остатком лизина помогают катализировать гидридный сдвиг необходим для изомеризации. Переходное состояние состоит из высокой энергии ион карбония который стабилизируется посредством всех взаимодействий металла с сахарным субстратом.[14]
Применение в промышленности
Наиболее широко этот фермент применяется для превращения глюкозы во фруктозу с образованием кукурузный сироп с высоким содержанием фруктозы (HFCS).[7]:27 Есть три основных этапа производства HFCS из крахмала:[8]:808–813
- ферментативное разложение крахмала с использованием α-амилаза. Также известен как сжижение.
- дальнейшая деградация с использованием глюкоамилаза и фермент разветвления.
- Производство фруктозы с помощью ксилозоизомеразы
Процесс осуществляется в биореакторы при 60–65 ° С.[7]:27 Ферменты становятся инактивированный при таких высоких температурах, как эта, и одним из направлений исследований была разработка более термостабильных версий ксилозоизомеразы и других ферментов в процессе.[7]:27 Ферменты обычно обездвижен увеличить пропускную способность; Еще одним направлением исследований было улучшение способов сделать это.[7]:358–360[15]
Ксилозоизомераза - один из ферментов, используемых бактериями в природе для использования целлюлоза в качестве продуктов питания, а также в целях промышленных и академических исследований, разрабатываются версии ксилозоизомеразы, которые могут быть полезны в производстве биотопливо.[7]:358[16]
Как диетическая добавка
Продукты, содержащие ксилозо-изомеразу, продаются как без рецепта пищевые добавки сражаться мальабсорбция фруктозы, в основном в Европе и под торговыми марками, включая Fructaid, Fructease и Фруктозин. Помимо общих опасений по поводу эффективности безрецептурных ферментов,[17] В настоящее время существует очень ограниченное количество исследований, касающихся ксилозо-изомеразы в качестве пищевой добавки, с единственным научным исследованием, показывающим положительное влияние на тошноту и боль в животе, связанную с мальабсорбцией, но ни одного на вздутие живота.[18]
Рекомендации
- ^ Кац, А. К .; Li, X .; Carrell, H.L .; Hanson, B.L .; Langan, P .; Coates, L .; Schoenborn, B.P .; Glusker, J. P .; Буник, Г. Дж. (2006). «Определение местонахождения атомов водорода в активном центре в D-ксилозоизомеразе: времяпролетная нейтронная дифракция». Труды Национальной академии наук. 103 (22): 8342–8347. Bibcode:2006PNAS..103.8342K. Дои:10.1073 / pnas.0602598103. ЧВК 1482496. PMID 16707576.
- ^ Му, Ванмэн; Hassanin, Hinawi A.M .; Чжоу, Леон; Цзян, Бо (2018). «Химия редких сахаров и биопереработка». Журнал сельскохозяйственной и пищевой химии. 66 (51): 13343–13345. Дои:10.1021 / acs.jafc.8b06293. PMID 30543101.
- ^ Mitsuhashi, S .; Лампен, Дж. (1953). «Превращение D-ксилозы в D-ксилулозу в экстрактах Lactobacillus pentosus» (PDF). Журнал биологической химии. 204 (2): 1011–8. PMID 13117877.
- ^ Шомбург, Дитмар (2001). Справочник по ферментам. Нью-Йорк: Спрингер. С. 259–260. ISBN 9783540410089.
- ^ Маршалл, Ричард; Куи, Эрл (1957). «Ферментативное превращение D-глюкозы в D-фруктозу». Наука. 125 (3249): 648–9. Bibcode:1957Sci ... 125..648M. Дои:10.1126 / science.125.3249.648. PMID 13421660.
- ^ а б c Джокела, Джоуни; Пастинен, Осси (2002). «Изомеризация пентозных и гексозных сахаров в ферментном реакторе, заполненном сшитыми кристаллами ксилозоизомеразы». Ферментные и микробные технологии. 31 (1–2): 67–76. Дои:10.1016 / s0141-0229 (02) 00074-1.
- ^ а б c d е ж грамм Вонг, Доминик В. С. (1995). Структура и механизм пищевых ферментов. Бостон, Массачусетс: Springer США. ISBN 978-1-4757-2349-6.
- ^ а б Хоббс, Ларри (2009). «21 - Подсластители из крахмала: производство, свойства и применение». В BeMiller, James N .; Уистлер, Рой Л. (ред.). Крахмал: химия и технология (3-е изд.). Лондон: Academic Press / Elsevier. стр.797 –832. ISBN 978-0-12-746275-2.
- ^ Бееренс, К. (2012). «Ферменты для биокаталитического производства редких сахаров». J. Ind. Microbiol. Биотехнология. 39 (6): 823–834. Дои:10.1007 / s10295-012-1089-х. PMID 22350065. S2CID 14877957.
- ^ Китахара, К. (1966). «Исследования молочнокислых бактерий». Нюсанкин Но Кенкю: 67~69.
- ^ Buchanan, R.E .; Гиббонс, Н. (1974). Руководство Берджи по определению бактериологии (8-е изд.). Балтимор: Уильямс и Уилкинс Ко. Стр. 584.
- ^ а б c Яманака, Кей; Такахара, Норитака (1977). «Очистка и свойства D-ксилозоизомеразы из Lactobacillus xylosus». Agric. Биол. Chem. 41 (10): 1909–1915. Дои:10.1271 / bbb1961.41.1909.
- ^ Устаревшие услуги
- ^ а б c Удар, Дэвид; Коллиер, Чарльз; Голдберг, Джонатан; Смарт, Оливер (1992). «Структура и механизм D-ксилозоизомеразы». Фарадеевские дискуссии. 93 (93): 67–73. Bibcode:1992FaDi ... 93 ... 67B. Дои:10.1039 / fd9929300067. PMID 1290940.
- ^ Волкин, Д; Клибанов, А. (1988). «Механизм термоинактивации иммобилизованной глюкозоизомеразы». Биотехнология Биоенг. 33 (9): 1104–1111. Дои:10.1002 / бит. 260330905. PMID 18588027. S2CID 39076432.
- ^ Марис, Ван; Антониус; и другие. (2007). «Развитие эффективной ферментации ксилозы в Saccharomyces Cerevisiae: ксилозоизомераза как ключевой компонент». Adv. Biochem. Engin / Biotechnol. Достижения в области биохимической инженерии / биотехнологии. 108: 179–204. Дои:10.1007/10_2007_057. ISBN 978-3-540-73650-9. PMID 17846724.
- ^ Варайил, Джитинрадж Эдакканамбет; Bauer, Brent A .; Больно, Райан Т. (2014). «Ферментные добавки, отпускаемые без рецепта: что должен знать врач». Краткий обзор для врачей. 89 (9): 1307. Дои:10.1111 / apt.12057. PMID 23002720. S2CID 6047336.
- ^ Komericki, P .; Аккилыч-Матерна, М .; Стримитцер, Т .; Weyermair, K .; Hammer, H.F .; Аберер, В. (2012). «Пероральная ксилозоизомераза снижает выведение водорода из дыхания и улучшает желудочно-кишечные симптомы при мальабсорбции фруктозы - двойное слепое плацебо-контролируемое исследование». Пищевая фармакология и терапия. 36 (10): 980. Дои:10.1111 / apt.12057. PMID 23002720. S2CID 6047336.
дальнейшее чтение
- Хохстер Р. М., Уотсон Р. В. (1954). «Ферментативная изомеризация D-ксилозы в D-ксилулозу». Arch. Biochem. Биофизы. 48 (1): 120–9. Дои:10.1016/0003-9861(54)90313-6. PMID 13125579.
- Slein MW (1955). «Ксилозоизомераза из Pasteurella pestis, штамм А-1122». Варенье. Chem. Soc. 77 (6): 1663–1667. Дои:10.1021 / ja01611a074.
- Яманака К. (1968). «Очистка, кристаллизация и свойства изомеразы D-ксилозы из Lactobacillus brevis». Биохим. Биофиз. Acta. 151 (3): 670–80. Дои:10.1016/0005-2744(68)90015-6. PMID 5646045.
