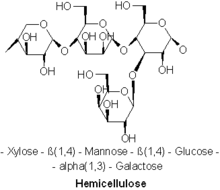
Гемицеллюлоза - Hemicellulose
А гемицеллюлоза (также известен как полиоза) является одним из ряда гетерополимер (матричные полисахариды), такие как арабиноксиланы, присутствуют вместе с целлюлоза почти во всех наземное растение клеточные стенки.[1] В то время как целлюлоза кристаллическая, прочная и устойчивая к гидролиз гемицеллюлозы имеют беспорядочную аморфную структуру с небольшой прочностью. Они легко гидролизуются разбавленными кислота или же основание а также множество гемицеллюлаза ферменты.
Сочинение
Известны самые разные виды гемицеллюлоз. Важные примеры включают ксилан, глюкуроноксилан, арабиноксилан, глюкоманнан, и ксилоглюкан.
Гемицеллюлозы бывают полисахариды часто ассоциируется с целлюлозой, но целлюлоза и гемицеллюлоза имеют разные составы и структуры. Разнообразные сахара включают гемицеллюлозу, тогда как целлюлоза получается исключительно из глюкозы. Например, помимо глюкозы, сахарные мономеры в гемицеллюлозах могут включать пятиуглеродные сахара. ксилоза и арабиноза, шестиуглеродные сахара манноза и галактоза, и шестиуглеродный дезокси сахар рамноза. Гемицеллюлозы содержат большую часть D-пентоза сахара, а иногда и небольшое количество L-сахаров. Ксилоза в большинстве случаев мономер сахара присутствует в наибольшем количестве, хотя в хвойных породах самым распространенным сахаром может быть манноза. В гемицеллюлозе можно найти не только обычные сахара, но и их подкисленную форму, например глюкуроновая кислота и галактуроновая кислота может присутствовать.[2][3]
Структурное сравнение с целлюлозой
В отличие от целлюлоза гемицеллюлозы состоят из более коротких цепочек - 500–3 000 сахарных единиц. Напротив, каждый полимер целлюлозы составляет от 7 000 до 15 000 молекул глюкозы.[4] Кроме того, гемицеллюлоза может быть разветвленной. полимеры, а целлюлоза неразветвленная. Гемицеллюлозы встраиваются в клеточные стенки растений, иногда в цепочки, которые образуют 'земля '- они связывают с пектин к целлюлозе с образованием сети из поперечно-сшитых волокон.

Основываясь на структурных различиях, таких как звенья основной цепи и боковые группы, а также других факторов, таких как численность и распределение в растениях, гемицеллюлозу можно разделить на четыре группы следующим образом:[3] 1) Ксиланы, 2) Маннаны; 3) Β-глюканы со смешанными связями; 4) Ксилоглюканы
Ксиланы
Ксиланы обычно состоят из основной цепи β- (1 → 4) -связанных ксилоза остатки. И его можно разделить на гомоксиланы и гетероксиланы. Homoxylans имеет основу из остатков D-ксилопиранозы, связанных β (1 → 3) или смешанными β (1 → 3, 1 → 4) -гликозидными связями. Гомоксиланы в основном несут структурные функции. Гетероксиланы, такие как глюкуроноксиланы, глюкуроноарабиноксиланы и сложные гетероксиланы имеют основу из D-ксилопиранозы и короткие углеводные ответвления. Например, глюкуроноксилан имеет замещение α- (1 → 2) -связанными глюкуронозильными и 4-O-метилглюкуронозильными остатками. И арабиноксиланы и глюкуроноарабиноксиланы содержат арабиноза остатки прикреплены к позвоночнику[5]
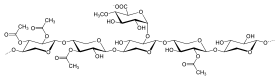
Маннаны
Гемицеллюлозу маннанового типа можно разделить на два типа в зависимости от различия их основных цепей: галактоманнаны и глюкоманнаны. Галактоманнаны имеют только β- (1 → 4) связанные остатки D-маннопиранозы в линейных цепях. Глюкоманнаны состоят как из β- (1 → 4) связанных остатков D-маннопиранозы, так и из остатков β- (1 → 4) D-глюкопиранозы в основных цепях. Что касается боковых цепей, остатки D-галактопиранозы имеют тенденцию быть 6-связанными с обоими типами в виде одинарных боковых цепей с различным количеством.[1]
Β-глюканы со смешанными связями
Подтверждение смешанного сцепления глюкан цепочки обычно содержат блоки β- (1 → 4) D-глюкопиранозы, разделенные одной β- (1 → 3) D-глюкопиранозой. Население β- (1 → 4) и β- (1 → 3) составляет около 70% и 30%. Эти глюканы в основном состоят из целлотриозида (C18ЧАС32О16) и целлотраозил (C24ЧАС42О21) сегменты в случайном порядке. Некоторые исследования показывают молярное соотношение целлотриозил / целлотраозил для овса (2,1–2,4), ячменя (2,8–3,3) и пшеницы (4,2–4,5).[1][4].

Ксилоглюканы
Ксилоглюканы имеют основу, аналогичную целлюлозе, с остатками α-D-ксилопиранозы в положении 6. Чтобы лучше описать различные боковые цепи, для каждого типа боковой цепи используется обозначение однобуквенного кода. G - неразветвленный остаток Glc; Х - α-d-Ксил- (1 → 6) -Glc. L - β-Гал, S - α-1-Араф, F- α-1-Фук. Это самые распространенные боковые цепи.[4]
Два наиболее распространенных типа ксилоглюканов в стенках растительных клеток обозначены как XXXG и XXGG.[1]
Биосинтез
Гемицеллюлозы синтезируются из нуклеотидов сахара в клетках. аппарат Гольджи.[7] Две модели объясняют их синтез: 1) «2-компонентная модель», в которой модификация происходит в двух трансмембранных белках, и 2) «1-компонентная модель», где модификация происходит только в одном трансмембранном белке. После синтеза гемицеллюлозы транспортируются к плазматической мембране через везикулы Гольджи.
Каждый вид гемицеллюлозы биосинтезируется специализированными ферментами.[7][8]
Маннан Остовы цепи синтезируются семейством целлюлозосинтазоподобных белков семейства A (CSLA) и, возможно, ферментами семейства D целлюлозосинтазоподобных белков (CSLD).[7][8] Маннан-синтаза, особый фермент CSLA, отвечает за добавление манноза единиц к магистрали.[7][8] В галактоза боковые цепи некоторых маннанов добавляются галактоманнан-галактозилтрансферазой.[7][8] Ацетилирование из маннаны опосредуется маннан-O-ацетилтрансферазой, однако этот фермент окончательно не идентифицирован.[8]
Ксилоглюкан синтез основной цепи опосредуется целлюлозосинтазоподобными белками семейства C (CSLC), в частности глюкансинтаза, что добавляет глюкоза единиц в цепочку.[7][8] Магистральный синтез ксилоглюкан также каким-то образом опосредуется ксилозилтрансфераза, но этот механизм не связан с его функцией трансферазы и остается неясным.[8] Ксилозилтрансфераза в своей трансферазной функции, однако, используется для добавления ксилоза к боковой цепи.[7][8] Другие ферменты, используемые для синтеза боковой цепи ксилоглюкан включают галактозилтрансфераза (который отвечает за добавление галактоза и из которых используются две разные формы), фукозилтрансфераза (который отвечает за добавление фукоза ), и ацетилтрансфераза (который отвечает за ацетилирование ).[7][8]
Ксилан синтез основной цепи, в отличие от других гемицеллюлоз, не опосредуется какими-либо белками, подобными синтазе целлюлозы.[8] Вместо этого ксилан-синтаза отвечает за синтез основной цепи, облегчая добавление ксилоза.[8] Идентифицировано несколько генов ксилансинтаз.[8] Несколько других ферментов используются для добавления и модификации звеньев боковой цепи ксилан, включая глюкуронозилтрансфераза (что добавляет глюкуроновая кислота единицы), ксилозилтрансфераза (что добавляет дополнительные ксилоза единицы), арабинозилтрансфераза (что добавляет арабиноза ), метилтрансфераза (ответственный за метилирование ), и ацетилтрансфераза (ответственный за ацетилирование ).[8]При условии глюкан со смешанными связями представляет собой неразветвленный гомополимер глюкоза, нет синтеза боковой цепи, только добавление глюкоза к позвоночнику двумя связями, β1-3 и β1-4.[8] Синтез каркаса опосредуется ферментами семейств белков F и H, подобных синтазе целлюлозы (CSLF и CSLH), в частности глюкансинтаза.[7][8] Несколько форм глюкансинтаза из CSLF и CSLH.[7][8] Все они отвечают за добавление глюкоза к остову, и все они способны продуцировать как связи β1-3, так и β1-4, однако неизвестно, насколько каждый конкретный фермент вносит вклад в распределение связей β1-3 и β1-4.[7][8]
Приложения
в процесс сульфитной целлюлозы гемицеллюлоза в значительной степени гидролизуется кислым щелоком варки целлюлозы, попадая в коричневый щелок, где ферментируемые гексоза сахара (около 2%) можно использовать для производства этиловый спирт. Этот процесс в основном применялся для коричневых щелоков с сульфитом кальция.
Арабиногалактаны можно использовать как эмульгаторы, стабилизаторы и связующие в соответствии с Федеральный закон о пищевых продуктах, лекарствах и косметических средствах. Арабиногалактаны также можно использовать в качестве связующего для множества вещей, таких как подсластители.[9]
Пленки на основе ксилана обладают низкой проницаемостью для кислорода и поэтому представляют потенциальный интерес в качестве упаковки для чувствительных к кислороду продуктов.[10]
Агар используется для приготовления желе и пудингов. Это также питательная среда с другими питательными веществами для микроорганизмы.[11]

Курдлан можно использовать в качестве заменителя жира для производства диетического питания, при этом он имеет вкус и ощущение во рту настоящих жиросодержащих продуктов.[12]
β-глюканы играют важную роль в добавках к пище, в то время как β-глюканы также перспективны для решения проблем, связанных со здоровьем, особенно при иммунных реакциях и лечении рака.[13]
Ксантан, с другими полисахариды может образовывать гели с высоким содержанием раствора вязкость который может использоваться в нефтяной промышленности для загущения бурового раствора. В пищевой промышленности ксантан используется в таких продуктах, как заправки и соусы.[14]
Альгинат играет важную роль в развитии противомикробный текстиль из-за его характеристик экологичности и высокого уровня индустриализации как экологически безопасного биополимер.[15]
Естественные функции

Гемицеллюлоза в растительных клетках
- Вместе с целлюлоза в стенках растительных клеток гемицеллюлоза способствует укреплению клеточной стенки
- Гемицеллюлоза также полисахарид соединение в стенках растительных клеток, подобное целлюлозе[5]
- Соединение гемицеллюлозы взаимодействует с целлюлоза путем сшивания целлюлоза микрофибриллы
- Гемицеллюлоза будет искать пустоты в клеточной стенке во время ее образования и обеспечивать поддержку вокруг целлюлозы. фибриллы[5]
- Этот процесс осуществляется гемицеллюлозой, чтобы придать клеточной стенке максимально возможную прочность, которую она может обеспечить.
- Гемицеллюлоза преобладает в середине ламели растительной клетки, в отличие от целлюлоза который в основном находится во вторичных слоях[16]
- Это позволяет гемицеллюлозе обеспечивать промежуточную поддержку целлюлозы на внешних слоях растительной клетки.
- Гемицеллюлоза будет искать пустоты в клеточной стенке во время ее образования и обеспечивать поддержку вокруг целлюлозы. фибриллы[5]
- В немногих клеточных стенках гемицеллюлоза также будет взаимодействовать с лигнин для обеспечения структурной тканевой поддержки большего количества сосудистых растений[2]
Добыча
Есть много способов получить гемицеллюлозу; все они основаны на методах экстракции из твердых или мягких пород деревьев, измельченных на более мелкие образцы. В древесине лиственных пород основным экстрактом гемицеллюлозы является глюкуронокслян (ацетилированные ксиланы), тогда как галактоглюкоманнан содержится в древесине хвойных пород.[17][18] Перед экстракцией древесину обычно необходимо измельчить в древесную щепу различных размеров в зависимости от используемого реактора. После этого применяется процесс экстракции горячей водой, также известный как автогидролиз или гидротермальная обработка, с добавлением кислот и оснований для значительного изменения размера и свойств выхода.[17][18] Основное преимущество экстракции горячей водой заключается в том, что он предлагает метод, при котором единственным необходимым химическим веществом является вода, что делает его экологически безопасным и дешевым.
Цель обработки горячей водой - добиться максимального удаления гемилекулозы из древесины. Это осуществляется путем гидролиза гемицеллюлозы с получением олигомеров меньшего размера и моносахаридной ксилозы. Ксилоза при обезвоживании превращается в фурфурол.[19] Когда целью является ксилоза и фуфурол, добавляются кислотные катализаторы, такие как муравьиная кислота, чтобы увеличить переход полисахарида в моносахарид. Также было показано, что этот катализатор также использует эффект растворителя, чтобы способствовать реакции.[19]
Один из методов предварительной обработки - пропитать древесину разбавленными кислотами (с концентрацией около 4%). Это превращает гидролозную гемицеллюлозу в моносахараиды. Когда предварительная обработка выполняется основаниями (например, гидроксидом натрия или калия), это разрушает структуру собственного лигнина.[18] Это изменяет структуру с кристаллической на аморфную. Другой метод предварительной обработки - это предварительная гидротермическая обработка. Это дает такие преимущества, как отсутствие необходимости в токсичных или коррозионных растворителях, в специальных реакторах и в дополнительных затратах на утилизацию опасных химикатов.[17]
Процесс экстракции горячей водой осуществляется в реакторах периодического действия, полунепрерывных реакторах или суспензионных реакторах непрерывного действия. Для реакторов периодического и полунепрерывного действия можно использовать образцы древесины в таких условиях, как щепа или гранулы, тогда как суспензионный реактор должен иметь частицы размером от 200 до 300 мкм.[18] По мере уменьшения размера частиц уменьшается и выход продукции.[20] Это связано с увеличением целлюлозы.
Процесс горячей воды работает в диапазоне температур от 160 до 240 градусов по Цельсию, чтобы сохранить жидкую фразу. Это делается при температуре выше нормальной температуры кипения воды для увеличения солюбилизации гемицеллюлозы и деполимеризации полисахаридов.[19] Этот процесс может занять от нескольких минут до нескольких часов в зависимости от температуры и pH системы.[18] Более высокие температуры в сочетании с более длительным временем экстракции приводят к более высоким выходам. Максимальный выход достигается при pH 3,5.[17] Если ниже, выход экстракции экспоненциально уменьшается. Для регулирования pH обычно добавляют бикарбонаты натрия.[17] Биокарбонаты натрия ингибируют автодиолиз ацетильных групп, а также ингибируют гликозные связи. В зависимости от температуры и времени гемицеллюлоза может быть далее преобразована в олигомеры, мономеры и лигнин.[17]
Смотрите также
Рекомендации
- ^ а б c d Шеллер Х.В., Ульвсков П.Гемицеллюлозы. // Annu Rev Plant Biol. 2010; 61: 263-89. DOI: 10.1146 / annurev-arplant-042809-112315.
- ^ а б Эбрингерова, Анна; Громадкова, Зденка; Хайнце, Томас (2005), Хайнце, Томас (редактор), «Гемицеллюлоза», Полисахариды I: структура, характеристика и использование, Достижения в науке о полимерах, Springer, стр. 1–67, Дои:10.1007 / b136816, ISBN 978-3-540-31583-4
- ^ а б Полисахариды I: структура, характеристика и применение. Хайнце, Томас, 1958-. Берлин: Springer. 2005 г. ISBN 978-3-540-31583-4. OCLC 262681325.CS1 maint: другие (связь)
- ^ а б c Гибсон LJ (2013). «Иерархическая структура и механика растительного сырья». Журнал интерфейса Королевского общества. 9 (76): 2749–2766. Дои:10.1098 / rsif.2012.0341. ЧВК 3479918. PMID 22874093.
- ^ а б c Шеллер, Хенрик Вайб; Ульвсков, Петр (02.06.2010). «Гемицеллюлозы». Ежегодный обзор биологии растений. 61 (1): 263–289. Дои:10.1146 / annurev-arplant-042809-112315. ISSN 1543-5008. PMID 20192742.
- ^ Nimz, Horst H .; Шмитт, Уве; Шваб, Эккарт; Виттманн, Отто; Вольф, Франц (2000-06-15), "Вуд", в Wiley-VCH Verlag GmbH & Co. KGaA (ред.), Энциклопедия промышленной химии Ульмана, Wiley-VCH Verlag GmbH & Co. KGaA, стр. A28_305, Дои:10.1002 / 14356007.a28_305, ISBN 978-3-527-30673-2
- ^ а б c d е ж грамм час я j k Чжу, Сяоюй; Синь, Сяорань; Гу, Инь (2019), Коэн, Ефрем; Мерцендорфер, Ханс (ред.), "Синтез целлюлозы и гемицеллюлозы и их регуляция в растительных клетках", Внеклеточные биополимерные матрицы на основе сахара, Издательство Springer International Publishing, 12, стр. 303–353, Дои:10.1007/978-3-030-12919-4_7, ISBN 978-3-030-12918-7
- ^ а б c d е ж грамм час я j k л м п о п q Поли, Маркус; Гилле, Саша; Лю, Лифэн; Мансури, Насим; де Соуза, Амансио; Шультинк, Алекс; Сюн, Гуанян (2013). «Биосинтез гемицеллюлозы». Planta. 238 (4): 627–642. Дои:10.1007 / s00425-013-1921-1. ISSN 0032-0935. PMID 23801299. S2CID 17501948.
- ^ УИСТЛЕР, Р. Л. (1993). ГЕМИЦЕЛЛЮЛОЗЫ. In Industrial Gums (стр. 295–308). Эльзевир. https://doi.org/10.1016/b978-0-08-092654-4.50015-2
- ^ Грёндаль, М., и Гатенхольм, П. (2007). Пленки кислородного барьера на основе ксиланов, выделенных из биомассы. В серии симпозиумов ACS (стр. 137–152). Американское химическое общество. https://doi.org/10.1021/bk-2007-0954.ch009
- ^ Спиридон И. и Попа В. И. (2008). Гемицеллюлозы: основные источники, свойства и применение. В «Мономеры, полимеры и композиты из возобновляемых источников» (стр. 289–304). Эльзевир. https://doi.org/10.1016/b978-0-08-045316-3.00013-2
- ^ Спиридон И. и Попа В. И. (2008). Гемицеллюлозы: основные источники, свойства и применение. В «Мономеры, полимеры и композиты из возобновляемых ресурсов» (стр. 289–304). Эльзевир. https://doi.org/10.1016/b978-0-08-045316-3.00013-2
- ^ Ветвицкая, В., Ваннуччи, Л., Сима, П., и Рихтер, Дж. (2019). Бета-глюкан: добавка или лекарство? От лаборатории к клиническим испытаниям. Молекулы, 24 (7), 1251. https://doi.org/10.3390/molecules24071251
- ^ Наваррете, Р. К., Хаймс, Р. Э. и Сеулт, Дж. М. (2000). Применение ксантановой камеди для контроля потери жидкости и связанного с ней повреждения пластами. Конференция SPE по добыче нефти и газа Пермского бассейна. Конференция SPE по добыче нефти и газа Пермского бассейна. https://doi.org/10.2118/59535-ms
- ^ Ли, Дж., Хе, Дж., И Хуанг, Ю. (2017). Роль альгината в антибактериальной отделке текстиля. Международный журнал биологических макромолекул, 94, 466–473. https://doi.org/10.1016/j.ijbiomac.2016.10.054
- ^ «Гемицеллюлоза - обзор | Темы ScienceDirect». www.sciencedirect.com. Получено 2020-04-30.
- ^ а б c d е ж Галлина, Джанлука; Кабеса, Альваро; Гренман, Хенрик; Биази, Пьердоменико; Гарсия-Серна, Хуан; Салми, Тапио (2018-03-01). «Экстракция гемицеллюлозы путем предварительной обработки горячей водой под давлением при 160ºC для 10 различных пород древесины: выход и молекулярная масса». Журнал сверхкритических жидкостей. Фракционирование биомассы субкритической и сверхкритической водой. 133: 716–725. Дои:10.1016 / j.supflu.2017.10.001. ISSN 0896-8446.
- ^ а б c d е Ли З, Цинь М., Сюй Ц. и Чен Х (2013). «Извлечение гемицеллюлозы горячей водой из опилок осины разной крупности :: Биоресурсы». bioresources.cnr.ncsu.edu. Получено 2020-04-24.CS1 maint: несколько имен: список авторов (связь)
- ^ а б c Тунч, М. Сефик; ван Хейнинген, Адриан Р. П. (17 сентября 2008 г.). «Экстракция гемицеллюлозы из смешанной южной твердой древесины с водой при 150 ° C: влияние времени». Исследования в области промышленной и инженерной химии. 47 (18): 7031–7037. Дои:10.1021 / ie8007105. ISSN 0888-5885.
- ^ Айрилмис Н., Квон Дж., Хан Т. (октябрь 2017 г.). «Влияние размера древесной стружки на извлечение гемицеллюлозы и технологические свойства древесноволокнистых плит». Турецкий журнал сельского хозяйства и лесоводства. 41: 331–337. Дои:10.3906 / tar-1704-63.CS1 maint: несколько имен: список авторов (связь)
внешняя ссылка
- Структура и свойства гемицеллюлозы / Урок химии древесины Дэвида Ванга
