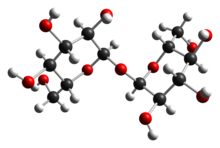
Трегалоза - Trehalose
 | |
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК (2р,3S,4S,5р,6р) -2- (Гидроксиметил) -6 - [(2р,3р,4S,5S,6р) -3,4,5-тригидрокси-6- (гидроксиметил) оксан-2-ил] оксиоксан-3,4,5-триол | |
| Другие имена α, α-трегалоза; α-D-глюкопиранозил- (1 → 1) -α-D-глюкопиранозид | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.002.490 |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C12ЧАС22О11 (ангидрид) | |
| Молярная масса | 342,296 г / моль (безводный) 378,33 г / моль (дигидрат) |
| Внешность | белый ромбический кристаллы |
| Плотность | 1,58 г / см3 при 24 ° C |
| Температура плавления | 203 ° С (397 ° F, 476 К) (безводный) 97 ° C (дигидрат) |
| 68,9 г на 100 г при 20 ° C[1] | |
| Растворимость | растворим в этиловый спирт, не растворим в диэтиловый эфир и бензол[2] |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Трегалоза (от турецкого trehala - сахар, полученный из коконов насекомых + -оза)[3] это сахар состоящий из двух молекул глюкоза. Он также известен как микоза или же тремалоз. Некоторые бактерии, грибы, растения и беспозвоночные животные синтезируют его как источник энергии, чтобы выжить при замораживании и недостатке воды.
Когда-то извлечение трегалозы было трудным и дорогостоящим процессом, но примерно в 2000 году компания Hayashibara (Окаяма, Япония) открыла недорогую технологию извлечения из крахмала.[4][5] Трегалоза обладает высокой способностью удерживать воду и используется в пищевых продуктах, косметике и в качестве лекарственного средства. Разработанная в 2017 году процедура с использованием трегалозы позволяет хранить сперму при комнатной температуре.[6]
Структура
Трегалоза - это дисахарид, образованный 1,1-гликозидный связь между двумя единицами α-глюкозы. Два других изомера в природе не встречаются.[7] Встречается в природе как дисахарид а также в качестве мономера в некоторых полимерах.[7]
Синтез
По крайней мере, три биологических пути поддерживают трегалозу биосинтез.[7] Промышленный процесс может получить трегалозу из кукурузный крахмал.[8]
Характеристики
Химическая
Трегалоза - это невосстанавливающий сахар образованный из двух единиц глюкозы, соединенных альфа-связью 1–1, что дало ему название α-D-глюкопиранозил- (1 → 1) -α-D-глюкопиранозид. Склеивание делает трегалозу очень устойчивой к кислоте. гидролиз, поэтому он стабилен в растворе при высоких температурах, даже в кислых условиях. Связывание удерживает невосстанавливающие сахара в форме замкнутого кольца, так что альдегид или же кетон конечные группы не привязываются к лизин или же аргинин остатки белков (процесс, называемый гликирование ). Трегалоза менее растворима, чем сахароза, кроме высоких температур (> 80 ° C). Трегалоза образует ромбовидный кристалл в виде дигидрата и имеет 90% калорийности сахарозы в этой форме. Безводные формы трегалозы легко восстанавливают влагу, образуя дигидрат. Безводный формы трегалозы могут проявлять интересные физические свойства при термообработке.
Водные растворы трегалозы проявляют тенденцию к кластеризации в зависимости от концентрации. Благодаря их способности формировать водородные связи, они самоассоцируются в воде, образуя кластеры различного размера. Полноатомное моделирование молекулярной динамики показало, что концентрация 1,5–2,2 моль позволяет молекулярным кластерам трегалозы образовываться. просачиваться и образуют большие сплошные агрегаты.[9]
Трегалоза напрямую взаимодействует с нуклеиновыми кислотами, способствует плавлению двухцепочечной ДНК и стабилизирует одноцепочечные нуклеиновые кислоты.[10]
Биологические
Организмы, начиная от бактерий, дрожжей, грибов, насекомых, беспозвоночных, а также низших и высших растений, имеют ферменты, которые могут вырабатывать трегалозу.[7]В природе трегалозу можно найти в растения, и микроорганизмы. У животных трегалоза преобладает в креветках, а также в насекомые, включая кузнечиков, саранчу, бабочек и пчел, у которых трегалоза служит сахаром в крови. Затем трегалоза расщепляется на глюкозу катаболическим ферментом треалазой для использования.[нужна цитата ]
Трегалоза - это основная молекула, запасающая энергию углеводов, используемую насекомыми для полета. Одна из возможных причин этого заключается в том, что гликозидная связь трегалозы при воздействии на нее трехалазы насекомых высвобождает две молекулы глюкозы, которые необходимы для быстрых энергетических потребностей полета. Это вдвое больше эффективности высвобождения глюкозы из запасного полимера. крахмал, для которого отщепление одной гликозидной связи высвобождает только одну молекулу глюкозы.[нужна цитата ]
В растениях трегалоза содержится в семенах подсолнечника, лунолистник, Селагинелла растения[11] и морские водоросли. Среди грибов он преобладает в некоторых грибах, таких как шиитаке (Lentinula edodes), устрица, королевская устрица и золотая игла.[12]
Даже в царстве растений Селагинелла (иногда называемое воскрешающим растением), которое растет в пустынях и горных районах, может потрескаться и высохнуть, но снова станет зеленым и возродится после дождя из-за функции трегалозы.[11]
Две распространенные теории о том, как трегалоза работает в организме в состоянии криптобиоза, являются остекловывание теория, состояние, которое предотвращает образование льда, или теория вытеснения воды, согласно которой вода заменяется трегалозой.[13]
Пищевые и диетические свойства
Трегалоза быстро расщепляется на глюкозу фермент трехалаза, который присутствует в кисть границы из слизистая оболочка кишечника всеядных (включая человека) и травоядных.[14]:135 Это вызывает меньший всплеск содержание сахара в крови чем глюкоза.[15] Трегалоза имеет около 45% сладости сахарозы при концентрациях выше 22%, но при снижении концентрации ее сладость уменьшается быстрее, чем сладость сахарозы, так что 2,3% раствор имеет вкус в 6,5 раз менее сладкий, чем эквивалентный раствор сахара.[16]:444
Его обычно используют в приготовленных замороженных продуктах, таких как мороженое, потому что он понижает точку замерзания еды.[15] В Cargill корпорация продвигает использование своей торговой марки трегалозы «Treha» как вещества, которое «усиливает и усиливает определенные вкусовые качества, чтобы раскрыть лучшее в ваших продуктах».[17]
Дефицит трехалазы фермент необычно для людей, за исключением Гренландские инуиты, где он встречается у 10–15% населения.[18]:197
Медицинское использование
Трегалоза является ингредиентом, наряду с гиалуроновая кислота, в искусственные слезы продукт, используемый для лечения сухой глаз.[19][20] Вспышки Clostridium difficile изначально были связаны с трегалозой,[15][21][22] хотя этот вывод оспаривался в 2019 году.[23]
История
В 1832 году H.A.L. Виггерс обнаружил трегалозу в спорынья ржи,[24] и в 1859 г. Марселлен Бертло изолировал это от Трехала манна, вещество, производимое долгоносики и назвал его трегалозой.[25]
Трегалоза давно известна как аутофагия индуктор, который действует независимо от mTOR.[26] В 2017 году было опубликовано исследование, показывающее, что трегалоза вызывает аутофагию, активируя TFEB,[27] белок, который действует как главный регулятор аутофагии -лизосома путь.[28]
Смотрите также
Рекомендации
- ^ Хигасияма Т. (2002). «Новые функции и применение трегалозы» (PDF). Pure Appl. Chem. 74 (7): 1263–1269. Дои:10.1351 / pac200274071263.
- ^ Лиде, Дэвид Р. (1998). Справочник по химии и физике (87 изд.). Бока-Ратон, Флорида: CRC Press. С. 3–534. ISBN 978-0-8493-0594-8.
- ^ «Трегалоза | Определение трегалозы от Lexico».
- ^ Cargill, Incorporated (30 мая 2011 г.). "Cargill и Hayashibara представят трегалозный подсластитель в Америке". PR Newswire. Получено 2011-07-31.
- ^ «ЯПОНИЯ: Cargill и Hayashibara представят трегалозный подсластитель в Америке». just-food.com. 2000-05-31. Получено 2 февраля 2013.
- ^ Патрик, Дженнифер Л .; Эллиотт, Глория Д .; Комиццоли, Пьер (1 ноября 2017 г.). «Структурная целостность и потенциал развития сперматозоидов после сушки с помощью микроволновой печи в модели домашней кошки». Териогенология. 103: 36–43. Дои:10.1016 / j.theriogenology.2017.07.037. PMID 28772113.
- ^ а б c d Эльбейн А.Д., Пан Ю.Т., Пастушак И., Кэрролл Д. (апрель 2003 г.). «Новое понимание трегалозы: многофункциональной молекулы». Гликобиология. 13 (4): 17R – 27R. Дои:10.1093 / glycob / cwg047. PMID 12626396.
- ^ [мертвая ссылка ]"Уведомление GRAS о Хаясибара трегалозе" (PDF). Управление по контролю за продуктами и лекарствами. 3 мая 2000 г .: 10. Цитировать журнал требует
| журнал =(помощь) - ^ Сапир Л., Харрис Д. (февраль 2011 г.). «Связывание самоассоциации трегалозы с уравнением состояния бинарного водного раствора». Журнал физической химии B. 115 (4): 624–34. Дои:10.1021 / jp109780n. PMID 21186829.
- ^ Безрукавников С., Машаги А., ван Вейк Р.Дж., Гу С., Ян Л.Дж., Гао Ю.К., Танс С.Дж. (октябрь 2014 г.). «Трегалоза способствует плавлению ДНК: исследование с помощью оптического пинцета с одной молекулой». Мягкая материя. 10 (37): 7269–77. Bibcode:2014SMat ... 10.7269B. Дои:10.1039 / C4SM01532K. PMID 25096217.
- ^ а б Зентелла Р., Маскорро-Галлардо Дж.О., Ван Дейк П., Фольч-Маллол Дж., Бонини Б., Ван Век С., Гаксиола Р., Коваррубиас А.А., Ньето-Сотело Дж., Тевелейн Дж. М., Итурриага Г. (апрель 1999 г.). «Трегалозо-6-фосфатсинтаза Selaginella lepidophylla дополняет рост и дефекты стрессоустойчивости у дрожжевого мутанта tps1». Физиология растений. 119 (4): 1473–82. Дои:10.1104 / pp.119.4.1473. ЧВК 32033. PMID 10198107.
- ^ Рейс Ф.С., Баррос Л., Мартинс А., Феррейра И.К. (февраль 2012 г.). «Химический состав и пищевая ценность наиболее широко известных культивируемых грибов: межвидовое сравнительное исследование» (PDF). Пищевая и химическая токсикология. 50 (2): 191–7. Дои:10.1016 / j.fct.2011.10.056. HDL:10198/7341. PMID 22056333.
- ^ Сола-Пенна М., Мейер-Фернандес-младший (декабрь 1998 г.). «Стабилизация структуры и функции ферментов против тепловой инактивации, которой способствуют сахара: почему трегалоза более эффективна, чем другие сахара?». Архивы биохимии и биофизики. 360 (1): 10–4. Дои:10.1006 / abbi.1998.0906. PMID 9826423.
- ^ Матлути, М., изд. (1999). Упаковка и консервирование пищевых продуктов. Гейтерсбург, штат Мэриленд: издательство Aspen Publishers. ISBN 978-0-8342-1349-4. Получено 25 июн 2014.
- ^ а б c Коллинз Ф (9 января 2018 г.). «Способствовала ли альтернатива столовому сахару эпидемии C. Diff.?». Блог директора NIH.
- ^ О'Брайен-Нэборс, Лин, изд. (2012). Альтернативные подсластители (4-е изд.). Бока-Ратон: CRC Press. ISBN 978-1-4398-4614-8. Получено 25 июн 2014.
- ^ «Поставщик трегалозы». Получено 14 июн 2018.
- ^ Кольмайер М (2003). Метаболизм питательных веществ. Берлингтон: Эльзевир. ISBN 978-0-08-053789-4. Получено 25 июн 2014.
- ^ Пинто-Бонилья JC, Дель Ольмо-Химено A, Льовет-Осуна F, Эрнандес-Галилея E (2015). «Рандомизированное перекрестное исследование, сравнивающее глазные капли трегалозы / гиалуроната и стандартное лечение: удовлетворенность пациентов лечением синдрома сухого глаза». Терапия и управление клиническими рисками. 11: 595–603. Дои:10.2147 / TCRM.S77091. ЧВК 4403513. PMID 25926736.
- ^ Пакер А.Д., Нг С.М., Николс Дж. Дж. (Февраль 2016 г.). «Безрецептурные капли искусственной слезы при синдроме сухого глаза». Кокрановская база данных систематических обзоров. 2: CD009729. Дои:10.1002 / 14651858.CD009729.pub2. ЧВК 5045033. PMID 26905373.
- ^ Баллард Дж. Д. (январь 2018 г.). «Патогены, усиленные пищевой добавкой». Природа. 553 (7688): 285–286. Дои:10.1038 / d41586-017-08775-4. PMID 29345660.
- ^ Коллинз Дж., Робинсон С., Данхоф Х., Кнетч С.В., ван Лиувен ХК, Лоули Т.Д., Аухтунг Дж. М., Бриттон Р. А. (январь 2018 г.). «Диетическая трегалоза увеличивает вирулентность эпидемии Clostridium difficile». Природа. 553 (7688): 291–294. Bibcode:2018Натура.553..291C. Дои:10.1038 / природа25178. ЧВК 5984069. PMID 29310122.
- ^ Эйр, Дэвид В .; Дидело, Ксавье; Бакли, Энтони М .; Фриман, Джейн; Моура, Инес Б .; Крук, Деррик В .; Пето, Тим Э.А.; Уокер, А. Сара; Wilcox, Mark H .; Дингл, Кейт Э. (2019). «Варианты метаболизма трегалозы Clostridium difficile являются обычными и не связаны с неблагоприятными исходами для пациентов, если они по-разному присутствуют в одной и той же линии». EBioMedicine. 43: 347–355. Дои:10.1016 / j.ebiom.2019.04.038. ISSN 2352-3964. ЧВК 6558026. PMID 31036529.
- ^ Виггерс HA (1832 г.). "Untersuchung über das Mutterkorn, Secale cornutum". Annalen der Pharmacie. 1 (2): 129–182. Дои:10.1002 / jlac.18320010202.
- ^ Тиллекин F (июль 2009 г.). «Le Tréhala, une drogue à la croisée des chemins» [Трехала, место встречи зоологии, ботаники, химии и биохимии]. Revue d'Histoire de la Pharmacie (На французском). 57 (362): 163–72. Дои:10.3406 / Pharm.2009.22043. PMID 20027793.
- ^ Menzies FM, Fleming A, Rubinsztein DC (июнь 2015 г.). «Нарушение аутофагии и нейродегенеративные заболевания». Обзоры природы. Неврология. 16 (6): 345–57. Дои:10.1038 / nrn3961. PMID 25991442.
- ^ Шарма Дж., Ди Ронза А., Лотфи П., Сардиелло М. (июль 2018 г.). «Лизосомы и здоровье мозга». Ежегодный обзор нейробиологии. 41: 255–276. Дои:10.1146 / annurev-neuro-080317-061804. PMID 29661037.
- ^ Сардиелло М (май 2016 г.). «Фактор транскрипции EB: от главного координатора лизосомальных путей до кандидата в терапевтическую мишень при дегенеративных болезнях накопления». Летопись Нью-Йоркской академии наук. 1371 (1): 3–14. Bibcode:2016НЯСА1371 .... 3С. Дои:10.1111 / няс.13131. ЧВК 5032832. PMID 27299292.
внешняя ссылка
 СМИ, связанные с Трегалоза в Wikimedia Commons
СМИ, связанные с Трегалоза в Wikimedia Commons- Трегалоза в сохранении спермы
