Пептид - Peptide

синий отмечен карбоксильный конец (L-аланин ).
Пептиды (из греческий язык πεπτός, пепто «переваренный»; полученный из πέσσειν, Песен "переваривать") - короткие цепочки от двух до пятидесяти аминокислоты, связаны пептидные связи.[1][2] Цепочки из менее чем десяти или пятнадцати аминокислот называются олигопептиды, и включать дипептиды, трипептиды, и тетрапептиды.
А полипептид представляет собой более длинную, непрерывную, неразветвленную пептидную цепь, состоящую примерно из пятидесяти аминокислот.[3] Следовательно, пептиды относятся к широким химическим классам биологические полимеры и олигомеры, рядом с нуклеиновые кислоты, олигосахариды, полисахариды, и другие.
Полипептид, содержащий более пятидесяти аминокислот, известен как белок.[3][4][5] Белки состоят из одного или нескольких полипептидов, расположенных биологически функциональным образом, часто связанных с лиганды Такие как коферменты и кофакторы, или к другому белку или другому макромолекула Такие как ДНК или же РНК, или сложить макромолекулярные сборки.[6]
Аминокислоты, включенные в пептиды, называются остатки. При образовании каждого из них высвобождается молекула воды. амид связь.[7] Все пептиды, кроме циклические пептиды есть N-концевой (аминогруппа) и C-терминал (карбоксильная группа) остаток на конце пептида (как показано для тетрапептида на изображении).
Классы
Известно много видов пептидов. Они были классифицированы или разделены на категории в зависимости от их источников и функций. Согласно Справочнику по биологически активным пептидам, некоторые группы пептидов включают пептиды растений, пептиды бактерий / антибиотиков, пептиды грибов, пептиды беспозвоночных, пептиды амфибий / кожи, пептиды яда, пептиды рака / противоопухолевые, пептиды вакцины, иммунные / воспалительные пептиды, мозг пептиды, эндокринные пептиды, пищевые пептиды, желудочно-кишечные пептиды, сердечно-сосудистые пептиды, почечные пептиды, респираторные пептиды, опиатные пептиды, нейротрофические пептиды и пептиды кровь-мозг.[8]
Некоторые рибосомальные пептиды подвержены протеолиз. Эти функции, как правило, у высших организмов, как гормоны и сигнальные молекулы. Некоторые организмы производят пептиды в виде антибиотики, Такие как микроцины и бактериоцины.[9]
Пептиды часто имеют посттрансляционные модификации Такие как фосфорилирование, гидроксилирование, сульфирование, пальмитоилирование, гликозилирование и дисульфид формирование. В целом пептиды линейны, хотя лариат структуры наблюдались.[10] Встречаются и более экзотические манипуляции, такие как рацемизация L-аминокислот в D-аминокислоты в яд утконоса.[11]
Нерибосомальные пептиды собраны ферменты а не рибосома. Обычным нерибосомным пептидом является глутатион, компонент антиоксидант защитные силы большинства аэробных организмов.[12] Другие нерибосомальные пептиды наиболее распространены в одноклеточные организмы, растения, и грибы и синтезируются модульный ферментные комплексы, называемые нерибосомные пептидные синтетазы.[13]
Эти комплексы часто располагаются сходным образом и могут содержать множество различных модулей для выполнения разнообразных химических манипуляций с развивающимся продуктом.[14] Эти пептиды часто циклический и могут иметь очень сложные циклические структуры, хотя линейные нерибосомные пептиды также широко распространены. Поскольку система тесно связана с машинным оборудованием для строительства жирные кислоты и поликетиды, часто встречаются гибридные соединения. Наличие оксазолы или же тиазолы часто указывает на то, что соединение было синтезировано таким образом.[15]
Пептоны получены из молока или мяса животных, перевариваемых протеолиз.[16] Помимо небольших пептидов, полученный материал включает жиры, металлы, соли, витамины и многие другие биологические соединения. Пептоны используются в питательных средах для выращивания бактерий и грибов.[17]
Пептидные фрагменты относятся к фрагментам белков, которые используются для идентификации или количественной оценки исходного белка.[18] Часто это продукты ферментативного разложения, проведенного в лаборатории на контролируемом образце, но также это могут быть образцы судебно-медицинской экспертизы или палеонтологические образцы, которые подверглись разложению в результате естественного воздействия.[19][20]
Химический синтез

Примеры семей
Семейства пептидов в этом разделе представляют собой рибосомальные пептиды, обычно с гормональной активностью. Все эти пептиды синтезируются клетками как более длинные «пропептиды» или «пропротеины» и усекаются перед выходом из клетки. Они попадают в кровоток, где выполняют свои сигнальные функции.
Антимикробные пептиды
- Магайнин семья
- Цекропин семья
- Кателицидин семья
- Дефенсин семья
Тахикининовые пептиды
Вазоактивные кишечные пептиды
- VIP (Vнеактивный якишечный пэптид; PHM27)
- PACAP пмуниципальный Аденилат Cиклаз Аактивизирующий пэптид
- Пептид ФИ 27 (пэптид ЧАСистидин ясолейцин 27)
- GHRH 1-24 (граммгрядка ЧАСОрмон рэлизинг ЧАСормон 1-24)
- Глюкагон
- Секретин
- NPY (Nевропэптид Y)
- PYY (пэптид YY)
- ПРИЛОЖЕНИЕ (Авиан панкреатический полипептид)
- PPY панкреатический полYпептид
Опиоидные пептиды
- Проопиомеланокортин (POMC) пептиды
- Энкефалин пентапептиды
- Продинорфин пептиды
Кальцитониновые пептиды
Самособирающиеся пептиды
- Ароматические короткие пептиды[21][22]
- Биомиметические пептиды[23]
- Пептидные амфифилы[24][25][26][27]
- Пептидные дендримеры[28]
Другие пептиды
- Натрийуретический пептид типа B (BNP) - производятся в миокарде и используются в медицинской диагностике
- Лактотрипептиды - Лактотрипептиды могут снизить артериальное давление,[29][30][31] хотя доказательства неоднозначны.[32]
- Пептидные компоненты из традиционной китайской медицины Colla Corii Asini в гемопоэзе.[33]
Терминология
Длина
Некоторые термины, относящиеся к пептидам, не имеют строгих определений длины, и их использование часто перекрывается.
- А полипептид представляет собой единую линейную цепь из множества аминокислот (любой длины), удерживаемых вместе амидные связи.
- А белок состоит из одного или нескольких полипептидов (длиной более 50 аминокислот).
- An олигопептид состоит всего из нескольких аминокислот (от двух до двадцати).
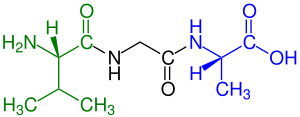
зеленый отмечен амино конец (L-валин ) и
синий отмечен карбоксильный конец (L-аланин )
Количество аминокислот
Пептиды определенной длины именуются с использованием Числовой множитель ИЮПАК префиксы.
- А монопептид имеет одну аминокислоту.
- А дипептид имеет две аминокислоты.
- А трипептид имеет три аминокислоты.
- А тетрапептид имеет четыре аминокислоты.
- А пентапептид имеет пять аминокислот.
- А гексапептид имеет шесть аминокислот.
- А гептапептид имеет семь аминокислот.
- An октапептид имеет восемь аминокислот (например, ангиотензин II ).
- А нонапептид имеет девять аминокислот (например, окситоцин ).
- А декапептид имеет десять аминокислот (например, гонадотропин-рилизинг гормон и ангиотензин I ).
Функция
- А нейропептид представляет собой пептид, который активен в связи с нервной тканью.
- А липопептид пептид, имеющий липид подключен к нему, и пепдуцины липопептиды, которые взаимодействуют с GPCR.
- А пептидный гормон пептид, который действует как гормон.
- А протеоз представляет собой смесь пептидов, образующихся при гидролизе белков. Термин несколько архаичный.
- А пептидергический агент (или лекарство) - это химическое вещество, которое действует для прямой модуляции пептидных систем в организме или головном мозге. Примером является опиоидергические препараты, которые нейропептидергики.
Смотрите также
- Ацетилгексапептид-3
- Мясистый мясистый пептид
- Пептид гибридизации коллагена, короткий пептид, который может связываться с денатурированным коллагеном в тканях.
- Бис-пептид
- CLE пептид
- Фактор эпидермального роста
- Журнал пептидной науки
- Лактотрипептиды
- Микропептид
- Многофункциональный пептид
- Нейропептид
- Пальмитоил пентапептид-4
- Гормон поджелудочной железы
- пептидная спектральная библиотека
- Синтез пептидов
- Пептидомиметики (Такие как пептоиды и β-пептиды ) до пептидов, но с другими свойствами.
- Белковая метка, описывающий добавление пептидных последовательностей для выделения или обнаружения белка
- Репликины
- Рибосома
- Перевод (биология)
Рекомендации
- ^ Хэмли, Айленд (сентябрь 2020 г.). введение в науку о пептидах. Вайли. ISBN 9781119698173.
- ^ Нельсон, Дэвид Л .; Кокс, Майкл М. (2005). Принципы биохимии (4-е изд.). Нью-Йорк: У. Х. Фриман. ISBN 0-7167-4339-6.
- ^ а б Саладин, К. (13 января 2011 г.). Анатомия и физиология: единство формы и функции (6-е изд.). Макгроу-Хилл. п. 67. ISBN 9780073378251.
- ^ ИЮПАК, Сборник химической терминологии, 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "белки ". Дои:10.1351 / goldbook.P04898
- ^ «Что такое пептиды». Зеландия Фарма A / S. В архиве из оригинала от 29.04.2019.
- ^ Ardejani, Maziar S .; Орнер, Брендан П. (2013-05-03). «Соблюдайте правила сборки пептидов». Наука. 340 (6132): 561–562. Bibcode:2013Наука ... 340..561A. Дои:10.1126 / science.1237708. ISSN 0036-8075. PMID 23641105. S2CID 206548864.
- ^ ИЮПАК, Сборник химической терминологии, 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "аминокислотный остаток в полипептиде ". Дои:10.1351 / goldbook.A00279
- ^ Абба Дж. Кастин, изд. (2013). Справочник по биологически активным пептидам (2-е изд.). ISBN 978-0-12-385095-9.
- ^ Duquesne S, Destoumieux-Garzón D, Peduzzi J, Rebuffat S (август 2007 г.). «Микроцины, кодируемые генами антибактериальные пептиды энтеробактерий». Отчеты о натуральных продуктах. 24 (4): 708–34. Дои:10.1039 / b516237h. PMID 17653356.
- ^ Понс М., Фелиз М., Антония Молинс М., Гиралт Э. (май 1991 г.). «Конформационный анализ бацитрацина А, природного лариата». Биополимеры. 31 (6): 605–12. Дои:10.1002 / bip.360310604. PMID 1932561. S2CID 10924338.
- ^ Торрес AM, Menz I, Alewood PF и др. (Июль 2002 г.). «Остаток D-аминокислоты в натрийуретическом пептиде С-типа из яда млекопитающего Ornithorhynchus anatinus, австралийского утконоса». Письма FEBS. 524 (1–3): 172–6. Дои:10.1016 / S0014-5793 (02) 03050-8. PMID 12135762. S2CID 3015474.
- ^ Мейстер А, Андерсон МЭ; Андерсон (1983). «Глутатион». Ежегодный обзор биохимии. 52 (1): 711–60. Дои:10.1146 / annurev.bi.52.070183.003431. PMID 6137189.
- ^ Hahn M, Stachelhaus T; Stachelhaus (ноябрь 2004 г.). «Избирательному взаимодействию между нерибосомными пептидными синтетазами способствуют короткие домены, опосредующие связь». Труды Национальной академии наук Соединенных Штатов Америки. 101 (44): 15585–90. Bibcode:2004PNAS..10115585H. Дои:10.1073 / pnas.0404932101. ЧВК 524835. PMID 15498872.
- ^ Finking R, Marahiel MA; Марахиэль (2004). «Биосинтез нерибосомальных пептидов1». Ежегодный обзор микробиологии. 58 (1): 453–88. Дои:10.1146 / annurev.micro.58.030603.123615. PMID 15487945.
- ^ Ду Л, Шен Б; Шен (март 2001 г.). «Биосинтез гибридных пептидно-поликетидных природных продуктов». Текущее мнение в области открытия и разработки лекарств. 4 (2): 215–28. PMID 11378961.
- ^ «UsvPeptides- USVPeptides - ведущая фармацевтическая компания в Индии». USVПептиды.
- ^ Пейн JW (1976). «Пептиды и микроорганизмы». Успехи микробной физиологии. 13: 55–113. Дои:10.1016 / S0065-2911 (08) 60038-7. ISBN 9780120277131. PMID 775944. Цитировать журнал требует
| журнал =(помощь) - ^ Хаммель Дж., Ниманн М., Винкооп С., Шульце В., Штайнхаузер Д., Селбиг Дж., Вальтер Д., Векверт В. (2007). «ProMEX: справочная база данных масс-спектров для белков и сайтов фосфорилирования белков». BMC Bioinformatics. 8 (1): 216. Дои:10.1186/1471-2105-8-216. ЧВК 1920535. PMID 17587460.
- ^ Вебстер Дж., Оксли Д.; Оксли (2005). Массовый фингерпринтинг пептидов: идентификация белков с помощью масс-спектрометрии MALDI-TOF. Методы молекулярной биологии. Методы молекулярной биологии ™. 310. С. 227–40. Дои:10.1007/978-1-59259-948-6_16. ISBN 978-1-58829-399-2. PMID 16350956.
- ^ Marquet P, Lachâtre G; Lachâtre (октябрь 1999 г.). «Жидкостная хроматография-масс-спектрометрия: возможности судебной медицины и клинической токсикологии». Журнал хроматографии B. 733 (1–2): 93–118. Дои:10.1016 / S0378-4347 (99) 00147-4. PMID 10572976.
- ^ Тао, Кай; Макам, Пандеесвар; Айзен, Рут; Газит, Эхуд (17 ноя 2017). «Самособирающиеся пептидные полупроводники». Наука. 358 (6365): eaam9756. Дои:10.1126 / science.aam9756. ЧВК 5712217. PMID 29146781.
- ^ Тао, Кай; Левин, Авиад; Адлер-Абрамович, Лихи; Газит, Эхуд (26 апреля 2016 г.). «Fmoc-модифицированные аминокислоты и короткие пептиды: простые биологические строительные блоки для изготовления функциональных материалов». Chem. Soc. Rev. 45 (14): 3935–3953. Дои:10.1039 / C5CS00889A. PMID 27115033.
- ^ Тао, Кай; Ван, Цзицянь; Чжоу, Пэн; Ван, Чэндун; Сюй, Хай; Чжао, Сюбо; Лу, Цзянь Р. (10 февраля 2011 г.). "Самосборка коротких пептидов Aβ (16-22): эффект концевого кэппинга и роль электростатического взаимодействия". Langmuir. 27 (6): 2723–2730. Дои:10.1021 / la1034273. PMID 21309606.
- ^ Ян Хэмли (2011). «Самосборка амфифильных пептидов» (PDF). Мягкая материя. 7 (9): 4122–4138. Дои:10.1039 / C0SM01218A.CS1 maint: использует параметр авторов (связь)
- ^ Кай Тао, Гай Джейкоби, Люба Бурлака, Рой Бек, Эхуд Газит (26 июля 2016 г.). «Дизайн управляемых биовдохновленных хироптических самосборок». Биомакромолекулы. 17 (9): 2937–2945. Дои:10.1021 / acs.biomac.6b00752. PMID 27461453.CS1 maint: использует параметр авторов (связь)
- ^ Кай Тао, Авиад Левин, Гай Джейкоби, Рой Бек, Эхуд Газит (23 августа 2016 г.). «Энтропийные фазовые переходы со стабильными скрученными промежуточными продуктами самосборки, вызванной биоинспекцией». Chem. Евро. J. 22 (43): 15237–15241. Дои:10.1002 / chem.201603882. PMID 27550381.CS1 maint: использует параметр авторов (связь)
- ^ Дунхуэй Цзя, Кай Тао, Цзицянь Ван, Чэндон Ван, Сюбо Чжао, Мохаммед Ясин, Хай Сюй, Гохэ Цюэ, Джон Р. П. Вебстер, Цзян Р. Лу (16 июня 2011 г.). «Динамическая адсорбция и структура межфазных бислоев, адсорбированных липопептидными поверхностно-активными веществами на границе гидрофильный кремний / вода: влияние длины головной группы». Langmuir. 27 (14): 8798–8809. Дои:10.1021 / la105129m. PMID 21675796.CS1 maint: использует параметр авторов (связь)
- ^ Хайц, Марк; Явор, Саша; Дарбре, Тамис; Реймон, Жан-Луи (21.08.2019). «Стереоселективные pH-чувствительные пептидные дендримеры для трансфекции миРНК». Биоконъюгат Химия. 30 (8): 2165–2182. Дои:10.1021 / acs.bioconjchem.9b00403. ISSN 1043-1802. PMID 31398014.
- ^ Boelsma E, Kloek J; Kloek (март 2009 г.). «Лактотрипептиды и антигипертензивные эффекты: критический обзор». Британский журнал питания. 101 (6): 776–86. Дои:10.1017 / S0007114508137722. PMID 19061526.
- ^ Сюй Цз.Ю., Цинь Л.К., Ван ПЙ, Ли В., Чанг С. (октябрь 2008 г.). «Влияние трипептидов молока на артериальное давление: метаанализ рандомизированных контролируемых исследований». Питание. 24 (10): 933–40. Дои:10.1016 / я.нут.2008.04.004. PMID 18562172.
- ^ Припп АХ (2008). «Влияние пептидов, полученных из пищевых белков, на артериальное давление: метаанализ рандомизированных контролируемых исследований». Исследования в области пищевых продуктов и питания. 52: 10.3402 / fnr.v52i0.1641. Дои:10.3402 / fnr.v52i0.1641. ЧВК 2596738. PMID 19109662.
- ^ Engberink MF, Schouten EG, Kok FJ, van Mierlo LA, Brouwer IA, Geleijnse JM (февраль 2008 г.). «Лактотрипептиды не влияют на кровяное давление человека: результаты двойного слепого рандомизированного контролируемого исследования». Гипертония. 51 (2): 399–405. Дои:10.1161 / ГИПЕРТЕНЗИЯAHA.107.098988. PMID 18086944.
- ^ Ву, Хунчжун; Рен, Чунян; Ян, Клык; Цинь, Юйфэн; Чжан, Юаньсин; Лю, Цзяньвэнь (апрель 2016 г.). «Извлечение и идентификация пептидов, полученных из коллагена с кроветворной активностью из Colla Corii Asini». Журнал этнофармакологии. 182: 129–136. Дои:10.1016 / j.jep.2016.02.019. PMID 26911525.
