Жировая ткань - Adipose tissue
| Жировая ткань | |
|---|---|
 Жировая ткань - один из основных видов соединительная ткань. | |
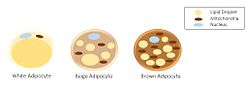 Морфология трех разных классов адипоцитов. | |
| Произношение | /ˈædɪˌпoʊs/ ( |
| Идентификаторы | |
| MeSH | D000273 |
| FMA | 20110 |
| Анатомическая терминология | |
Жировая ткань, телесный жир, или просто толстый свободный соединительная ткань состоит в основном из адипоциты.[1] Помимо адипоцитов, жировая ткань содержит стромальная сосудистая фракция (SVF) клеток, включая преадипоциты, фибробласты, сосудистый эндотелиальные клетки и различные иммунные клетки, такие как макрофаги жировой ткани. Жировая ткань происходит из преадипоцитов. Его основная роль - хранить энергию в виде липиды, хотя он также смягчает и изолирует тело. В последние годы жировая ткань не только гормонально инертна, но и признана одной из основных эндокринный орган[2] как он производит гормоны Такие как лептин, эстроген, сопротивляться, и цитокин (особенно TNFα ). Два типа жировой ткани: белая жировая ткань (WAT), в котором накапливается энергия, и коричневая жировая ткань (BAT), который выделяет тепло тела. Формирование жировой ткани, по-видимому, частично контролируется жировой ген. Жировая ткань, а точнее коричневая жировая ткань, была впервые идентифицирована швейцарским естествоиспытателем. Конрад Гесснер в 1551 г.[3]
Анатомические особенности

У человека жировая ткань расположена: под кожа (подкожный жир ), вокруг внутренней органы (нутряной жир ), в костном мозге (желтый костный мозг ), межмышечный (Мышечная система ) и в груди (ткани молочной железы ). Жировая ткань находится в определенных местах, которые называются жировые отложения. Помимо адипоцитов, которые составляют самый высокий процент клеток в жировой ткани, присутствуют другие типы клеток, все вместе называемые стромальной сосудистой фракцией (SVF) клеток. SVF включает преадипоциты, фибробласты, жировая ткань макрофаги, и эндотелиальные клетки. Жировая ткань содержит много мелких кровеносный сосуд. в покровная система, который включает в себя кожу, он накапливается на самом глубоком уровне, подкожный слой, обеспечивающий изоляцию от жары и холода. Он обеспечивает защитную прокладку вокруг органов. Однако его основная функция - быть запасом липидов, которые могут окисляться для удовлетворения энергетических потребностей организма и защиты его от избытка глюкозы путем хранения триглицеридов, производимых печенью из сахаров, хотя некоторые данные свидетельствуют о том, что большая часть синтеза липидов из углеводов происходит в самой жировой ткани.[4] Жировые депо в разных частях тела имеют разные биохимические профили. В нормальных условиях он обеспечивает обратную связь с мозгом о голоде и диете.
мышей
У мышей восемь основных жировых депо, четыре из которых находятся в брюшная полость.[1] Парные гонадальные депо прикрепляются к матка и яичники у женщин и придаток яичка и яички у мужчин; парные забрюшинные депо находятся вдоль спинной стена брюшная полость, окружает почку и в массивном случае распространяется в таз. Депо брыжейки образует похожую на клей сеть, которая поддерживает кишечник и сальниковое депо (которое берет начало недалеко от желудок и селезенка ) и - в массивном - простирается в брюшную полость. И брыжеечные, и сальниковые депо содержат много лимфоидная ткань как лимфатические узлы и молочные пятна, соответственно.
Два поверхностных депо - это парные паховые депо, которые находятся впереди верхнего сегмента задних конечностей (под кожей) и подлопаточные депо, парные медиальные смеси коричневой жировой ткани, прилегающие к участкам белой жировой ткани, которые обнаруживаются. под кожа между спинными гребнями лопаток. Слой коричневой жировой ткани в этом депо часто покрыт «глазурью» белой жировой ткани; иногда эти два типа жира (коричневый и белый) трудно различить. Паховые отложения охватывают паховую группу лимфатических узлов. Незначительные склады включают перикардиальный, который окружает сердце, и парные подколенные депо между основными мышцами за коленями, каждая из которых содержит по одной большой лимфатический узел.[5] Из всех депо у мышей половые депо являются самыми большими и наиболее легко расчлененными.[6] содержащий около 30% расслаиваемого жира.[7]
Ожирение
В тучный человека, избыточная жировая ткань, свисающая вниз от живота, называется панникулюс. Панникулус осложняет операцию у человека с болезненным ожирением. Он может оставаться в буквальном смысле «кожным фартуком», если человек с тяжелым ожирением быстро теряет большое количество жира (частый результат операция обходного желудочного анастомоза ). Ожирение лечится с помощью упражнений, диеты и поведенческой терапии. Реконструктивная хирургия - один из методов лечения.[8]
Нутряной жир
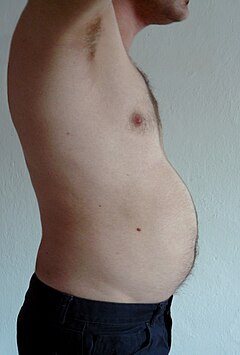
Висцеральный жир или абдоминальный жир[9] (также известный как органный жир или интраабдоминальный жир) находится внутри брюшная полость, упакованные между органами (желудок, печень, кишечник, почки и т. д.). Висцеральный жир отличается от подкожный жир под кожа, и внутримышечный жир вперемешку с скелетные мышцы. Жир в нижней части тела, например в бедрах и ягодицах, является подкожным и представляет собой не равномерно распределенную ткань, тогда как жир в брюшная полость в основном висцеральный и полужидкий.[10] Висцеральный жир состоит из нескольких жировых отложений, в том числе брыжеечный, придаток яичка белая жировая ткань (EWAT) и периренальный депо. Висцеральный жир часто выражается в его площади в см.2 (VFA, область висцерального жира).[11]
Избыток висцерального жира известен как центральное ожирение, или «жир живота», при котором живот чрезмерно выпячивается. Новые разработки, такие как Индекс объема тела (BVI) специально разработаны для измерения объема брюшной полости и брюшного жира. Избыточный висцеральный жир также связан с диабет 2 типа,[12] резистентность к инсулину,[13] воспалительные заболевания,[14] и другие заболевания, связанные с ожирением.[15] Аналогичным образом, накопление шейного жира (или шейной жировой ткани) связано со смертностью.[16] Несколько исследований показали, что висцеральный жир можно предсказать с помощью простых антропометрических измерений.[17] и прогнозирует смертность более точно, чем индекс массы тела или окружность талии.[18]
У мужчин больше шансов накапливать жир в брюшной полости из-за: различия половых гормонов. Женский половой гормон вызывает накопление жира в ягодицах, бедрах и бедрах у женщин.[19][20] Когда женщины достигают менопауза снижается уровень эстрогена, вырабатываемого яичниками, жир мигрирует из ягодиц, бедер и бедер к талии;[21] позже жир откладывается в брюшной полости.[10]
Упражнения высокой интенсивности - это один из способов эффективно снизить общий уровень абдоминального жира.[22][23] Одно исследование предлагает не менее 10 ВСТРЕТИЛИСЬ -часов в неделю упражнение аэробики требуется для уменьшения висцерального жира.[24] Диета с ограничением энергии в сочетании с упражнениями уменьшит общий жир тела и соотношение висцеральной жировой ткани к подкожной жировой ткани, предполагая преимущественную мобилизацию висцерального жира над подкожным.[25]
Эпикардиальный жир
Эпикардиальный жировая ткань (EAT) - это особая форма висцерального жира, откладывающегося вокруг сердца и являющегося метаболически активным органом, генерирующим различные биоактивные молекулы, которые могут значительно повлиять на сердечный функция.[26] Заметные различия компонентов наблюдались при сравнении EAT с подкожный жир, что предполагает специфическое влияние депо накопленных жирных кислот на функцию и метаболизм адипоцитов.[27]
Подкожный жир
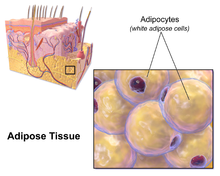
Большая часть оставшегося невисцерального жира находится чуть ниже кожи в области, называемой гиподерма.[28] Этот подкожный жир не связан со многими классическими патологиями, связанными с ожирением, такими как сердечное заболевание, рак и Инсульт, и некоторые данные даже предполагают, что это может быть защитным.[29] Типично женский (или гинекоидный) образец распределения жира в организме вокруг бедер, бедер и ягодиц - это подкожный жир, поэтому он представляет меньший риск для здоровья по сравнению с висцеральным жиром.[30][31]
Как и все другие жировые органы, подкожный жир является активной частью эндокринной системы, вырабатывающей гормоны. лептин и сопротивляться.[28]
Взаимосвязь между подкожным жировым слоем и общим содержанием жира в организме человека часто моделируется с помощью уравнений регрессии. Наиболее популярное из этих уравнений было составлено Дарнином и Уормерсли, которые тщательно протестировали многие типы кожных складок и в результате создали две формулы для расчета плотности тела как мужчин, так и женщин. Эти уравнения представляют обратную корреляцию между кожными складками и плотностью тела - по мере увеличения суммы кожных складок плотность тела уменьшается.[32]
Такие факторы, как пол, возраст, численность населения или другие переменные, могут сделать уравнения недействительными и непригодными для использования, а с 2012 г.[Обновить], Уравнения Дарнина и Уормерсли остаются лишь оценками истинного уровня полноты человека. Новые формулы все еще создаются.[32]
Костный жир
Костный жир, также известный как жировая ткань костного мозга (МАТ ), представляет собой малоизученное жировое депо, которое находится в кости и перемежается кроветворными клетками, а также костными элементами. Адипоциты в этом депо происходят из мезенхимальные стволовые клетки (МСК) которые могут давать начало жировым клеткам, костным клеткам, а также другим типам клеток. Тот факт, что MAT увеличивается при ограничении калорийности / анорексии, является особенностью, которая отличает это депо от других жировых депо.[33][34][35] Упражнения регулируют МАТ, уменьшая количество МАТ и уменьшая размер адипоцитов костного мозга.[36][37][38] Регулирование содержания жира в костном мозге при физической нагрузке предполагает, что он имеет некоторое физиологическое сходство с другими депо белого жира. Более того, повышенный уровень МАТ при ожирении также предполагает сходство с депо белого жира.[36]
Эктопический жир
Внематочный жир - это хранилище триглицериды в тканях, отличных от жировой, которые, как предполагается, содержат лишь небольшое количество жира, например печень, скелетные мышцы, сердце, и поджелудочная железа.[1] Это может мешать клеточным функциям и, следовательно, функциям органов, и связано с инсулинорезистентностью при диабете 2 типа.[39] Он хранится в относительно больших количествах вокруг органов брюшная полость, но не следует путать с висцеральным жиром.
Конкретная причина накопления эктопического жира неизвестна. Причина, вероятно, заключается в сочетании генетических, экологических и поведенческих факторов, которые участвуют в избыточном потреблении энергии и снижении физической активности. Существенная потеря веса может уменьшить эктопические жировые отложения во всех органах, и это связано с улучшением функции этого органа.[39]
В последнем случае неинвазивные меры по снижению веса, такие как диета или упражнения, могут уменьшить эктопический жир (особенно в сердце и печени) у детей и взрослых с избыточным весом или ожирением.[40][41]
Физиология
Свободные жирные кислоты (FFA) освобождены от липопротеины к липопротеинлипаза (LPL) и попадают в адипоцит, где они снова собираются в триглицериды к этерифицирующий их на глицерин. В жировой ткани человека содержится около 87% липиды.[42]
Существует постоянный поток свободных жирных кислот, поступающих и покидающих жировую ткань. Чистое направление этого потока контролируется инсулином и лептином - если инсулин повышен, тогда возникает чистый приток FFA внутрь, и только при низком уровне инсулина FFA могут покинуть жировую ткань. Секреция инсулина стимулируется высоким уровнем сахара в крови, который возникает в результате потребления углеводов.[43]
У людей липолиз (гидролиз триглицеридов до свободных жирных кислот) контролируется посредством сбалансированного контроля липолитических свойств. B-адренорецепторы и антилиполиз, опосредованный a2A-адренергическим рецептором.
Жировые клетки имеют важное физиологический роль в поддержании уровня триглицеридов и свободных жирных кислот, а также определение резистентность к инсулину. Брюшной жир имеет другое метаболический профиль - более склонен к развитию инсулинорезистентности. Это в значительной степени объясняет, почему центральное ожирение является маркером нарушения толерантности к глюкозе и является независимым фактором риска сердечно-сосудистые заболевания (даже при отсутствии сахарный диабет и гипертония ).[44] Исследования самок обезьян на Университет Уэйк Форест (2009) обнаружили, что люди, страдающие высшей стресс имеют более высокий уровень висцерального жира в организме. Это предполагает возможную причинно-следственную связь между ними, при которой стресс способствует накоплению висцерального жира, что, в свою очередь, вызывает гормональные и метаболические изменения, которые способствуют сердечным заболеваниям и другим проблемам со здоровьем.[45]
Последние достижения в области биотехнологии позволили собирать урожай взрослые стволовые клетки из жировой ткани, что позволяет стимулировать рост тканей с использованием собственных клеток пациента. Кроме того, как сообщается, стволовые клетки, полученные из жировой ткани, от человека и животных, можно эффективно перепрограммировать в индуцированные плюрипотентные стволовые клетки без необходимости питающие ячейки.[46] Использование собственных клеток пациента снижает вероятность отторжения тканей и позволяет избежать этических проблем, связанных с использованием человеческих эмбриональные стволовые клетки.[47] Растущее количество данных также свидетельствует о том, что различные жировые отложения (например, брюшные, сальниковые, перикардиальные) дают стволовые клетки, полученные из жировой ткани, с разными характеристиками.[47][48] Эти зависящие от депо функции включают скорость распространения, иммунофенотип, потенциал дифференциации, экспрессия гена, а также чувствительность к условиям гипоксической культуры.[49] Уровни кислорода, по-видимому, играют важную роль в метаболизме и в целом функции стволовых клеток, полученных из жировой ткани.[50]
Жировая ткань является основным периферическим источником ароматаза как у мужчин, так и у женщин, способствуя производству эстрадиол.[51]
Гормоны из жировой ткани включают:
Жировая ткань также выделяет тип цитокины (сигнальные белки от клетки к клетке), называемые адипокины (жировые цитокины), которые играют роль в осложнениях, связанных с ожирением. Периваскулярная жировая ткань выделяет адипокины, такие как адипонектин, которые влияют на сократительную функцию окружающих их сосудов.[1][52]
Бурый жир

Бурый жир или коричневая жировая ткань (BAT) - это особая форма жировой ткани, важная для адаптивного термогенез у человека и других млекопитающих. BAT может генерировать тепло, "разъединяя" дыхательная цепь из окислительного фосфорилирования в митохондрии через тканеспецифическое выражение разобщающий белок 1 (UCP1).[53] BAT в основном расположены вокруг шеи и крупных кровеносных сосудов грудная клетка, где может эффективно действовать при теплообмене. BAT активно активируется при воздействии холода путем выделения катехоламины из симпатические нервы что приводит к активации UCP1. Активация BAT также может происходить в ответ на перекорм.[54] Активность UCP1 стимулируется длинноцепочечными жирными кислотами, которые образуются после β-адренорецептор активация.[53] Предполагается, что UCP1 действует как протон жирной кислоты. сторонник, хотя точный механизм еще предстоит выяснить.[55] Напротив, UCP1 ингибируется АТФ, ADP, и GTP.[56]
Попытки смоделировать этот процесс фармакологически до сих пор были безуспешными. Методы управления дифференциацией «бурого жира» могут стать механизмом потеря веса терапии в будущем, стимулируя рост тканей с помощью этого специализированного метаболизма, не вызывая его в других органах.
До недавнего времени считалось, что коричневая жировая ткань в первую очередь ограничивается грудными детьми у людей, но теперь новые данные опровергли это мнение. Метаболически активная ткань с температурной реакцией, подобной коричневой жировой ткани, была впервые обнаружена в шее и туловище некоторых взрослых людей в 2007 году.[57] и присутствие коричневого жира у взрослых людей было позже подтверждено гистологически в тех же анатомических областях.[58][59][60]
Бежевый жир и WAT подрумянивание
Потемнение WAT, также называемое «появлением», происходит, когда адипоциты в депо WAT развивают черты BAT. Бежевые адипоциты приобретают многоячеистый вид (содержат несколько липидных капель) и увеличивают экспрессию разобщающий белок 1 (UCP1).[61] При этом эти обычно накапливающие энергию адипоциты становятся адипоцитами, высвобождающими энергию.
Способность коричневого и бежевого жира сжигать калории широко изучалась, поскольку исследовательские усилия сосредоточены на методах лечения ожирения и диабета. Наркотик 2,4-динитрофенол, который также действует как химический разобщитель, аналогично UCP1, использовался для снижения веса в 1930-х годах. Однако его быстро прекратили, когда чрезмерное дозирование привело к побочным эффектам, включая гипертермию и смерть.[61] Агонисты β3, такие как CL316,243, также были разработаны и испытаны на людях. Однако использование таких лекарств оказалось в значительной степени безуспешным из-за нескольких проблем, в том числе из-за различной специфичности рецепторов видов и плохой пероральной биодоступности.[62]
Холод является основным регулятором процессов НДТ и вызывает потемнение ВАТ. Подрумянивание в ответ на хроническое воздействие холода хорошо задокументировано и является обратимым процессом. Исследование на мышах показало, что потемнение, вызванное холодом, может быть полностью обращено вспять за 21 день, при этом заметное снижение UCP1 наблюдается в течение 24-часового периода.[63] Исследование Rosenwald et al. показали, что, когда животные повторно подвергаются воздействию холода, те же адипоциты приобретают бежевый фенотип, что свидетельствует о сохранении бежевых адипоцитов.[64]
Регуляторы транскрипции, а также растущее число других факторов регулируют индукцию бежевого жира. Четыре регулятора транскрипции играют центральную роль в потемнении WAT и служат мишенями для многих молекул, которые, как известно, влияют на этот процесс.[65] К ним относятся гамма-рецепторы, активируемые пролифератором пероксисом. (PPARγ), PR домен, содержащий 16 (PRDM16 ),[66] Гамма-коактиватор рецептора, активируемого пролифератором пероксисом, 1 альфа (PGC-1α) и ранний фактор B-клеток-2 (EBF2).[67][68][69]
Список молекул, влияющих на потемнение, вырос прямо пропорционально популярности этой темы и постоянно расширяется по мере получения новых знаний. Среди этих молекул есть ирисин и фактор роста фибробластов 21 (FGF21 ), которые хорошо изучены и считаются важными регуляторами потемнения. Ирисин секретируется мышцами в ответ на упражнения и, как было показано, усиливает потемнение, воздействуя на бежевые преадипоциты.[70] FGF21, гормон, секретируемый в основном печенью, вызвал большой интерес после того, как был идентифицирован как мощный стимулятор поглощения глюкозы и регулятор потемнения благодаря его влиянию на PGC-1α.[61] Во время воздействия холода в нем повышается содержание BAT, и считается, что он способствует сопротивлению ожирению, вызванному диетой.[71] FGF21 также может секретироваться в ответ на упражнения и низкобелковую диету, хотя последнее не было тщательно исследовано.[72][73] Данные этих исследований показывают, что факторы окружающей среды, такие как диета и упражнения, могут быть важными медиаторами потемнения. У мышей было обнаружено, что зарождение может происходить за счет продукции пептидов метионин-энкефалин посредством врожденные лимфоидные клетки 2 типа в ответ на интерлейкин 33.[74]
Инструменты геномики и биоинформатики для изучения потемнения
Из-за сложной природы жировой ткани и растущего списка молекул, регулирующих потемнение, существует большой потенциал для использования биоинформатика инструменты для улучшения учебы в этой области. Исследования WAT-потемнения в значительной степени выиграли от достижений этих методов, поскольку бежевый жир быстро набирает популярность в качестве терапевтической мишени для лечения ожирения и диабета.
Микрочип ДНК это инструмент биоинформатики, используемый для одновременной количественной оценки уровней экспрессии различных генов, который широко используется при изучении жировой ткани. В одном из таких исследований использовался анализ микроматриц в сочетании с программным обеспечением Ingenuity IPA для изучения изменений экспрессии генов WAT и BAT, когда мышей подвергали воздействию температур 28 и 6 ° C.[75] Затем были идентифицированы наиболее значимые гены с повышенной и пониженной регуляцией, которые использовали для анализа дифференциально экспрессируемых путей. Было обнаружено, что многие из путей, активируемых в WAT после воздействия холода, также сильно экспрессируются в BAT, например окислительного фосфорилирования, метаболизм жирных кислот и метаболизм пирувата.[75] Это говорит о том, что некоторые из адипоцитов перешли на бежевый фенотип при 6 ° C. Mössenböck et al. также использовали анализ микрочипов, чтобы продемонстрировать, что инсулин дефицит подавляет дифференцировку бежевых адипоцитов, но не нарушает их способность к потемнению.[76] Эти два исследования демонстрируют возможность использования микроматрицы в изучении потемнения WAT.
Секвенирование РНК (РНК-Seq ) - мощный вычислительный инструмент, позволяющий количественно оценить экспрессию РНК для всех генов в образце. Включение RNA-Seq в исследования коричневого цвета имеет большую ценность, поскольку предлагает лучшую специфичность, чувствительность и более полный обзор экспрессии генов, чем другие методы. RNA-Seq использовался как в исследованиях на людях, так и на мышах в попытке охарактеризовать бежевые адипоциты в соответствии с профилями их экспрессии генов и идентифицировать потенциальные терапевтические молекулы, которые могут индуцировать бежевый фенотип. Одно из таких исследований использовало RNA-Seq для сравнения профилей экспрессии генов WAT дикого типа. (WT) мышей и мышей со сверхэкспрессией раннего B-клеточного фактора-2 (EBF2). WAT трансгенных животных проявлял генную программу бурого жира и снижал экспрессию WAT-специфического гена по сравнению с мышами WT.[77] Таким образом, EBF2 был идентифицирован как потенциальная терапевтическая молекула, способная вызвать заболевание.
Иммунопреципитация хроматина с секвенированием (ChIP-seq) это метод, используемый для определения сайтов связывания белков на ДНК и оценки гистон модификации. Этот инструмент позволил изучить эпигенетический регулирование потемнения и помогает выяснить механизмы, с помощью которых взаимодействия белок-ДНК стимулируют дифференцировку бежевых адипоцитов. Исследования ландшафтов хроматина бежевых адипоцитов показали, что адипогенез этих клеток является результатом образования клеточно-специфических ландшафтов хроматина, которые регулируют программу транскрипции и, в конечном итоге, контролируют дифференцировку. Используя ChIP-seq в сочетании с другими инструментами, недавние исследования выявили более 30 транскрипционных и эпигенетических факторов, которые влияют на развитие бежевых адипоцитов.[77]
Генетика
В гипотеза бережливого гена (также называемая гипотезой голода) утверждает, что в некоторых популяциях организм будет более эффективно удерживать жир в периоды изобилия, тем самым обеспечивая большую сопротивляемость голоданию в периоды нехватки пищи. Эта гипотеза, первоначально выдвинутая в контексте метаболизма глюкозы и инсулинорезистентности, была дискредитирована физическими антропологами, физиологами и исследователями. оригинальный сторонник идеи в отношении этого контекста, хотя, по словам его разработчика, он остается «таким же жизнеспособным, как когда [он был] впервые продвинут» в других контекстах.[78][79]
В 1995 г. Джеффри Фридман, в своей резиденции в Рокфеллеровский университет, вместе с Рудольф Лейбель, Дуглас Коулман и другие. открыл белок лептин чего не хватало мыши с генетическим ожирением.[80][81][82] Лептин вырабатывается в белой жировой ткани и сигнализирует гипоталамус. Когда уровень лептина падает, организм интерпретирует это как потерю энергии, и чувство голода усиливается. Мыши, которым не хватает этого белка, едят, пока они не станут в четыре раза больше своего обычного размера.
Лептин, однако, играет иную роль в ожирении, вызванном диетой, у грызунов и людей. Поскольку адипоциты вырабатывают лептин, уровень лептина повышается у людей с ожирением. Однако голод остается, а когда уровень лептина падает из-за потери веса, голод усиливается. Падение лептина лучше рассматривать как сигнал голода, чем повышение лептина как сытость сигнал.[83] Однако повышенный уровень лептина при ожирении известен как устойчивость к лептину. Изменения, которые происходят в гипоталамусе и приводят к резистентности к лептину при ожирении, в настоящее время находятся в центре внимания исследований ожирения.[84]
Генные дефекты в гене лептина (ob) редки при ожирении человека.[85] По состоянию на июль 2010 г.[Обновить]во всем мире было идентифицировано только 14 человек из пяти семей, несущих мутировавший ob ген (один из которых был первой идентифицированной причиной генетического ожирения у людей) - две семьи пакистанского происхождения, живущие в Великобритании, одна семья, живущая в Турции, одна в Египте и одна в Австрии[86][87][88][89][90]- и были обнаружены две другие семьи, несущие мутировавшие ob рецептор.[91][92] Другие были идентифицированы как генетически частично дефицитные по лептину, и у этих людей уровни лептина на нижнем конце нормального диапазона могут предсказать ожирение.[93]
Несколько мутации генов, связанных с меланокортины (используются в передаче сигналов мозга, связанных с аппетитом) и их рецепторы также были идентифицированы как вызывающие ожирение у большей части населения, чем мутации лептина.[94]
Физические свойства
Жировая ткань имеет плотность ~ 0,9 г / мл.[95] Таким образом, человек с большим количеством жировой ткани будет плавать легче, чем человек того же веса с большим количеством жировой ткани. мышечная ткань, так как мышечная ткань имеет плотность 1,06 г / мл.[96]
Измеритель жира в организме
А измеритель жира в организме широко доступный инструмент, используемый для измерения процентного содержания жира в организме человека. Разные измерители используют разные методы для определения соотношение телесного жира к весу. Они склонны занижать процентное содержание жира в организме.
В отличие от клинических инструментов, в одном относительно недорогом измерителе жира в организме используется принцип анализ биоэлектрического импеданса (BIA), чтобы определить процентное содержание жира в организме человека. Для этого счетчик проходит небольшой, безвредный, электрический ток через тело и измеряет сопротивление, затем использует информацию о весе, росте, возрасте и поле человека для расчета приблизительного значения процента жира в организме человека.Расчет измеряет общий объем воды в теле (безжировая ткань и мышцы содержат более высокий процент воды, чем жир) и оценивает процентное содержание жира на основе этой информации. Результат может колебаться на несколько процентов в зависимости от того, что было съедено и сколько воды было выпито перед анализом. Перед анализ биоэлектрического импеданса были разработаны машины, было много разных способов анализа состава тела, таких как кожная складка методы с использованием суппорты, подводное взвешивание, все тело плетизмография с вытеснением воздуха (ADP) и DXA.
Исследования на животных
В жировой (жировой) ткани CCR2 неполноценный мышей, увеличивается количество эозинофилы, большая альтернатива Макрофаги активация и склонность к типу 2 цитокин выражение. Более того, этот эффект был преувеличен, когда мыши стали тучный от диеты с высоким содержанием жиров.[97]
Галерея

Схематический разрез кожи (увеличен).

Белая жировая ткань в парафиновом срезе

Электронный прибор для измерения жира в организме
Смотрите также
- Белок, связанный с дифференцировкой жировой ткани
- Адипозопатия
- Апелин
- Анализ биоэлектрического импеданса - метод измерения процентного содержания жира в организме.
- Ворвань - очень толстая форма жировой ткани, встречающаяся у некоторых морских млекопитающих.
- Процент жира в организме
- Целлюлит
- Липолиз
- Липодистрофия
- Человеческий жир используется как лекарственное средство в традиционной медицине
- Ожирение
- Голодание
- Стеатоз (также называется жировым изменением, жировой дегенерацией или жировой дегенерацией)
- Стволовые клетки
- Подкожный жир
- Бариатрия
- Классификация ожирения
- Классификация детского ожирения
- EPODE Международная сеть, крупнейшая в мире сеть по профилактике ожирения
- World Fit Программа Олимпийского комитета США (USOC) и Ассоциации олимпийцев и паралимпийцев США (USOP).
- Ожирение и ходьба
- Социальная стигма ожирения
Рекомендации
- ^ а б c d Бирбрайр А., Чжан Т., Ван З.М., Месси М.Л., Эниколопов Г.Н., Минц А., Дельбоно О. (август 2013 г.). «Роль перицитов в регенерации скелетных мышц и накоплении жира». Стволовые клетки и развитие. 22 (16): 2298–314. Дои:10.1089 / scd.2012.0647. ЧВК 3730538. PMID 23517218.
- ^ Кершоу Е.Е., Флиер Дж.С. (июнь 2004 г.). «Жировая ткань как эндокринный орган». Журнал клинической эндокринологии и метаболизма. 89 (6): 2548–56. Дои:10.1210 / jc.2004-0395. PMID 15181022.
- ^ Cannon B, Nedergaard J (август 2008 г.). «Биология развития: Ни жир, ни плоть». Природа. 454 (7207): 947–48. Bibcode:2008Натура.454..947C. Дои:10.1038 / 454947a. PMID 18719573. S2CID 205040511.
- ^ Aarsland A, Chinkes D, Wolfe RR (июнь 1997 г.). «Синтез жира в печени и во всем теле у человека при перекармливании углеводов». Американский журнал клинического питания. 65 (6): 1774–82. Дои:10.1093 / ajcn / 65.6.1774. PMID 9174472.
- ^ Пруд CM (1998). Жиры жизни. Издательство Кембриджского университета. ISBN 978-0-521-63577-6.
- ^ Cinti S (июль 2005 г.). «Жировой орган». Простагландины, лейкотриены и незаменимые жирные кислоты. 73 (1): 9–15. Дои:10.1016 / j.plefa.2005.04.010. PMID 15936182.
- ^ Бахманов А.А., Reed DR, Tordoff MG, Price RA, Beauchamp GK (март 2001 г.). «Предпочтение питательных веществ и ожирение, вызванное диетой у мышей C57BL / 6ByJ и 129P3 / J». Физиология и поведение. 72 (4): 603–13. Дои:10.1016 / S0031-9384 (01) 00412-7. ЧВК 3341942. PMID 11282146.
- ^ Вирт, Альфред; Вабич, Мартин; Хаунер, Ганс (октябрь 2014 г.). «Профилактика и лечение ожирения». Deutsches Ärzteblatt International. 111 (42): 705–713. Дои:10.3238 / arztebl.2014.0705. ISSN 1866-0452. ЧВК 4233761. PMID 25385482.
- ^ Жир изнутри: выглядеть худым - недостаточно, Фиона Хейнс, About.com
- ^ а б «Абдоминальный жир и что с ним делать». Президент и научные сотрудники Гарвардского колледжа. Сентябрь 2005 г.
Висцеральный жир больше опасен для здоровья, чем подкожный жир
- ^ Нагай М., Комия Х., Мори Й., Охта Т., Касахара Й., Икеда Й. (май 2010 г.). «Оценка площади висцерального жира по многочастотному биоэлектрическому импедансу». Уход за диабетом. 33 (5): 1077–79. Дои:10.2337 / dc09-1099. ЧВК 2858179. PMID 20150289.
- ^ Монтегю, CT, O'Rahilly S (июнь 2000 г.). «Опасности полноты: причины и последствия висцерального ожирения». Сахарный диабет. 49 (6): 883–88. Дои:10.2337 / диабет.49.6.883. PMID 10866038.
- ^ Керн П.А., Ранганатан С., Ли К., Вуд Л., Ранганатан Г. (май 2001 г.). «Фактор некроза опухоли жировой ткани и экспрессия интерлейкина-6 при ожирении и инсулинорезистентности человека». Американский журнал физиологии. Эндокринология и метаболизм. 280 (5): E745–51. Дои:10.1152 / ajpendo.2001.280.5.e745. PMID 11287357. S2CID 24306481.
- ^ Маретт А (декабрь 2003 г.). «Молекулярные механизмы воспаления при инсулинорезистентности, связанной с ожирением». Международный журнал ожирения и связанных с ним нарушений обмена веществ. 27 Дополнение 3: S46–48. Дои:10.1038 / sj.ijo.0802500. PMID 14704744.
- ^ Мокдад А.Х., Форд Э.С., Боуман Б.А., Дитц У.Х., Виникор Ф., Бейлз В.С. и др. (Январь 2003 г.). «Распространенность ожирения, диабета и факторов риска для здоровья, связанных с ожирением, 2001 г.». JAMA. 289 (1): 76–79. Дои:10.1001 / jama.289.1.76. PMID 12503980.
- ^ Марески Х.С., Шарфман З., Зив-Баран Т., Гомори Дж.М., Копель Л., Таль С. (ноябрь 2015 г.). «Антропометрическая оценка объема жировой ткани шеи и дыхательных путей с использованием мультидетекторной компьютерной томографии: метод визуализации и связь с общей смертностью». Лекарство. 94 (45): e1991. Дои:10.1097 / MD.0000000000001991. ЧВК 4912280. PMID 26559286.
- ^ Браун Дж. К., Хархай М. О., Хархай М. Н. (2016). «Антропометрически предсказанные биомаркеры висцеральной жировой ткани и крови: поперечный анализ». Европейский журнал питания. 57 (1): 191–198. Дои:10.1007 / s00394-016-1308-8. ЧВК 5513780. PMID 27614626.
- ^ Браун Дж. К., Хархай М. О., Хархай М. Н. (2017). «Антропометрический прогноз висцеральной жировой ткани и смертность среди мужчин и женщин в третьем национальном обследовании здоровья и питания (NHANES III)». Американский журнал биологии человека. 29 (1): e22898. Дои:10.1002 / ajhb.22898. ЧВК 5241265. PMID 27427402.
- ^ «Уменьшить жир в брюшной полости». Архивировано из оригинал на 2011-09-28. Получено 2009-04-10.
Эстроген вызывает накопление жира в области таза, бедер, ягодиц и бедер (область таза).
- ^ «Беспокойство по поводу талии: превращение яблок в груши». Healthywomen.org. Архивировано из оригинал на 2009-06-09.
- ^ Исследователи считают, что недостаток эстрогена во время менопаузы играет роль в перемещении нашего жира на север. Видеть: Эндрюс, Мишель (01.12.2006). «Жирное дело». Yahoo Health. Женское здоровье. Архивировано из оригинал 15 марта 2007 г.
- ^ Ирвинг Б.А., Дэвис К.К., Брок Д.В., Велтман Д.Ю., Свифт Д., Барретт Е.Дж., Гэссер Г.А., Велтман А. (ноябрь 2008 г.). «Влияние интенсивности тренировок на висцеральный жир брюшной полости и состав тела». Медицина и наука в спорте и физических упражнениях. 40 (11): 1863–72. Дои:10.1249 / MSS.0b013e3181801d40. ЧВК 2730190. PMID 18845966.
- ^ Кокер Р.Х., Уильямс Р.Х., Кортебейн П.М., Салливан Д.Х., Эванс В.Дж. (август 2009 г.). «Влияние интенсивности упражнений на абдоминальный жир и адипонектин у пожилых людей». Метаболический синдром и связанные с ним расстройства. 7 (4): 363–68. Дои:10.1089 / мет.2008.0060. ЧВК 3135883. PMID 19196080.
- ^ Окавара К., Танака С., Миячи М., Исикава-Таката К., Табата I. (декабрь 2007 г.). «Доза-реакция между аэробными упражнениями и снижением висцерального жира: систематический обзор клинических испытаний». Международный журнал ожирения. 31 (12): 1786–97. Дои:10.1038 / sj.ijo.0803683. PMID 17637702.
- ^ Р, Росс; Дж. Риссанен (ноябрь 1994 г.). «Мобилизация висцеральной и подкожной жировой ткани в ответ на ограничение энергии и упражнения». Американский журнал клинического питания. 60 (5): 695–703. Дои:10.1093 / ajcn / 60.5.695. PMID 7942575. Получено 2020-06-05.
- ^ Мазурек Т., Чжан Л., Залевски А., Маннион Дж. Д., Диль Дж. Т., Арафат Х., Саров-Блат Л., О'Брайен С., Кейпер Е.А., Джонсон А.Г., Мартин Дж., Гольдштейн Б.Дж., Ши Й. и др. (Ноябрь 2003 г.). «Эпикардиальная жировая ткань человека является источником медиаторов воспаления». Тираж. 108 (20): 2460–66. Дои:10.1161 / 01.CIR.0000099542.57313.C5. PMID 14581396.
- ^ Пезешкиан М., Нури М., Наджарпур-Джаббари Х., Абольфати А., Дараби М., Дараби М., Шаакер М., Шахмохаммади Г. и др. (Апрель 2009 г.). «Жирнокислотный состав эпикардиальной и подкожной жировой ткани человека». Метаболический синдром и связанные с ним расстройства. 7 (2): 125–31. Дои:10.1089 / мет.2008.0056. PMID 19422139.
- ^ а б Hoehn K, Marieb EN (2008). Анатомия и физиология (3-е изд.). Сан-Франциско, Калифорния: Пирсон / Бенджамин Каммингс. ISBN 978-0-8053-0094-9.
- ^ Портер С.А., Массаро Дж.М., Хоффманн Ю., Васан Р.С., О'Доннел С.Дж., Фокс С.С. (июнь 2009 г.). "Подкожно-жировая клетчатка брюшной полости: защитное депо жира?". Уход за диабетом. 32 (6): 1068–75. Дои:10.2337 / dc08-2280. ЧВК 2681034. PMID 19244087.
- ^ «Жир на животе у женщин: убрать - и удержать - прочь». MayoClinic.com. 2013-06-08. Получено 2013-12-02.
- ^ Frayn, K. N .; Карпе, Ф .; Манолопулос, К. Н. (июнь 2010 г.). «Ягодично-бедренный жир как фактор, определяющий метаболическое здоровье». Международный журнал ожирения. 34 (6): 949–959. Дои:10.1038 / ijo.2009.286. ISSN 1476-5497. PMID 20065965.
- ^ а б Броди Д., Москрип V, Хатчеон Р. (март 1998 г.). «Измерение состава тела: обзор методов гидроденситометрии, антропометрии и импеданса». Питание. 14 (3): 296–310. Дои:10.1016 / S0899-9007 (97) 00474-7. PMID 9583375.
- ^ Девлин MJ, Cloutier AM, Thomas NA, Panus DA, Lotinun S, Pinz I, Baron R, Rosen CJ, Bouxsein ML (сентябрь 2010 г.). «Ограничение калорийности приводит к высокому ожирению костного мозга и низкой костной массе у растущих мышей». Журнал исследований костей и минералов. 25 (9): 2078–88. Дои:10.1002 / jbmr.82. ЧВК 3127399. PMID 20229598.
- ^ Cawthorn WP, Scheller EL, Parlee SD, Pham HA, Learman BS, Redshaw CM, Sulston RJ, Burr AA, Das AK, Simon BR, Mori H, Bree AJ, Schell B., Krishnan V, MacDougald OA (февраль 2016 г.). «Расширение жировой ткани костного мозга при ограничении калорийности связано с увеличением циркулирующих глюкокортикоидов, а не с гиполептинемией». Эндокринология. 157 (2): 508–21. Дои:10.1210 / en.2015-1477. ЧВК 4733126. PMID 26696121.
- ^ Бределла М.А., Фазели П.К., Миллер К.К., Мисра М., Торриани М., Томас Б.Дж., Гоми Р.Х., Розен С.Дж., Клибански А. (июнь 2009 г.). «Повышенное содержание жира в костном мозге при нервной анорексии». Журнал клинической эндокринологии и метаболизма. 94 (6): 2129–36. Дои:10.1210 / jc.2008-2532. ЧВК 2690416. PMID 19318450.
- ^ а б Стайнер М., Пагнотти Г.М., МакГрат К., Ву Х, Сен Б., Узер Дж., Се З., Зонг Х, Стайнер М.А., Рубин К.Т., Рубин Дж. (Август 2017 г.). «Упражнения уменьшают количество жировой ткани костного мозга за счет ß-окисления у бегущих мышей с ожирением». Журнал исследований костей и минералов. 32 (8): 1692–702. Дои:10.1002 / jbmr.3159. ЧВК 5550355. PMID 28436105.
- ^ Стайнер М., Пагнотти Г.М., Галиор К., Ву Х, Томпсон В.Р., Узер Дж., Сен Б., Се З., Хоровиц М.С., Стайнер М.А., Рубин С., Рубин Дж. (Август 2015 г.). «Регулировка физической нагрузки костного мозга при лечении агонистом PPARγ у самок мышей C57BL / 6». Эндокринология. 156 (8): 2753–61. Дои:10.1210 / en.2015-1213. ЧВК 4511140. PMID 26052898.
- ^ Стайнер М., Томпсон В. Р., Галиор К., Узер Г., Ву Х, Кадари С., Кейс N, Се З, Сен Б., Ромейн А., Пагнотти Г. М., Рубин К. Т., Стайнер М. А., Горовиц М. С., Рубин Дж. (Июль 2014 г.). «Накопление жира в костном мозге, ускоренное диетой с высоким содержанием жиров, подавляется упражнениями». Кость. 64: 39–46. Дои:10.1016 / j.bone.2014.03.044. ЧВК 4041820. PMID 24709686.
- ^ а б Снел М., Йонкер Дж. Т., Скунс Дж., Лэмб Х., де Роос А., Пийл Х., Смит Дж. В., Майндерс А. Э., Джазет И. М. (2012). «Внематочный жир и инсулинорезистентность: патофизиология и влияние диет и изменений образа жизни». Международный журнал эндокринологии. 2012: 1–18. Дои:10.1155/2012/983814. ЧВК 3366269. PMID 22675355.
- ^ Куры В., Виссерс Д., Хансен Д., Пеэтерс С., Гилен Дж., Ван Гал Л., Тэйманс Дж. (2017). «Влияние диеты или упражнений на эктопическое ожирение у детей и подростков с ожирением: систематический обзор и метаанализ». Обзоры ожирения. 18 (11): 1310–22. Дои:10.1111 / obr.12577. HDL:1942/24948. PMID 28913977. S2CID 10876113.
- ^ Курицы В., Тейман Дж., Корнелис Дж., Гилен Дж., Ван Гал Л., Виссерс Д. (2016). «Влияние вмешательств, связанных с образом жизни, на избыточное внематочное отложение жира, измеренное неинвазивными методами у взрослых с избыточным весом и ожирением: систематический обзор и метаанализ». Журнал физической активности и здоровья. 13 (6): 671–94. Дои:10.1123 / jpah.2015-0560. HDL:10067/1321600151162165141. PMID 26694194.
- ^ Томас, Лоретт В. (1962-04-07). «Химический состав жировой ткани человека и мышей». Ежеквартальный журнал экспериментальной физиологии и когнитивных медицинских наук. 47 (2): 179–188. Дои:10.1113 / expphysiol.1962.sp001589. ISSN 1469-445X. PMID 13920823.
- ^ Амитани, Мари; Асакава, Акихиро; Амитани, Харука; Инуи, Акио (2013). «Роль лептина в контроле оси инсулин-глюкоза». Границы неврологии. 7: 51. Дои:10.3389 / fnins.2013.00051. ISSN 1662-453X. ЧВК 3619125. PMID 23579596.
- ^ Дхаливал С.С., Велборн Т.А. (2009). «Центральное ожирение и многовариантный сердечно-сосудистый риск по оценкам прогнозов Фрамингема». Am J Cardiol. 103 (10): 1403–07. Дои:10.1016 / j.amjcard.2008.12.048. PMID 19427436.
- ^ Парк А (2008-08-08). «Толстобрюхие обезьяны подсказывают, почему стресс - отстой». Время. В архиве с оригинала от 20 декабря 2013 г.. Получено 2013-12-19.
- ^ Sugii S, Kida Y, Kawamura T, Suzuki J, Vassena R, Yin YQ и др. (Февраль 2010 г.). «Клетки, полученные из жировой ткани человека и мыши, поддерживают индукцию плюрипотентных стволовых клеток, не зависящую от питателя». Труды Национальной академии наук. 107 (8): 3558–63. Bibcode:2010ПНАС..107.3558С. Дои:10.1073 / pnas.0910172106. ЧВК 2840462. PMID 20133714.
- ^ а б Ацмон Дж., Ян Х. М., Музумдар Р., Ма Х. Х., Габриэли И., Барзилай Н. (ноябрь 2002 г.). «Дифференциальная экспрессия генов между депо висцерального и подкожного жира». Гормоны и метаболические исследования. 34 (11–12): 622–28. Дои:10.1055 / с-2002-38250. PMID 12660871.
- ^ Baglioni S, Cantini G, Poli G, Francalanci M, Squecco R, Di Franco A, Borgogni E, Frontera S, Nesi G, Liotta F, Lucchese M, Perigli G, Francini F, Forti G, Serio M, Luconi M (4 Май 2012 г.). «Функциональные различия подушечек висцерального и подкожного жира происходят из-за различий в стволовых клетках жировой ткани». PLOS ONE. 7 (5): e36569. Bibcode:2012PLoSO ... 736569B. Дои:10.1371 / journal.pone.0036569. ЧВК 3344924. PMID 22574183.
- ^ Руссо В., Ю. К., Белливо П., Гамильтон А., Флинн Л. Е. (февраль 2014 г.). «Сравнение стволовых клеток, полученных из жировой ткани человека, выделенных из подкожных, сальниковых и внутригрудных депо жировой ткани для регенеративных применений». Трансляционная медицина стволовых клеток. 3 (2): 206–17. Дои:10.5966 / sctm.2013-0125. ЧВК 3925056. PMID 24361924.
- ^ Lempesis, Ioannis G .; Мейель, Ренс Л. Дж. Ван; Manolopoulos, Konstantinos N .; Гуссенс, Гийс Х. (2019). «Оксигенация жировой ткани: взгляд человека». Acta Physiologica. 0 (1): e13298. Дои:10.1111 / apha.13298. ISSN 1748-1716. ЧВК 6916558. PMID 31077538.
- ^ Стокко, Карлос (январь 2012 г.). «Тканевая физиология и патология ароматазы». Стероиды. 77 (1–2): 27–35. Дои:10.1016 / j.steroids.2011.10.013. ISSN 0039-128X. ЧВК 3286233. PMID 22108547.
- ^ Лён М., Дубровска Г., Лаутербах Б., Люфт ФК, Голлаш М., Шарма А.М. (июль 2002 г.). «Периадвентициальный жир выделяет фактор расслабления сосудов». Журнал FASEB. 16 (9): 1057–63. Дои:10.1096 / fj.02-0024com. PMID 12087067. S2CID 902537.
- ^ а б Cannon B, Nedergaard J (январь 2004 г.). «Коричневая жировая ткань: функция и физиологическое значение». Физиологические обзоры. 84 (1): 277–359. Дои:10.1152 / физрев.00015.2003. PMID 14715917. S2CID 14289041.
- ^ Бусиелло Р.А., Саварезе С., Ломбарди А. (2015). "Митохондриальные разобщающие белки и энергетический метаболизм". Границы физиологии. 6 (36): 36. Дои:10.3389 / fphys.2015.00036. ЧВК 4322621. PMID 25713540.
- ^ Федоренко А., Лишко П.В., Киричок Ю. (октябрь 2012 г.). «Механизм зависимого от жирных кислот разобщения UCP1 в митохондриях бурого жира». Клетка. 151 (2): 400–13. Дои:10.1016 / j.cell.2012.09.010. ЧВК 3782081. PMID 23063128.
- ^ Аззу Ви, бренд-MD (май 2010 г.). «Двухпозиционные переключатели митохондриальных разобщающих белков». Тенденции в биохимических науках. 35 (5): 298–307. Дои:10.1016 / j.tibs.2009.11.001. ЧВК 3640847. PMID 20006514.
- ^ Недергаард Дж., Бенгтссон Т., Пушка Б (август 2007 г.). «Неожиданные доказательства активной коричневой жировой ткани у взрослых людей». Американский журнал физиологии. Эндокринология и метаболизм. 293 (2): E444–52. Дои:10.1152 / ajpendo.00691.2006. PMID 17473055. S2CID 230947.
- ^ Виртанен К.А., Лиделл М.Э., Орава Дж., Хеглинд М., Вестергрен Р., Ниеми Т. и др. (Апрель 2009 г.). «Функциональная коричневая жировая ткань у здоровых взрослых». Медицинский журнал Новой Англии. 360 (15): 1518–25. Дои:10.1056 / NEJMoa0808949. PMID 19357407.
- ^ van Marken Lichtenbelt WD, Vanhommerig JW, Smulders NM, Drossaerts JM, Kemerink GJ, Bouvy ND, et al. (Апрель 2009 г.). «Холодная активированная коричневая жировая ткань у здоровых мужчин». Медицинский журнал Новой Англии. 360 (15): 1500–08. Дои:10.1056 / NEJMoa0808718. PMID 19357405. S2CID 477352.
- ^ Сайпесс AM, Lehman S, Williams G, Tal I, Rodman D, Goldfine AB и др. (Апрель 2009 г.). «Идентификация и важность коричневой жировой ткани у взрослых людей». Медицинский журнал Новой Англии. 360 (15): 1509–17. Дои:10.1056 / NEJMoa0810780. ЧВК 2859951. PMID 19357406.
- ^ а б c Хармс М., Сил П. (октябрь 2013 г.). «Коричневый и бежевый жир: развитие, функции и терапевтический потенциал». Природа Медицина. 19 (10): 1252–63. Дои:10,1038 / нм. 3361. PMID 24100998.
- ^ Сайпесс AM, Кан CR (апрель 2010 г.). «Бурый жир как средство от ожирения и диабета». Текущее мнение в области эндокринологии, диабета и ожирения. 17 (2): 143–49. Дои:10.1097 / MED.0b013e328337a81f. ЧВК 3593105. PMID 20160646.
- ^ Gospodarska E, Nowialis P, Kozak LP (март 2015 г.). «Митохондриальный оборот: фенотип, отличающий коричневые адипоциты от межлопаточной коричневой жировой ткани и белой жировой ткани». Журнал биологической химии. 290 (13): 8243–55. Дои:10.1074 / jbc.M115.637785. ЧВК 4375480. PMID 25645913.
- ^ Розенвальд М., Пердикари А., Рюликке Т., Вольфрум С. (июнь 2013 г.). «Двунаправленное взаимопревращение британских и белых адипоцитов». Природа клеточной биологии. 15 (6): 659–67. Дои:10.1038 / ncb2740. PMID 23624403. S2CID 2842953.
- ^ Ло КА, Сун Л. (сентябрь 2013 г.). «Превращение WAT в BAT: обзор регуляторов, контролирующих потемнение белых адипоцитов». Отчеты по бионауке. 33 (5): 711–19. Дои:10.1042 / BSR20130046. ЧВК 3764508. PMID 23895241.
- ^ Хармс MJ, Ishibashi J, Wang W, Lim HW, Goyama S, Sato T, Kurokawa M, Won KJ, Seale P (апрель 2014 г.). «Prdm16 необходим для поддержания идентичности и функции коричневых адипоцитов у взрослых мышей». Клеточный метаболизм. 19 (4): 593–604. Дои:10.1016 / j.cmet.2014.03.007. ЧВК 4012340. PMID 24703692.
- ^ Ван В., Киссиг М., Раджакумари С., Хуанг Л., Лим Х.В., Вон К.Дж., Сил П. (октябрь 2014 г.). «Ebf2 - селективный маркер коричневых и бежевых адипогенных клеток-предшественников». Труды Национальной академии наук. 111 (40): 14466–71. Bibcode:2014PNAS..11114466W. Дои:10.1073 / pnas.1412685111. ЧВК 4209986. PMID 25197048.
- ^ Киссиг М., Шапира С.Н., Сил П. (июнь 2016 г.). «SnapShot: термогенез коричневого и бежевого жира». Клетка. 166 (1): 258–258.e1. Дои:10.1016 / j.cell.2016.06.038. ЧВК 5478388. PMID 27368105.
- ^ Шапира С.Н., Лим Х.В., Раджакумари С., Сакерс А.П., Ишибаши Дж., Хармс М.Дж., Вон К.Дж., Сил П. (апрель 2017 г.). «EBF2 транскрипционно регулирует коричневый адипогенез посредством считывателя гистонов DPF3 и комплекса ремоделирования хроматина BAF». Гены и развитие. 31 (7): 660–73. Дои:10.1101 / gad.294405.116. ЧВК 5411707. PMID 28428261.
- ^ Boström P, Wu J, Jedrychowski MP, Korde A, Ye L, Lo JC, Rasbach KA, Boström EA, Choi JH, Long JZ, Kajimura S, Zingaretti MC, Vind BF, Tu H, Cinti S, Højlund K, Gygi SP , Шпигельман Б.М. (январь 2012 г.). «PGC1-α-зависимый миокин, который стимулирует развитие белого жира, подобное бурому жиру, и термогенез». Природа. 481 (7382): 463–68. Bibcode:2012Натура.481..463Б. Дои:10.1038 / природа10777. ЧВК 3522098. PMID 22237023.
- ^ Охта Х, Ито Н (2014). «Роль FGF как адипокинов в развитии, ремоделировании и метаболизме жировой ткани». Границы эндокринологии. 5 (18): 18. Дои:10.3389 / fendo.2014.00018. ЧВК 3932445. PMID 24605108.
- ^ Фенцл А., Кифер Ф.В. (июль 2014 г.). «Коричневая жировая ткань и термогенез». Молекулярная биология гормонов и клинические исследования. 19 (1): 25–37. Дои:10.1515 / hmbci-2014-0022. PMID 25390014. S2CID 35008082.
- ^ Laeger T, Henagan TM, Albarado DC, Редман Л.М., Брей Г.А., Ноланд Р.К., Мюнцберг Х., Хатсон С.М., Gettys TW, Шварц М.В., Моррисон С.Д. (сентябрь 2014 г.). «FGF21 - это эндокринный сигнал ограничения белка». Журнал клинических исследований. 124 (9): 3913–22. Дои:10.1172 / JCI74915. ЧВК 4153701. PMID 25133427.
- ^ Брестофф, Джонатан Р .; Ким, Брайан С .; Саенс, Стивен А .; Стайн, Рэйчел Р .; Монтичелли, Лорел А .; Зонненберг, Грегори Ф .; Том, Джозеф Дж .; Фарбер, Донна Л .; Лютфи, Кабирулла (12 марта 2015 г.). «Врожденные лимфоидные клетки группы 2 способствуют образованию белой жировой ткани и ограничивают ожирение». Природа. 519 (7542): 242–246. Bibcode:2015Натура.519..242Б. Дои:10.1038 / природа14115. ISSN 1476-4687. ЧВК 4447235. PMID 25533952.
- ^ а б Rosell M, Kaforou M, Frontini A, Okolo A, Chan YW, Nikolopoulou E, Millership S, Fenech ME, MacIntyre D, Turner JO, Moore JD, Blackburn E, Gullick WJ, Cinti S, Montana G, Parker MG, Christian M (Апрель 2014 г.). «Коричневая и белая жировая ткань: внутренние различия в экспрессии генов и реакции на воздействие холода у мышей». Американский журнал физиологии. Эндокринология и метаболизм. 306 (8): E945–64. Дои:10.1152 / ajpendo.00473.2013. ЧВК 3989735. PMID 24549398.
- ^ Инагаки Т., Сакаи Дж., Каджимура С. (август 2016 г.). «Транскрипционный и эпигенетический контроль судьбы и функции коричневых и бежевых жировых клеток». Обзоры природы Молекулярная клеточная биология. 17 (8): 480–95. Дои:10.1038 / nrm.2016.62. ЧВК 4956538. PMID 27251423.
- ^ а б Стин Р.Р., Шапира С.Н., Лим Х.В., Ишибаши Дж., Хармс М., Вон К.Дж., Сил П. (январь 2016 г.). «EBF2 способствует привлечению бежевых адипоцитов в белой жировой ткани». Молекулярный метаболизм. 5 (1): 57–65. Дои:10.1016 / j.molmet.2015.11.001. ЧВК 4703852. PMID 26844207.
- ^ Спикер JR (2007). «Генетика ожирения: пять фундаментальных проблем с гипотезой голода». В Fantuzzi G, Mazzone T (ред.). Жировая ткань и адипокины в здоровье и болезнях. Питание и здоровье. Humana Press. С. 221–236. Дои:10.1007/978-1-59745-370-7_17. ISBN 978-1-58829-721-1.
- ^ Нил СП (1989). «Изучение естественного отбора в примитивных и цивилизованных популяциях человека. 1958». Человеческая биология. 61 (5–6): 781–810, обсуждение 811–23. PMID 2699601.
- ^ Shell E (1 января 2002 г.). «Глава 4: На передовой». Голодный ген: внутренняя история индустрии ожирения. Atlantic Monthly Press. ISBN 978-1-4223-5243-4.
- ^ Shell E (1 января 2002 г.). «Глава 5: Голод». Голодный ген: внутренняя история индустрии ожирения. Atlantic Monthly Press. ISBN 978-1-4223-5243-4.
- ^ Пеллеймонтер М.А., Каллен М.Дж., Бейкер МБ, Хехт Р., Винтерс Д., Бун Т. и др. (Июль 1995 г.). «Влияние продукта гена ожирения на регуляцию массы тела у мышей ob / ob». Наука. 269 (5223): 540–43. Bibcode:1995Научный ... 269..540P. Дои:10.1126 / science.7624776. PMID 7624776.
- ^ Равуссин Э., Смит С.Р. (2013). «Глава 11: Роль адипоцитов в метаболизме и эндокринной функции». В Weir GC, Jameson JL, De Groot LJ (ред.). Эндокринология для взрослых и детей. Сахарный диабет и ожирение (6-е изд.). Elsevier Health Sciences. ISBN 978-0-323-22154-2.[страница нужна ]
- ^ Моррис Д.Л., Руи Л. (декабрь 2009 г.). «Последние достижения в понимании передачи сигналов лептина и устойчивости к лептину». Американский журнал физиологии. Эндокринология и метаболизм. 297 (6): E1247–59. Дои:10.1152 / ajpendo.00274.2009. ЧВК 2793049. PMID 19724019.
- ^ Карлссон Б., Линделл К., Габриэльссон Б., Карлссон С., Бьярнасон Р., Вестфаль О. и др. (Январь 1997 г.). «Дефекты генов ожирения (ob) редки при ожирении у человека». Исследование ожирения. 5 (1): 30–35. Дои:10.1002 / j.1550-8528.1997.tb00280.x. PMID 9061713.
- ^ Montague CT, Farooqi IS, Whitehead JP, Soos MA, Rau H, Wareham NJ, Sewter CP, Digby JE, Mohammed SN, Hurst JA, Cheetham CH, Earley AR, Barnett AH, Prins JB, O'Rahilly S (июнь 1997 г.) . «Врожденная недостаточность лептина у людей связана с тяжелым ранним началом ожирения». Природа. 387 (6636): 903–8. Bibcode:1997Натура.387..903М. Дои:10.1038/43185. PMID 9202122. S2CID 205032762.
- ^ Стробель А., Иссад Т., Камоин Л., Озата М., Стросберг А.Д. (март 1998 г.). «Миссенс-мутация лептина, связанная с гипогонадизмом и патологическим ожирением». Природа Генетика. 18 (3): 213–15. Дои:10.1038 / ng0398-213. PMID 9500540. S2CID 36920931.
- ^ Гибсон В.Т., Фаруки И.С., Моро М., ДеПаоли А.М., Лоуренс Э., О'Рахилли С., Трассел Р.А. (октябрь 2004 г.). «Врожденный дефицит лептина из-за гомозиготности по мутации Delta133G: отчет о другом случае и оценка ответа на четырехлетнюю терапию лептином». Журнал клинической эндокринологии и метаболизма. 89 (10): 4821–26. Дои:10.1210 / jc.2004-0376. PMID 15472169.
- ^ Мазен И., Эль-Гаммал М., Абдель-Хамид М., Амр К. (август 2009 г.). «Новая гомозиготная миссенс-мутация гена лептина (N103K) у пациента из Египта с ожирением». Молекулярная генетика и метаболизм. 97 (4): 305–08. Дои:10.1016 / j.ymgme.2009.04.002. PMID 19427251.
- ^ Fischer-Posovszky P, von Schnurbein J, Moepps B, Lahr G, Strauss G, Barth TF, Kassubek J, Mühleder H, Möller P, Debatin KM, Gierschik P, Wabitsch M (июнь 2010 г.). «Новая миссенс-мутация в гене лептина вызывает умеренное ожирение и гипогонадизм, не влияя на реакцию Т-клеток». Журнал клинической эндокринологии и метаболизма. 95 (6): 2836–40. Дои:10.1210 / jc.2009-2466. PMID 20382689.
- ^ Клеман К., Вайсс С., Лахлу Н., Каброл С., Пеллу В., Кассуто Д., Гурмелен М., Дина С., Шамбаз Дж., Лакорте Дж. М., Басдеван А., Бугнер П., Лебук И., Фрогель П., Ги-Гран Б. (1998). «Мутация в гене рецептора лептина человека вызывает ожирение и дисфункцию гипофиза». Природа. 392 (6674): 398–401. Bibcode:1998Натура.392..398C. Дои:10.1038/32911. PMID 9537324. S2CID 4400661.
- ^ Панков Ю.А. (1999). «Жировая ткань как эндокринный орган, регулирующий рост, половое созревание и другие физиологические функции». Биохимия. Биохимия. 64 (6): 601–09. PMID 10395972.
- ^ Фаруки И.С., Кио Дж. М., Камат С., Джонс С., Гибсон В. Т., Трассел Р., Джебб С. А., Губ Г. Ю., О'Рахилли С. (ноябрь 2001 г.). «Частичная лептиновая недостаточность и ожирение человека». Природа. 414 (6859): 34–35. Bibcode:2001Натура 414 ... 34F. Дои:10.1038/35102112. PMID 11689931. S2CID 4344492.
- ^ Фаруки И.С., О'Рахилли С. (октябрь 2008 г.). «Мутации лигандов и рецепторов лептин-меланокортинового пути, приводящие к ожирению». Природа Клиническая практика Эндокринология и метаболизм. 4 (10): 569–77. Дои:10.1038 / ncpendmet0966. PMID 18779842. S2CID 13946212.
- ^ Фарвид М.С., Нг Т.В., Чан Д.С., Барретт PH, Уоттс Г.Ф. (июль 2005 г.). «Связь адипонектина и резистина с отделами жировой ткани, инсулинорезистентностью и дислипидемией». Диабет, ожирение и метаболизм. 7 (4): 406–13. Дои:10.1111 / j.1463-1326.2004.00410.x. PMID 15955127. S2CID 46736884.(требуется регистрация)
- ^ Урбанчек М.Г., Пикен Е.Б., Каллиайнен Л.К., Кузон В.М. (май 2001 г.). «Недостаток удельной силы в скелетных мышцах старых крыс частично объясняется наличием денервированных мышечных волокон». Журналы геронтологии. Серия A, Биологические и медицинские науки. 56 (5): B191–97. Дои:10.1093 / gerona / 56.5.B191. PMID 11320099.
- ^ Bolus WR, Gutierrez DA, Kennedy AJ, Anderson-Baucum EK, Hasty AH (октябрь 2015 г.). «Дефицит CCR2 приводит к увеличению эозинофилов, альтернативной активации макрофагов и экспрессии цитокинов 2 типа в жировой ткани». Журнал биологии лейкоцитов. 98 (4): 467–77. Дои:10.1189 / jlb.3HI0115-018R. ЧВК 4763864. PMID 25934927. Архивировано из оригинал на 2017-05-09. Получено 2016-09-08.
дальнейшее чтение
- MeSH A10.165.114
- Сток MJ, Cinti S (2003). «Жировая ткань / структура и функция коричневой жировой ткани». Энциклопедия пищевых наук и питания. С. 29–34. Дои:10.1016 / B0-12-227055-X / 00008-0. ISBN 978-0-12-227055-0.
- Вернон RG, Флинт DJ (2003). «Жировая ткань / Структура и функция белой жировой ткани». Энциклопедия пищевых наук и питания. С. 23–29. Дои:10.1016 / B0-12-227055-X / 00007-9. ISBN 978-0-12-227055-0.