Эмбриональные стволовые клетки - Embryonic stem cell


Эмбриональные стволовые клетки (ES клетки или Регуляторы) находятся плюрипотентный стволовые клетки полученный из внутренняя клеточная масса из бластоциста, ранняя предварительнаяимплантация эмбрион.[1][2] Человек эмбрионы достичь бластоциста этап 4–5 дней после оплодотворение, при этом они состоят из 50–150 клеток. Изоляция эмбриобласт, или внутренняя клеточная масса (ICM) приводит к разрушению бластоцисты, процессу что поднимает этические вопросы, включая вопрос о том, должны ли эмбрионы на предимплантационной стадии иметь те же моральные соображения, что и эмбрионы на постимплантационной стадии развития.[3][4]
В настоящее время исследователи уделяют большое внимание терапевтическому потенциалу эмбриональных стволовых клеток, при этом клиническое использование является целью многих лабораторий.[5] Возможные варианты использования включают лечение сахарный диабет и сердечное заболевание.[5] Клетки изучаются для использования в качестве клинических методов лечения, моделей генетические нарушения и восстановление клеток / ДНК. Однако побочные эффекты в исследованиях и клинических процессах, такие как опухоли и нежелательные иммунные ответы также поступали сообщения.[6]
Характеристики
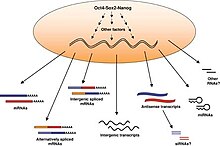
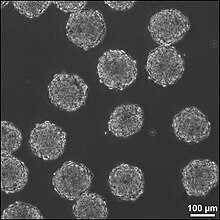
Эмбриональные стволовые клетки (ЭСК), происходящие на стадии бластоцисты ранних эмбрионов млекопитающих, отличаются своей способностью дифференцироваться в любой тип эмбриональных клеток и своей способностью к самообновлению. Именно эти качества делают их ценными в научной и медицинской областях. ESC имеют нормальный кариотип, поддерживать высокий теломераза активности и демонстрируют замечательные долгосрочные пролиферативный потенциал.[7]
Плюрипотентный
Эмбриональные стволовые клетки внутренней клеточной массы плюрипотентный, что означает, что они могут различать для создания примитивной эктодермы, которая в конечном итоге дифференцируется во время гаструляция во все производные от трех основных ростковые отростки: эктодерма, энтодерма, и мезодерма. Эти зародышевые листки производят каждый из более чем 220 типы клеток в теле взрослого человека. При подаче соответствующих сигналов ESC первоначально формируют клетки-предшественники которые впоследствии дифференцируются в желаемые типы клеток. Плюрипотентность отличает эмбриональные стволовые клетки от взрослые стволовые клетки, которые мультипотентный и может производить только ограниченное количество типов клеток.
Самостоятельное обновление и ремонт конструкции
В определенных условиях эмбриональные стволовые клетки способны бесконечно самообновляться в недифференцированном состоянии. Условия самообновления должны предотвращать слипание клеток и поддерживать среду, которая поддерживает неспециализированное состояние.[8] Обычно это делается в лаборатории со средами, содержащими сыворотка и фактор ингибирования лейкемии или бессывороточные питательные добавки с двумя ингибиторами («2i»), Ингибитор МЕК PD03259010 и Ингибитор ГСК-3 CHIR99021.[9]
Рост
ESC делятся очень часто из-за укороченного Фаза G1 в их клеточный цикл. Быстрое деление клеток позволяет клеткам быстро расти в количестве, но не в размере, что важно для раннего развития эмбриона. В ESCs, циклин А и циклин E белки, участвующие в Переход G1 / S всегда выражены на высоком уровне.[10] Циклинзависимые киназы такие как CDK2 которые способствуют развитию клеточного цикла, являются сверхактивными, отчасти из-за подавления их ингибиторов.[11] Белки ретинобластомы которые препятствуют фактор транскрипции E2F пока ячейка не будет готова войти Фаза S гиперфосфорилируются и инактивируются в ESC, что приводит к постоянной экспрессии генов пролиферации.[10] Эти изменения приводят к ускорению циклов деления клеток. Хотя укороченная фаза G1 была связана с поддержанием плюрипотентности,[12] ESC, выращенные в бессывороточных условиях 2i, действительно экспрессируют гипофосфорилированные активные белки ретинобластомы и имеют удлиненную фазу G1.[13] Несмотря на это различие в клеточном цикле по сравнению с ESC, выращенными в среде, содержащей сыворотку, эти клетки имеют сходные плюрипотентные характеристики.[14] Факторы плюрипотентности 4 октября и Наног играют роль в транскрипционной регуляции клеточного цикла ESC.[15][16]
Использует
Благодаря своей пластичности и потенциально неограниченной способности к самообновлению эмбриональные лечение стволовыми клетками были предложены для регенеративной медицины и замены тканей после травм или болезней. Плюрипотентные стволовые клетки показали себя многообещающими при лечении ряда различных состояний, включая, помимо прочего: травмы спинного мозга, возрастная дегенерация желтого пятна, сахарный диабет, нейродегенеративные расстройства (такие как болезнь Паркинсона ), СПИД, так далее.[17] В дополнение к их потенциалу в регенеративной медицине, эмбриональные стволовые клетки представляют собой возможный альтернативный источник тканей / органов, который служит возможным решением дилеммы нехватки доноров. Однако вокруг этого есть некоторые этические противоречия (см. Этические дебаты раздел ниже). Помимо этих применений, ESC также могут использоваться для исследований в области раннего развития человека, определенных генетических заболеваний и in vitro токсикология тестирование.[7]
Утилизации
Согласно статье 2002 г. PNAS «Эмбриональные стволовые клетки человека обладают потенциалом дифференцироваться в различные типы клеток и, таким образом, могут быть полезны в качестве источника клеток для трансплантации или тканевой инженерии».[18]
Однако эмбриональные стволовые клетки не ограничиваются клеточной / тканевой инженерией.
Терапия замещения клеток
Текущие исследования сосредоточены на дифференциации ESC на различные типы клеток для последующего использования в качестве терапии замещения клеток (CRT). Некоторые из типов клеток, которые уже разработаны или разрабатываются в настоящее время, включают: кардиомиоциты (СМ), нейроны, гепатоциты, Костный мозг клетки островок клетки и эндотелиальный клетки.[19] Однако получение таких типов клеток из ESC не обходится без препятствий, поэтому текущие исследования сосредоточены на преодолении этих барьеров. Напр., Ведутся исследования, чтобы дифференцировать ESC в тканеспецифичные CM и искоренить их незрелые свойства, которые отличают их от взрослых CM.[20]
Клинический потенциал
- Исследователи дифференцировали ESC в клетки, продуцирующие дофамин, в надежде, что эти нейроны могут быть использованы при лечении болезни Паркинсона.[21][22]
- ESC были дифференцированы на естественные клетки-киллеры (NK) и костная ткань.[23]
- В настоящее время проводятся исследования с участием ЭСК, чтобы предложить альтернативное лечение диабета. Например, D’Amour и другие. смогли дифференцировать ESC в клетки, продуцирующие инсулин[24] и исследователи в Гарвардский университет были способны производить большое количество панкреатических бета-клетки от ES.[25]
- Статья опубликована в Европейский журнал сердца описывает трансляционный процесс создания кардиальных клеток-предшественников, полученных из человеческих эмбриональных стволовых клеток, которые будут использоваться в клинических испытаниях пациентов с тяжелой сердечной недостаточностью.[26]
Открытие наркотиков
Помимо того, что они являются важной альтернативой трансплантации органов, ESC также используются в области токсикологии и в качестве клеточных экранов для выявления новых химических соединений (NCE), которые могут быть разработаны как низкомолекулярные препараты. Исследования показали, что кардиомиоциты, полученные из ESC, проверены на моделях in vitro для тестирования лекарственного ответа и прогнозирования профилей токсичности.[19] Было показано, что кардиомиоциты, полученные из ES, реагируют на фармакологические стимулы и, следовательно, могут использоваться для оценки кардиотоксичности, например Торсад де Пуант.[27]
Гепатоциты, полученные из ESC, также являются полезными моделями, которые можно использовать на доклинических этапах открытия лекарств. Однако оказалось, что развитие гепатоцитов из ЭСК является сложной задачей, и это препятствует возможности тестирования метаболизма лекарств. Таким образом, текущие исследования сосредоточены на создании полностью функциональных гепатоцитов, полученных из ESC, со стабильной ферментативной активностью фазы I и II.[28]
Модели генетического расстройства
Несколько новых исследований начали рассматривать концепцию моделирования генетических нарушений с помощью эмбриональных стволовых клеток. Либо путем генетических манипуляций с клетками, либо, в последнее время, путем получения линий пораженных клеток, идентифицированных с помощью пренатальной генетической диагностики (ПГД), моделирование генетических нарушений - это то, что было достигнуто с помощью стволовых клеток. Этот подход может оказаться полезным при изучении таких расстройств, как: Синдром ломкой Х-хромосомы, Кистозный фиброз, и другие генетические заболевания, не имеющие надежной модельной системы.
Юрий Верлинский, русско-американский медицинский исследователь кто специализировался на эмбрион и сотовая связь генетика (генетический цитология ), развитый пренатальная диагностика методы тестирования для определения генетических и хромосомные нарушения на полтора месяца раньше стандартного амниоцентез. В настоящее время эти методы используются многими беременными женщинами и потенциальными родителями, особенно парами, у которых в анамнезе есть генетические аномалии или где женщина старше 35 лет (когда риск генетически связанных заболеваний выше). Кроме того, позволяя родителям выбирать эмбрион без генетических нарушений, они могут спасти жизни братьев и сестер, у которых уже были подобные расстройства и заболевания, с использованием клеток потомства, свободного от болезней.[29]
Ремонт повреждений ДНК
Дифференцированные соматические клетки и ES-клетки используют разные стратегии для борьбы с повреждениями ДНК. Например, фибробласты крайней плоти человека, один из типов соматических клеток, используют негомологичное соединение концов (NHEJ), склонный к ошибкам процесс репарации ДНК, как основной путь репарации двухцепочечных разрывов (DSB) на всех стадиях клеточного цикла.[30] Из-за своей склонности к ошибкам NHEJ имеет тенденцию вызывать мутации в клональных потомках клетки.
ES-клетки используют другую стратегию для работы с DSB.[31] Поскольку ES-клетки дают начало всем типам клеток организма, включая клетки зародышевой линии, мутации, возникающие в ES-клетках из-за неправильной репарации ДНК, представляют собой более серьезную проблему, чем в дифференцированных соматических клетках. Следовательно, в ES-клетках необходимы надежные механизмы для точного восстановления повреждений ДНК и, если восстановление не удается, для удаления этих клеток с не восстановленными повреждениями ДНК. Таким образом, мышиные ES-клетки преимущественно используют высокую точность воспроизведения. гомологичная рекомбинационная репарация (HRR) для ремонта DSB.[31] Этот тип восстановления зависит от взаимодействия двух сестринских хромосом.[требуется проверка ] образуются во время фазы S и присутствуют вместе во время фазы G2 клеточного цикла. HRR может точно восстанавливать DSB в одной сестринской хромосоме, используя неповрежденную информацию из другой сестринской хромосомы. Клетки в фазе G1 клеточного цикла (то есть после метафазы / деления клетки, но до следующего раунда репликации) имеют только одну копию каждой хромосомы (т.е. сестринские хромосомы отсутствуют). ES-клетки мыши не имеют контрольной точки G1 и не подвергаются аресту клеточного цикла при повреждении ДНК.[32] Скорее они подвергаются запрограммированной гибели клеток (апоптозу) в ответ на повреждение ДНК.[33] Апоптоз можно использовать в качестве безотказной стратегии для удаления клеток с не восстановленными повреждениями ДНК, чтобы избежать мутации и развития рака.[34] В соответствии с этой стратегией, мышиные ES стволовые клетки имеют частоту мутаций примерно в 100 раз ниже, чем изогенные соматические клетки мыши.[35]
Клинические испытания
23 января 2009 г. состоялась фаза I клинических испытаний трансплантации олигодендроциты (тип клеток головного и спинного мозга), полученные из человеческих ES-клеток в травма спинного мозга лица получили одобрение от Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), что стало первым в мире испытанием ES-клеток на людях.[36] Исследование, приведшее к этому научному прогрессу, было проведено Хансом Кирстедом и его коллегами из Калифорнийский университет в Ирвине и поддерживается Корпорация Geron из Менло-Парк, Калифорния, основан Майкл Д. Уэст, Кандидат наук. Предыдущий эксперимент показал улучшение локомоторного восстановления у крыс с повреждением спинного мозга после 7-дневной отсроченной трансплантации человеческих ES-клеток, которые были перенесены в олигодендроцитарный клон.[37] Клиническое исследование фазы I было разработано для включения от восьми до десяти людей, страдающих параличом нижних конечностей, у которых были травмы не ранее, чем за две недели до начала исследования, поскольку клетки должны быть введены до того, как рубцовая ткань сможет сформироваться. Исследователи подчеркнули, что инъекции не должны были полностью вылечить пациентов и восстановить их подвижность. Основываясь на результатах испытаний на грызунах, исследователи предположили, что может произойти восстановление миелиновых оболочек и увеличение подвижности. Это первое испытание было в первую очередь предназначено для проверки безопасности этих процедур, и если все пойдет хорошо, есть надежда, что это приведет к будущим исследованиям с участием людей с более тяжелыми формами инвалидности.[38] Исследование было приостановлено в августе 2009 года из-за опасений FDA относительно небольшого количества микроскопических кист, обнаруженных на нескольких моделях обработанных крыс, но 30 июля 2010 года приостановка была снята.[39]
В октябре 2010 г. исследователи зарегистрировали и назначили EST первому пациенту в Пастырский центр в Атланта.[40] Создатели терапии стволовыми клетками, Корпорация Geron, подсчитали, что для репликации стволовых клеток и для GRNOPC1 терапия должна быть оценена на успех или неудачу.
В ноябре 2011 года Geron объявил о прекращении исследования и прекращении исследования стволовых клеток по финансовым причинам, но продолжит наблюдение за существующими пациентами и пытается найти партнера, который мог бы продолжить их исследования.[41] В 2013 BioTime во главе с генеральным директором Dr. Майкл Д. Уэст, приобрела все активы стволовых клеток Geron с заявленным намерением возобновить клинические испытания на основе эмбриональных стволовых клеток Geron для исследование травм спинного мозга.[42]
Компания «Биотайм» Asterias Biotherapeutics (NYSE MKT: AST) получила награду за стратегическое партнерство в размере 14,3 миллиона долларов от Калифорнийского института регенеративной медицины (CIRM) за возобновление первого в мире клинического испытания на людях с использованием эмбриональных стволовых клеток при повреждении спинного мозга. Поддерживаемый государственными фондами Калифорнии, CIRM является крупнейшим в мире спонсором исследований и разработок стволовых клеток.[43]
Премия обеспечивает финансирование Asterias для возобновления клинической разработки AST-OPC1 у субъектов с травмой спинного мозга и для расширения клинических испытаний возрастающих доз в целевой популяции, предназначенных для будущих ключевых испытаний.[43]
AST-OPC1 - это популяция клеток, полученных из эмбриональных стволовых клеток человека (hESC), которые содержат клетки-предшественники олигодендроцитов (OPC). OPC и их зрелые производные, называемые олигодендроцитами, обеспечивают важную функциональную поддержку нервным клеткам спинного и головного мозга. Asterias недавно представил результаты фазы 1 клинического испытания низкой дозы AST-OPC1 у пациентов с неврологически полным повреждением грудного отдела спинного мозга. Результаты показали, что AST-OPC1 был успешно доставлен в поврежденный участок спинного мозга. Пациенты наблюдались через 2–3 года после введения AST-OPC1, при детальных последующих оценках, включая частые неврологические осмотры и МРТ, не было выявлено серьезных побочных эффектов, связанных с клетками. Иммунный мониторинг субъектов в течение одного года после трансплантации не показал доказательств наличия антител или клеточного иммунного ответа на AST-OPC1. У четырех из пяти пациентов последовательные МРТ, выполненные в течение 2–3-летнего периода наблюдения, показали, что могло иметь место уменьшение кавитации спинного мозга и что AST-OPC1 мог иметь некоторые положительные эффекты в снижении разрушения ткани спинного мозга. По оценке Международных стандартов неврологической классификации травм спинного мозга (ISNCSCI), неожиданной неврологической дегенерации или улучшения у пяти испытуемых не было.[43]
Грант стратегического партнерства III от CIRM предоставит Asterias финансирование для поддержки следующего клинического испытания AST-OPC1 на субъектах с травмой спинного мозга, а также для усилий Asterias по разработке продуктов по совершенствованию и масштабированию производственных методов для поддержки более поздних стадий испытаний и, в конечном итоге, коммерциализация. Финансирование CIRM будет зависеть от одобрения FDA для испытания, завершения окончательного соглашения между Asterias и CIRM и дальнейшего продвижения Asterias к достижению определенных заранее определенных этапов проекта.[43]
Обеспокоенность и противоречие
Побочные эффекты
Основная проблема с возможной трансплантацией ESC пациентам в качестве терапии - их способность образовывать опухоли, включая тератому.[44] Проблемы безопасности побудили FDA приостановить первое клиническое испытание ESC, однако опухолей не наблюдалось.
Основная стратегия повышения безопасности ESC для потенциального клинического использования - дифференцировать ESC на определенные типы клеток (например, нейроны, мышцы, клетки печени), у которых снижена или устранена способность вызывать опухоли. После дифференцировки клетки подвергаются сортировке по проточной цитометрии для дальнейшей очистки. Предполагается, что ESC по своей сути безопаснее, чем Ячейки IPS созданы с помощью генетически интегрируемых вирусные векторы потому что они не генетически модифицированы такими генами, как c-Myc, которые связаны с раком. Тем не менее, ESC экспрессируют очень высокие уровни генов, индуцирующих iPS, и эти гены, включая Myc, необходимы для самообновления и плюрипотентности ESC,[45] и потенциальные стратегии повышения безопасности за счет устранения экспрессии c-Myc вряд ли сохранят «стволовость» клеток. Однако было установлено, что N-myc и L-myc индуцируют iPS-клетки вместо c-myc с аналогичной эффективностью.[46]Более современные протоколы для индукции плюрипотентности полностью обходят эти проблемы за счет использования неинтегрирующих вирусных векторов РНК, таких как вирус Сендай или мРНК трансфекция.
Этические дебаты
Из-за характера исследования эмбриональных стволовых клеток существует множество противоречивых мнений по этой теме. Поскольку сбор эмбриональных стволовых клеток требует уничтожения эмбриона, из которого эти клетки получены, моральный статус эмбриона ставится под сомнение. Некоторые люди утверждают, что 5-дневная масса клеток слишком молода для достижения индивидуальности, или что эмбрион, если его пожертвовать из клиники ЭКО (где лаборатории обычно получают эмбрионы), в противном случае все равно попал бы в медицинские отходы. Противники исследования ESC утверждают, что эмбрион - это человеческая жизнь, поэтому его уничтожение - убийство, и эмбрион должен быть защищен с той же этической точки зрения, что и более развитый человек.[47]
История
- 1964: Льюис Кляйнсмит и Дж. Барри Пирс-младший выделили один тип клеток из тератокарцинома, опухоль, известная из половая клетка.[48] Эти клетки были изолированы от тератокарцинома реплицировались и росли в клеточной культуре как стволовые клетки и теперь известны как клетки эмбриональной карциномы (ЭК).[нужна цитата ] Хотя сходство в морфологии и дифференцирующем потенциале (плюрипотентность ) привело к использованию ЭК-клеток в качестве in vitro модель для раннего развития мышей,[49] Клетки ЭК несут генетические мутации и часто аномальные кариотипы накопленные в процессе развития тератокарцинома. Эти генетические отклонения еще больше подчеркнули необходимость культивирования плюрипотентный ячейки прямо из внутренняя клеточная масса.

- 1981: Эмбриональные стволовые клетки (ES-клетки) были впервые независимо получены из эмбрионов мыши двумя группами. Мартин Эванс и Мэтью Кауфман из отдела генетики, Кембриджский университет опубликовано впервые в июле, раскрывая новую технику культивирования мышиных эмбрионов в матке, позволяющую увеличить количество клеток, что позволяет получить ES-клетки из этих эмбрионов.[50] Гейл Р. Мартин, от кафедры анатомии, Калифорнийский университет в Сан-Франциско, опубликовала свою статью в декабре и ввела термин «эмбриональная стволовая клетка».[51] Она показала, что эмбрионы можно культивировать in vitro и что ES-клетки могут происходить из этих эмбрионов.
- 1989: Марио Р. Каппечи, Мартин Дж. Эванс, и Оливер Смитис опубликовать свои исследования, в которых подробно описывается их изоляция и генетические модификации эмбриональных стволовых клеток, создавая первые "нокаутные мыши ".[52] При создании мышей с нокаутом эта публикация предоставила ученым совершенно новый способ изучения болезней.
- 1998: Команда из Университет Висконсина, Мэдисон (Джеймс А. Томсон, Джозеф Ицковиц-Элдор, Сандер С. Шапиро, Мишель А. Вакниц, Дженнифер Дж. Свиергель, Вивьен С. Маршалл и Джеффри М. Джонс) публикуют статью под названием «Линии эмбриональных стволовых клеток, полученные из бластоцист человека. ". Исследователи, стоящие за этим исследованием, не только создали первые эмбриональные стволовые клетки, но и признали их плюрипотентность, а также их способность к самообновлению. В аннотации к статье отмечается важность открытия для области биологии развития и открытия лекарств.[53]
- 2001: Президент Джордж Буш позволяет федеральное финансирование для поддержки исследований примерно 60 - в настоящее время уже существующих - линий эмбриональных стволовых клеток. Поскольку ограниченные линии, разрешенные Бушем для исследований, уже установлены, этот закон поддерживает исследования эмбриональных стволовых клеток, не вызывая при этом никаких дополнительных затрат. этические вопросы это может возникнуть при создании новых статей в федеральном бюджете.[54]
- 2006: японские ученые Шинья Яманака и Кадзутоши Такаши публикуют статью, описывающую индукцию плюрипотентных стволовых клеток из культур взрослых мышей. фибробласты. Индуцированные плюрипотентные стволовые клетки (ИПСК) являются огромным открытием, поскольку они кажутся идентичными эмбриональным стволовым клеткам и могут использоваться, не вызывая таких же моральных споров.[55]
- Январь 2009 г .: Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) дает разрешение на Корпорация Geron Фаза I испытания их лечения на основе человеческих эмбриональных стволовых клеток травмы спинного мозга. Это объявление было встречено с энтузиазмом в научном сообществе, но также с осторожностью со стороны противников стволовых клеток. Однако лечебные клетки были получены из клеточных линий, одобренных Джорджем Бушем-младшим. Политика ESC.[56]
- Март 2009 г .: Распоряжение 13505 подписано Президент Барак Обама, сняв ограничения, введенные предыдущей президентской администрацией на федеральное финансирование стволовых клеток человека. Это позволило бы Национальные институты здоровья (NIH), чтобы обеспечить финансирование исследований hESC. В документе также говорится, что NIH должен предоставить пересмотренные руководящие принципы федерального финансирования в течение 120 дней с момента подписания приказа.[57]
Методы и условия происхождения и культуры
Происхождение от человека
В результате оплодотворения in vitro образуется несколько эмбрионов. Излишки эмбрионов не используются в клинических условиях или не подходят для имплантации пациенту и поэтому могут быть переданы донором с согласия. Эмбриональные стволовые клетки человека могут быть получены из этих донорских эмбрионов или, кроме того, они также могут быть извлечены из клонированных эмбрионов с использованием клетки пациента и донорской яйцеклетки.[58] Внутренняя клеточная масса (представляющие интерес клетки) на стадии бластоцисты эмбриона отделяется от трофэктодермы, клеток, которые могут дифференцироваться во внеэмбриональную ткань. Иммунохирургия, процесс, при котором антитела связываются с трофэктодермой и удаляются другим раствором, и механическое рассечение выполняется для достижения разделения. Полученные клетки внутренней клеточной массы наносят на клетки, которые будут обеспечивать поддержку. Клетки внутренней клеточной массы прикрепляются и расширяются, образуя линию эмбриональных клеток человека, которые недифференцированы. Эти клетки питаются ежедневно и разделяются ферментативно или механически каждые четыре-семь дней. Для того чтобы дифференцировка произошла, линия эмбриональных стволовых клеток человека удаляется из поддерживающих клеток с образованием эмбриоидных тел, культивируется совместно с сывороткой, содержащей необходимые сигналы, или для получения результата прививается в трехмерный каркас.[59]
Происхождение от других животных
Эмбриональные стволовые клетки получают из внутренняя клеточная масса раннего эмбрион, которые получены от материнского животного-донора. Мартин Эванс и Мэтью Кауфман сообщили о технике, которая задерживает имплантацию эмбриона, позволяя увеличивать внутреннюю клеточную массу. Этот процесс включает удаление донорской матери яичники и дозируя ее прогестерон, изменяя гормональную среду, которая заставляет эмбрионы оставаться свободными в матке. Через 4–6 дней внутриутробного культивирования эмбрионы собирают и выращивают в in vitro культивировать до тех пор, пока внутренняя клеточная масса не образует «цилиндрические структуры яйца», которые диссоциируют на отдельные клетки и высевают на фибробласты лечится с митомицин-с (для предотвращения фибробластов митоз ). Клональный Сотовые линии создаются путем выращивания одной клетки. Эванс и Кауфман показали, что клетки, выросшие из этих культур, могут образовывать тератомы и эмбриоидные тела, и дифференцировать in vitro, все это указывает на то, что клетки плюрипотентный.[50]
Гейл Мартин по-разному получали и культивировали ее ES-клетки. Она удалила эмбрионы от матери-донора примерно через 76 часов после совокупления и культивировала их в течение ночи в среде, содержащей сыворотку. На следующий день она удалила внутренняя клеточная масса с конца бластоциста с помощью микрохирургия. Извлеченный внутренняя клеточная масса был выращен на фибробласты лечится с митомицин-с в среде, содержащей сыворотку и кондиционированной ES-клетками. Примерно через неделю выросли колонии клеток. Эти клетки выросли в культуре и продемонстрировали плюрипотентный характеристики, о чем свидетельствует способность формировать тератомы, дифференцировать in vitro, и форма эмбриоидные тела. Мартин называл эти клетки ES-клетками.[51]
Теперь известно, что питающие ячейки предоставлять фактор ингибирования лейкемии (LIF) и сыворотка обеспечивают костные морфогенетические белки (BMP), которые необходимы для предотвращения дифференцировки ES-клеток.[60][61] Эти факторы чрезвычайно важны для эффективности получения ES-клеток. Кроме того, было продемонстрировано, что разные линии мышей обладают разной эффективностью для выделения ES-клеток.[62] Текущее использование ES-клеток мыши включает создание трансгенный мышей, в том числе нокаутные мыши. Для лечения человека необходимы плюрипотентные клетки, специфичные для пациента. Создание человеческих ES-клеток сложнее и сталкивается с этическими проблемами. Таким образом, в дополнение к исследованиям человеческих ES-клеток, многие группы сосредоточены на создании индуцированные плюрипотентные стволовые клетки (iPS-клетки).[63]
Возможный метод получения новой клеточной линии
23 августа 2006 г. онлайн-издание Природа в научном журнале опубликовано письмо доктора В. Роберт Ланца (медицинский директор Передовая клеточная технология в Вустере, Массачусетс), заявив, что его команда нашла способ извлекать эмбриональные стволовые клетки без разрушения самого эмбриона.[64] Это техническое достижение потенциально позволит ученым работать с новыми линиями эмбриональных стволовых клеток, полученными с использованием государственного финансирования в США, где федеральное финансирование в то время ограничивалось исследованиями с использованием линий эмбриональных стволовых клеток, полученных до августа 2001 г. В марте 2009 г. ограничение снято.[65]
Индуцированные плюрипотентные стволовые клетки
Технология iPSC была впервые разработана Шинья Яманака Лаборатория в Киото, Япония, которые в 2006 году показали, что введение четырех специфических генов, кодирующих факторы транскрипции может превращать взрослые клетки в плюрипотентные стволовые клетки.[66] Он был удостоен Нобелевской премии 2012 года вместе с сэром Джон Гэрдон «за открытие, что зрелые клетки можно перепрограммировать, чтобы стать плюрипотентными». [67]
В 2007 году было показано, что плюрипотентный стволовые клетки очень похожие на эмбриональные стволовые клетки могут быть получены путем доставки трех генов (4 октября, Sox2, и Klf4) к дифференцированным клеткам.[68] Доставка этих генов «перепрограммирует» дифференцированные клетки в плюрипотентные стволовые клетки, позволяя генерировать плюрипотентные стволовые клетки без эмбриона. Поскольку этические проблемы в отношении эмбриональных стволовых клеток обычно связаны с их происхождением из терминированных эмбрионов, считается, что перепрограммирование на эти «индуцированные плюрипотентные стволовые клетки» (iPS-клетки) может быть менее спорным. С помощью этой методологии можно перепрограммировать как человеческие, так и мышиные клетки, создавая как плюрипотентные стволовые клетки человека, так и плюрипотентные стволовые клетки мыши без эмбриона.[69]
Это может позволить создание специфичных для пациента линий ES-клеток, которые потенциально могут быть использованы для терапии замещения клеток. Кроме того, это позволит получать линии ES-клеток от пациентов с различными генетическими заболеваниями и предоставит бесценные модели для изучения этих заболеваний.
Однако в качестве первого признака того, что индуцированная плюрипотентная стволовая клетка (iPS) клеточная технология может быстро привести к новым лекарствам, ее использовала исследовательская группа во главе с Рудольф Яениш из Институт биомедицинских исследований Уайтхеда в Кембридж, Массачусетс, чтобы вылечить мышей от серповидноклеточная анемия, как сообщает Наука журнал Интернет-издание от 6 декабря 2007 г.[70][71]
16 января 2008 года калифорнийская компания Stemagen объявила, что они создали первые зрелые клонированные человеческие эмбрионы из отдельных клеток кожи, взятых у взрослых. Эти эмбрионы могут быть получены для сопоставления с пациентами эмбриональных стволовых клеток.[72]
Загрязнение реагентами, используемыми в культуре клеток
Интернет-издание Природа Медицина опубликовал исследование 24 января 2005 года, в котором говорилось, что человеческие эмбриональные стволовые клетки, доступные для исследований, финансируемых из федерального бюджета, загрязнены нечеловеческими молекулами из культуральной среды, используемой для выращивания клеток.[73] Это общепринятая методика использования клеток мышей и других клеток животных для поддержания плюрипотентности активно делящихся стволовых клеток. Проблема была обнаружена, когда нечеловеческий сиаловая кислота в среде для выращивания было обнаружено, что ставит под угрозу потенциальное использование эмбриональных стволовых клеток у людей, по словам ученых из Калифорнийский университет в Сан-Диего.[74]
Однако исследование, опубликованное в онлайн-издании Ланцет Медицинский журнал 8 марта 2005 г. подробная информация о новой линии стволовых клеток, полученной из человеческих эмбрионов в полностью бесклеточных и бессывороточных условиях. После более чем 6 месяцев недифференцированной пролиферации эти клетки продемонстрировали способность образовывать производные всех трех зародышевых листков эмбриона. in vitro И в тератомы. Эти свойства также были успешно поддержаны (более 30 пассажей) с помощью установленных линий стволовых клеток.[75]
Смотрите также
- Эмбриоидное тело
- Комитеты по надзору за исследованиями эмбриональных стволовых клеток
- Имплантат ткани плода
- Индуцированные стволовые клетки
- Противоречие стволовых клеток
использованная литература
- ^ Томсон; Ицковиц-Элдор, Дж; Шапиро, СС; Вакниц, Массачусетс; Swiergiel, JJ; Маршалл, VS; Джонс, JM (1998). «Линии эмбриональных стволовых клеток бластоцисты, полученные от человека». Наука. 282 (5391): 1145–1147. Bibcode:1998Научный ... 282.1145Т. Дои:10.1126 / science.282.5391.1145. PMID 9804556.
- ^ "Основы стволовых клеток NIH. Что такое эмбриональные стволовые клетки?". Архивировано из оригинал на 31.08.2016. Получено 2014-03-25.
- ^ Болдуинг А (2009). «Исследование нравственности и человеческого эмбриона. Введение в тему для обсуждения морали и исследования человеческого эмбриона». EMBO отчеты. 10 (4): 299–300. Дои:10.1038 / embor.2009.37. ЧВК 2672902. PMID 19337297.
- ^ Накая, Андреа К. (1 августа 2011 г.). Биомедицинская этика. Сан-Диего, Калифорния: ReferencePoint Press. стр.96. ISBN 978-1601521576.
- ^ а б «Введение: что такое стволовые клетки и почему они так важны?». Национальные институты здоровья. Получено 28 октября 2018.
- ^ Карла А. Хербертс; Марсель С.Г. Ква; Вред PH Hermsen (2011). «Факторы риска в развитии терапии стволовыми клетками». Журнал трансляционной медицины. 9 (29): 29. Дои:10.1186/1479-5876-9-29. ЧВК 3070641. PMID 21418664.
- ^ а б Thomson, J. A .; Ицковиц-Элдор, Дж; Шапиро, С. С .; Вакниц, М. А .; Swiergiel, J. J .; Маршалл, В. С .; Джонс, Дж. М. (1998). «Линии эмбриональных стволовых клеток, полученные из бластоцист человека». Наука. 282 (5391): 1145–7. Bibcode:1998Научный ... 282.1145Т. Дои:10.1126 / science.282.5391.1145. PMID 9804556.
- ^ Инь; Николс, Дж; Камеры, I; Смит, А (2003). «Индукция BMP белков Id подавляет дифференцировку и поддерживает самообновление эмбриональных стволовых клеток в сотрудничестве с STAT3». Ячейка. 115 (3): 281–292. Дои:10.1016 / S0092-8674 (03) 00847-X. PMID 14636556. S2CID 7201396.
- ^ Мартелло, G .; Смит, А. (2014). «Природа эмбриональных стволовых клеток». Ежегодный обзор клеточной биологии и биологии развития. 30: 647–75. Дои:10.1146 / annurev-cellbio-100913-013116. PMID 25288119.
- ^ а б Boward, B .; Wu, T .; Далтон, С. (2016). «Краткий обзор: контроль клеточной судьбы посредством клеточного цикла и сетей плюрипотентности». Стволовые клетки. 34 (6): 1427–36. Дои:10.1002 / шток.2345. ЧВК 5201256. PMID 26889666.
- ^ White, J .; Stead, E .; Faast, R .; Conn, S .; Картрайт, П .; Далтон, С. (2005). «Активация развития пути Rb-E2F и установление регулируемой клеточного цикла циклин-зависимой киназной активности во время дифференцировки эмбриональных стволовых клеток». Молекулярная биология клетки. 16 (4): 2018–27. Дои:10.1091 / mbc.e04-12-1056. ЧВК 1073679. PMID 15703208.
- ^ Сингх, Амар М .; Далтон, Стивен (2007-08-07). «Клеточный цикл и Myc пересекаются с механизмами, регулирующими плюрипотентность и перепрограммирование». Стволовая клетка. 5 (2): 141–149. Дои:10.1016 / j.stem.2009.07.003. ISSN 1875-9777. ЧВК 2909475. PMID 19664987.
- ^ Тер Хюрне, Менно; Чаппелл, Джеймс; Далтон, Стивен; Штунненберг, Хендрик Г. (5 октября 2017 г.). «Четкий контроль клеточного цикла в двух разных состояниях плюрипотентности мышей». Стволовая клетка. 21 (4): 449–455.e4. Дои:10.1016 / j.stem.2017.09.004. ISSN 1875-9777. ЧВК 5658514. PMID 28985526.
- ^ Инь, Ци-Лун; Рэй, Джейсон; Николс, Дженнифер; Батль-Морера, Лаура; Добл, Брэдли; Вудгетт, Джеймс; Коэн, Филипп; Смит, Остин (22 мая 2008 г.). «Основное состояние самообновления эмбриональных стволовых клеток». Природа. 453 (7194): 519–523. Bibcode:2008Натура.453..519л. Дои:10.1038 / природа06968. ISSN 1476-4687. ЧВК 5328678. PMID 18497825.
- ^ Lee, J .; Вперед, Y .; Канг, И .; Han, Y.M .; Ким, Дж. (2010). «Oct-4 контролирует развитие клеточного цикла эмбриональных стволовых клеток». Биохимический журнал. 426 (2): 171–81. Дои:10.1042 / BJ20091439. ЧВК 2825734. PMID 19968627.
- ^ Чжан, X .; Неганова, И .; Пржиборски, С .; Ян, С .; Cooke, M .; Аткинсон, С.П .; Anyfantis, G .; Феник, С .; Keith, W. N .; Hoare, S. F .; Hughes, O .; Страчан, Т .; Стойкович, М .; Hinds, P.W .; Armstrong, L .; Лако, М. (2009). «Роль NANOG в переходе с G1 на S в эмбриональных стволовых клетках человека посредством прямого связывания CDK6 и CDC25A». Журнал клеточной биологии. 184 (1): 67–82. Дои:10.1083 / jcb.200801009. ЧВК 2615089. PMID 19139263.
- ^ Махла, Ранджит (19 июля 2016 г.). «Применение стволовых клеток в регенеративной медицине и терапии болезней». Международный журнал клеточной биологии. 2016: 6940283. Дои:10.1155/2016/6940283. ЧВК 4969512. PMID 27516776.
- ^ Левенберг, С. (2002). «Эндотелиальные клетки, полученные из эмбриональных стволовых клеток человека». Труды Национальной академии наук. 99 (7): 4391–4396. Bibcode:2002PNAS ... 99.4391L. Дои:10.1073 / pnas.032074999. ЧВК 123658. PMID 11917100.
- ^ а б Davila, JC; Cezar, GG; Thiede, M; Стром, S; Мики, Т; Троско, Дж (2004). «Использование и применение стволовых клеток в токсикологии». Токсикологические науки. 79 (2): 214–23. Дои:10.1093 / toxsci / kfh100. PMID 15014205.
- ^ Сиу, CW; Мур, JC; Ли, РА (2007). «Кардиомиоциты, полученные из эмбриональных стволовых клеток человека, для лечения сердца». Цели лекарств от сердечно-сосудистых и гематологических заболеваний. 7 (2): 145–52. Дои:10.2174/187152907780830851. PMID 17584049.
- ^ Перье, А. Л. (2004). «Получение дофаминовых нейронов среднего мозга из эмбриональных стволовых клеток человека». Труды Национальной академии наук. 101 (34): 12543–12548. Bibcode:2004ПНАС..10112543П. Дои:10.1073 / pnas.0404700101. ЧВК 515094. PMID 15310843.
- ^ Приход, CL; Аренас, Э (2007). «Стратегии на основе стволовых клеток для лечения болезни Паркинсона». Нейродегенеративные заболевания. 4 (4): 339–47. Дои:10.1159/000101892. PMID 17627139. S2CID 37229348.
- ^ Waese, EY; Кандел, РА; Стэнфорд, Вашингтон (2008). «Применение стволовых клеток в восстановлении костей». Скелетная радиология. 37 (7): 601–8. Дои:10.1007 / s00256-007-0438-8. PMID 18193216. S2CID 12401889.
- ^ d'Amour, KA; Bang, AG; Элиазер, S; Келли, О.Г .; Agulnick, AD; Смарт, НГ; Мурман, Массачусетс; Kroon, E; Карпентер, МК; Баетге, EE (2006). «Производство эндокринных клеток, экспрессирующих гормон поджелудочной железы, из человеческих эмбриональных стволовых клеток». Природа Биотехнологии. 24 (11): 1392–401. Дои:10.1038 / nbt1259. PMID 17053790. S2CID 11040949.
- ^ Колен, Б. (9 октября 2014 г.) Гигантский скачок против диабета The Harvard Gazette, последнее посещение - 24 ноября 2014 г.
- ^ Менаше, Филипп; Ванно, Валери; Фабрегетт, Жан-Рош; Бел, Ален; Тоска, Люси; Гарсия, Сильви (21 марта 2015 г.). «На пути к клиническому использованию кардиальных предшественников, полученных из человеческих эмбриональных стволовых клеток: трансляционный опыт». Европейский журнал сердца. 36 (12): 743–750. Дои:10.1093 / eurheartj / ehu192. PMID 24835485.
- ^ Дженсен, Дж; Hyllner, J; Бьорквист, П. (2009). «Технологии эмбриональных стволовых клеток человека и открытие лекарств». Журнал клеточной физиологии. 219 (3): 513–9. Дои:10.1002 / jcp.21732. PMID 19277978. S2CID 36354049.
- ^ Söderdahl, T; Кюпперс-Мюнтер, Б; Heins, N; Эдсбэгдж, Дж; Björquist, P; Котгрив, I; Йернстрем, Б. (2007). «Глутатионтрансферазы в гепатоцитоподобных клетках, полученных из эмбриональных стволовых клеток человека». Токсикология in vitro. 21 (5): 929–37. Дои:10.1016 / j.tiv.2007.01.021. PMID 17346923.
- ^ «Доктор Юрий Верлинский, 1943–2009: Специалист по репродуктивным технологиям» В архиве 2008-08-08 на Wayback Machine Чикаго Трибьюн, 20 июля 2009 г.
- ^ Мао З., Боццелла М., Селуанов А., Горбунова В. (сентябрь 2008 г.). «Ремонт ДНК путем негомологичного соединения концов и гомологичной рекомбинации во время клеточного цикла в клетках человека». Клеточный цикл. 7 (18): 2902–6. Дои:10.4161 / cc.7.18.6679. ЧВК 2754209. PMID 18769152.
- ^ а б Тихи Э.Д., Пиллай Р., Дэн Л. и др. (Ноябрь 2010 г.). «Эмбриональные стволовые клетки мыши, но не соматические клетки, в основном используют гомологичную рекомбинацию для восстановления двухцепочечных разрывов ДНК». Стволовые клетки Dev. 19 (11): 1699–711. Дои:10.1089 / scd.2010.0058. ЧВК 3128311. PMID 20446816.
- ^ Хонг И., Стамбрук П.Дж. (октябрь 2004 г.). «Восстановление отсутствующей остановки G1 и защиты от апоптоза в эмбриональных стволовых клетках после ионизирующего излучения». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 101 (40): 14443–8. Bibcode:2004PNAS..10114443H. Дои:10.1073 / pnas.0401346101. ЧВК 521944. PMID 15452351.
- ^ Аладжем М.И., Спайк Б.Т., Родевальд Л.В. и др. (Январь 1998 г.). «ES-клетки не активируют p53-зависимые стрессовые ответы и подвергаются p53-независимому апоптозу в ответ на повреждение ДНК». Curr. Биол. 8 (3): 145–55. Дои:10.1016 / S0960-9822 (98) 70061-2. PMID 9443911. S2CID 13938854.
- ^ Бернштейн C, Бернштейн H, Пейн CM, Гарвал H (июнь 2002 г.). «Репарация ДНК / проапоптотические белки с двойной ролью в пяти основных путях репарации ДНК: надежная защита от канцерогенеза». Мутат. Res. 511 (2): 145–78. Дои:10.1016 / S1383-5742 (02) 00009-1. PMID 12052432.
- ^ Сервантес РБ, Стрингер Дж. Р., Шао С., Тишфилд Дж. А., Стамбрук П. Дж. (Март 2002 г.). «Эмбриональные стволовые клетки и соматические клетки различаются по частоте и типу мутаций». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 99 (6): 3586–90. Bibcode:2002PNAS ... 99.3586C. Дои:10.1073 / pnas.062527199. ЧВК 122567. PMID 11891338.
- ^ «FDA одобряет исследование эмбриональных стволовых клеток человека - CNN.com». 23 января 2009 г.. Получено 1 мая, 2010.
- ^ Кейрстед Х.С., Нистор Г., Бернал Г. и др. (2005). «Трансплантаты клеток-предшественников олигодендроцитов, полученных из эмбриональных стволовых клеток человека, ремиелинизируют и восстанавливают двигательную активность после повреждения спинного мозга» (PDF). J. Neurosci. 25 (19): 4694–705. Дои:10.1523 / JNEUROSCI.0311-05.2005. ЧВК 6724772. PMID 15888645.
- ^ Рейнберг, Стивен (23.01.2009) FDA одобрило первое испытание эмбриональных стволовых клеток. Вашингтон Пост
- ^ Geron комментирует, что FDA продолжает исследование травмы спинного мозга. geron.com (27 августа 2009 г.)
- ^ Вергано, Дэн (11 октября 2010 г.). «Эмбриональные стволовые клетки используются пациенту впервые». USA Today. Получено 12 октября 2010.
- ^ Браун, Эрин (15 ноября 2011 г.). "Geron прекращает исследования стволовых клеток". LA Times. Получено 2011-11-15.
- ^ «Отличные новости: дочерняя компания BioTime Asterias приобретает программу эмбриональных стволовых клеток Geron». iPScell.com. 1 октября 2013.
- ^ а б c d Калифорнийский институт регенеративной медицины В архиве 2017-10-24 на Wayback Machine. BioTime, Inc.
- ^ Кнёпфлер, Пол С. (2009). «Деконструкция онкогенности стволовых клеток: дорожная карта для безопасной регенеративной медицины». Стволовые клетки. 27 (5): 1050–6. Дои:10.1002 / шток.37. ЧВК 2733374. PMID 19415771.
- ^ Варлаханова Наталья В .; Коттерман, Ребекка Ф .; Деврис, Вильгельмин Н .; Морган, Джуди; Донахью, Лия Рэй; Мюррей, Стивен; Ноулз, Барбара Б .; Кнёпфлер, Пол С. (2010). «Myc поддерживает плюрипотентность и самообновление эмбриональных стволовых клеток». Дифференциация. 80 (1): 9–19. Дои:10.1016 / j.diff.2010.05.001. ЧВК 2916696. PMID 20537458.
- ^ Верниг, Мариус; Мейснер, Александр; Кэссиди, Джон П.; Яениш, Рудольф (2008). «C-Myc незаменим для прямого репрограммирования фибробластов мыши». Стволовая клетка. 2 (1): 10–2. Дои:10.1016 / j.stem.2007.12.001. PMID 18371415.
- ^ Кинг, Нэнси; Перрин, Джейкоб (7 июля 2014 г.). «Этические вопросы исследования и лечения стволовых клеток». Исследование стволовых клеток и терапия. 5 (4): 85. Дои:10.1186 / scrt474. ЧВК 4097842. PMID 25157428.
- ^ Кляйнсмит LJ, Пирс GB младший (1964). «Мультипотентность клеток одиночной эмбриональной карциномы». Рак Res. 24: 1544–51. PMID 14234000.
- ^ Мартин Г.Р. (1980). «Тератокарциномы и эмбриогенез млекопитающих». Наука. 209 (4458): 768–76. Bibcode:1980Sci ... 209..768M. Дои:10.1126 / science.6250214. PMID 6250214.
- ^ а б Эванс М, Кауфман М (1981). «Создание в культуре плюрипотентных клеток из эмбрионов мыши». Природа. 292 (5819): 154–6. Bibcode:1981Натура.292..154E. Дои:10.1038 / 292154a0. PMID 7242681. S2CID 4256553.
- ^ а б Мартин Дж. (1981). «Выделение плюрипотентной клеточной линии из ранних эмбрионов мыши, культивированных в среде, кондиционированной стволовыми клетками тератокарциномы». Proc Natl Acad Sci USA. 78 (12): 7634–8. Bibcode:1981PNAS ... 78.7634M. Дои:10.1073 / pnas.78.12.7634. ЧВК 349323. PMID 6950406.
- ^ «Нобелевская премия 2007 года по физиологии и медицине - расширенная информация». Нобелевская премия. Nobel Media.
- ^ Томпсон, Джеймс А .; Ицковиц-Эльдор, Джозеф; Шапиро, Сандер С .; Waknitz, Michelle A .; Swiergiel, Jennifer J .; Marshall, Vivienne S .; Джонс, Джеффри М. (6 ноября 1998 г.). «Линии эмбриональных стволовых клеток, полученные из бластоцисты человека». Наука. 282 (5391): 1145–1147. Bibcode:1998Научный ... 282.1145Т. Дои:10.1126 / science.282.5391.1145. PMID 9804556.
- ^ "Обращение президента Джорджа Буша к исследованию стволовых клеток". CNN Внутри политики. CNN. 9 августа 2001 г.
- ^ Яманака, Шинья; Такахаши, Кадзутоши (25 августа 2006 г.). «Индукция плюрипотентных стволовых клеток из эмбриональных и взрослых культур фибробластов мышей с помощью определенных факторов». Ячейка. 126 (4): 663–676. Дои:10.1016 / j.cell.2006.07.024. HDL:2433/159777. PMID 16904174. S2CID 1565219.
- ^ Вадман, Мередит (27 января 2009 г.). «Стволовые клетки готовы к прайм-тайму». Природа. 457 (7229): 516. Дои:10.1038 / 457516a. PMID 19177087.
- ^ «Правительственный указ 13505 - Устранение барьеров для ответственных научных исследований с участием стволовых клеток человека» (PDF). Федеральный реестр: документы президента. 74 (46). 11 марта 2009 г.
- ^ Маунтфорд, JC (2008). «Эмбриональные стволовые клетки человека: происхождение, характеристики и возможности регенеративной терапии». Трансфус Мед. 18 (1): 1–12. Дои:10.1111 / j.1365-3148.2007.00807.x. PMID 18279188. S2CID 20874633.
- ^ Томсон Дж., Ицковиц-Элдор Дж, Шапиро С.С., Вакниц М.А., Свиергель Дж. Дж., Маршалл В. С., Джонс Дж. М. (1998). «Линии эмбриональных стволовых клеток, полученные из бластоцист человека». Наука. 282 (5391): 1145–1147. Bibcode:1998Научный ... 282.1145Т. Дои:10.1126 / science.282.5391.1145. PMID 9804556.
- ^ Смит А.Г., Хит Дж. К., Дональдсон Д. Д., Вонг Г. Г., Моро Дж., Шталь М., Роджерс Д. (1988). «Ингибирование плюрипотенциальной дифференцировки эмбриональных стволовых клеток очищенными полипептидами». Природа. 336 (6200): 688–690. Bibcode:1988Натура.336..688С. Дои:10.1038 / 336688a0. PMID 3143917. S2CID 4325137.
- ^ Уильямс Р.Л., Хилтон Д.Д., Пис С., Уилсон Т.А., Стюарт К.Л., Геринг Д.П., Вагнер Э.Ф., Меткалф Д., Никола Н.А., Гоф Н.М. (1988). «Фактор ингибирования миелоидной лейкемии поддерживает потенциал развития эмбриональных стволовых клеток». Природа. 336 (6200): 684–687. Bibcode:1988 Натур. 336..684Вт. Дои:10.1038 / 336684a0. PMID 3143916. S2CID 4346252.
- ^ Ледерманн Б., Бюрки К. (1991). «Создание компетентной зародышевой линии линии эмбриональных стволовых клеток C57BL / 6». Exp Cell Res. 197 (2): 254–258. Дои:10.1016/0014-4827(91)90430-3. PMID 1959560.
- ^ Такахаши К., Танабе К., Охнуки М., Нарита М., Ичисака Т., Томода К., Яманака С. (2007). «Индукция плюрипотентных стволовых клеток из фибробластов взрослого человека определенными факторами». Ячейка. 131 (5): 861–872. Дои:10.1016 / j.cell.2007.11.019. HDL:2433/49782. PMID 18035408. S2CID 8531539.
- ^ Климанская И., Чунг Ю., Беккер С., Лу С. Дж., Ланза Р. (2006). «Линии эмбриональных стволовых клеток человека, полученные из отдельных бластомеров». Природа. 444 (7118): 481–5. Bibcode:2006Натура 444..481K. Дои:10.1038 / природа05142. PMID 16929302. S2CID 84792371.
- ^ Ученые США почувствовали облегчение, когда Обама снял запрет на исследования стволовых клеток, Хранитель, 10 марта 2009 г.
- ^ Такахаши, К. Яманака, S (2006). «Индукция плюрипотентных стволовых клеток из эмбриональных и взрослых культур фибробластов мыши с помощью определенных факторов». Ячейка. 126 (4): 663–76. Дои:10.1016 / j.cell.2006.07.024. HDL:2433/159777. PMID 16904174. S2CID 1565219.

- ^ "Нобелевская премия по физиологии и медицине - пресс-релиз 2012 г.". Nobel Media AB. 8 октября 2012 г.
- ^ Верниг, Мариус; Мейснер, Александр; Форман, Рут; Брамбринк, Тобиас; Ку, Манчинг; Hochedlinger, Конрад; Бернштейн, Брэдли Э .; Яениш, Рудольф (19 июля 2007 г.). «Перепрограммирование фибробластов in vitro в плюрипотентное состояние, подобное ES-клеткам». Природа. 448 (7151): 318–324. Bibcode:2007 Натур.448..318Вт. Дои:10.1038 / природа05944. ISSN 1476-4687. PMID 17554336. S2CID 4377572.
- ^ «Эмбриональные стволовые клетки, полученные без эмбрионов». Рейтер. 2007-11-21.
- ^ Вайс, Рик (2007-12-07). «Ученые лечат мышей от серповидных клеток, используя метод стволовых клеток: новый подход - это кожа, а не эмбрионы». Вашингтон Пост. стр. A02.
- ^ Hanna, J .; Wernig, M .; Маркулаки, S .; Sun, C.-W .; Meissner, A .; Cassady, J. P .; Beard, C .; Brambrink, T .; Wu, L.-C .; Townes, T. M .; Яениш Р. (2007). «Лечение мышиной модели серповидноклеточной анемии iPS-клетками, полученными из аутологичной кожи». Наука. 318 (5858): 1920–3. Bibcode:2007Научный ... 318.1920H. Дои:10.1126 / science.1152092. PMID 18063756. S2CID 657569.
- ^ Хелен Бриггс (17 января 2008 г.). «Команда США создает клон эмбриона человека». BBC. стр. A01.
- ^ Эберт, Джессика (24 января 2005 г.). «Стволовые клетки человека вызывают иммунную атаку». Новости природы. Лондон: Издательская группа Nature. Дои:10.1038 / news050124-1. Архивировано из оригинал на 24.09.2010. Получено 2009-02-27.
- ^ Мартин MJ, Муотри А, Гейдж Ф, Варки А (2005). «Эмбриональные стволовые клетки человека экспрессируют иммуногенную сиаловую кислоту, отличную от человека». Nat. Med. 11 (2): 228–32. Дои:10,1038 / нм 1181. PMID 15685172. S2CID 13739919.
- ^ Климанская И., Чунг Ю., Мейснер Л., Джонсон Дж., Западный доктор медицины, Ланза Р. (2005). «Эмбриональные стволовые клетки человека, полученные без питающих клеток». Ланцет. 365 (9471): 1636–41. Дои:10.1016 / S0140-6736 (05) 66473-2. PMID 15885296. S2CID 17139951.
внешняя ссылка
- Понимание стволовых клеток: взгляд на науку и проблемы национальных академий
- Национальные институты здоровья
- Практический семинар Оксфордского университета по технологии плюрипотентных стволовых клеток
- Информационный бюллетень об эмбриональных стволовых клетках
- Информационный бюллетень по этическим вопросам исследования эмбриональных стволовых клеток
- Информация и альтернативы исследованиям эмбриональных стволовых клеток
- Блог, посвященный ES-клеткам и iPS-клеткам, включая исследования, биотехнологии и вопросы, ориентированные на пациентов.
