Надпочечник - Adrenal gland
Эта статья может быть написано с чрезмерно ориентированный на человека перспектива. (Март 2019 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
| Надпочечник | |
|---|---|
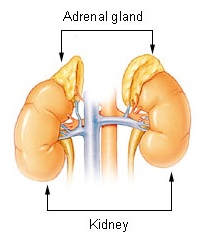 Надпочечники лежат над почками. | |
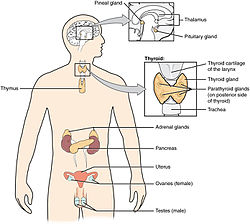 | |
| Подробности | |
| Предшественник | Мезодерма и нервный гребень |
| Система | Эндокринная система |
| Артерия | Начальство, середина и нижние надпочечные артерии |
| Вен | Надпочечные вены |
| Нерв | Целиакия и почечное сплетение |
| Лимфа | Поясничные лимфатические узлы |
| Идентификаторы | |
| латинский | Надпочечная железа |
| MeSH | D000311 |
| TA98 | A11.5.00.001 |
| TA2 | 3874 |
| FMA | 9604 |
| Анатомическая терминология | |
В надпочечники (также известен как надпочечники) находятся эндокринные железы которые производят множество гормонов, включая адреналин и стероиды альдостерон и кортизол.[1][2] Они находятся над почки. Каждая железа имеет внешний кора который производит стероидные гормоны и внутренний мозговое вещество. В кора надпочечников сам разделен на три зоны: зона клубочков, то зона фасцикулата и zona reticularis.[3]
Кора надпочечников производит три основных типа стероидные гормоны: минералокортикоиды, глюкокортикоиды, и андрогены. Минералокортикоиды (такие как альдостерон ), произведенные в клубочковой зоне, помогают регулировать кровяное давление и электролитный баланс. Глюкокортикоиды кортизол и кортизон синтезируются в фасцикулатной зоне; в их функции входит регулирование метаболизм и иммунная система подавление. Самый внутренний слой коры, ретикулярная зона, производит андрогены, которые превращаются в полнофункциональные половые гормоны в гонады и другие органы-мишени.[4] Производство стероидных гормонов называется стероидогенез, и включает в себя ряд реакций и процессов, происходящих в корковых клетках.[5] Мозговое вещество производит катехоламины, какая функция производит быстрый ответ по всему телу в стресс ситуации.[4]
Номер эндокринные заболевания вовлекают дисфункцию надпочечников. Избыточное производство кортизола приводит к синдром Кушинга, а недостаточное производство связано с Болезнь Эддисона. Врожденная гиперплазия надпочечников это генетическое заболевание, вызванное нарушением регуляции механизмов эндокринного контроля.[4][6] Разнообразие опухоли могут возникать из ткани надпочечников и обычно встречаются в медицинская визуализация при поиске других болезней.[7]
Структура
Надпочечники расположены по обе стороны тела в забрюшинное пространство, выше и немного медиальный к почки. У людей правый надпочечник имеет пирамидальную форму, тогда как левый - полулунный или серповидный и несколько больше.[8] Надпочечники составляют примерно 3 см в ширину, 5,0 см в длину и до 1,0 см в толщину.[9] Их общий вес у взрослого человека колеблется от 7 до 10 граммов.[10] Железы желтоватого цвета.[8]
Надпочечники окружены жировая капсула и лежать внутри почечная фасция, который также окружает почки. Слабый перегородка (стена) из соединительная ткань отделяет железы от почек.[11] Надпочечники находятся прямо под диафрагма, и прикреплены к ножки диафрагмы почечной фасцией.[11]
Каждый надпочечник состоит из двух частей, каждая из которых выполняет уникальную функцию. кора надпочечников и внутренний мозговое вещество, оба из которых производят гормоны.[12]
Кора надпочечников
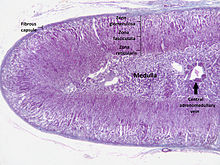
Кора надпочечников - это самый внешний слой надпочечника. Внутри коры есть три слоя, называемые «зонами». Когда рассматривается под микроскопом Каждый слой имеет индивидуальный внешний вид и выполняет свою функцию.[13] В кора надпочечников посвящен производству гормоны, а именно альдостерон, кортизол, и андрогены.[14]
Зона гломерулоза
Крайняя зона коры надпочечников - это зона клубочков. Он лежит непосредственно под фиброзной капсулой железы. Клетки в этом слое образуют овальные группы, разделенные тонкие пряди соединительной ткани от фиброзной капсулы железы и несут широкий капилляры.[15]
Этот слой является основным местом производства альдостерон, а минералокортикоид, под действием фермента альдостерон-синтаза.[16][17] Альдостерон играет важную роль в долгосрочной перспективе. регулирование артериального давления.[18]
Зона фасцикулата
В зона фасцикулата расположена между клубочковой и ретикулярной зонами. Клетки в этом слое отвечают за производство глюкокортикоиды Такие как кортизол.[19] Это самый большой из трех слоев, составляющий почти 80% объема коры.[3] В зоне фасцикулята клетки расположены столбиками, радиально ориентированными к мозговому веществу. Клетки содержат многочисленные липидные капли, обильные митохондрии и комплекс гладкая эндоплазматическая сеть.[15]
Zona reticularis
Самый внутренний кортикальный слой, zona reticularis, лежит непосредственно рядом с мозговым веществом. Он производит андрогены, в основном дегидроэпиандростерон (ДГЭА), Сульфат ДГЭА (DHEA-S) и андростендион (предшественник тестостерон ) в людях.[19] Его маленькие клетки образуют неровные тяжи и скопления, разделенные капиллярами и соединительной тканью. Клетки содержат относительно небольшое количество цитоплазмы и липидных капель и иногда имеют коричневый цвет. липофусцин пигмент.[15]
Медулла
В мозговое вещество надпочечников находится в центре каждого надпочечника и окружен корой надпочечников. В хромаффинные клетки мозгового вещества являются основным источником катехоламины адреналин и норадреналин, выделяемые мозговым веществом. Здесь секретируется примерно 20% норадреналина (норэпинефрин) и 80% адреналина (эпинефрин).[19]
Мозговое вещество надпочечников приводится в движение Симпатическая нервная система через преганглионарные волокна происходящий из грудной отдел спинного мозга, от позвонков T5 – T11.[20] Потому что это иннервируется преганглионарные нервные волокна мозговое вещество надпочечников можно рассматривать как специализированный симпатический ганглий.[20] Однако, в отличие от других симпатических ганглиев, мозговое вещество надпочечников не имеет четких синапсов и выделяет свои секреты непосредственно в кровь.
Кровоснабжение
Надпочечники имеют один из самых высоких показателей кровоснабжения на грамм ткани среди всех органов: до 60 мелкие артерии может попасть в каждую железу.[21] Каждый надпочечник обычно кровоснабжает три артерии:[8]
- В верхняя надпочечная артерия, филиал нижняя диафрагмальная артерия
- В средняя надпочечная артерия, прямое отделение брюшная аорта
- В нижняя надпочечная артерия, филиал почечная артерия
Эти кровеносные сосуды снабжают сеть мелких артерий в капсуле надпочечников. Тонкие тяжи капсулы входят в железы, разнося к ним кровь.[8]
Венозная кровь выводится из желез надпочечные вены, обычно по одному на каждую железу:[8]
- В правая надпочечная вена стекает в нижняя полая вена
- В левая надпочечная вена стекает влево почечная вена или слева нижняя диафрагмальная вена.
Центральная адреномедуллярная вена в мозговом веществе надпочечников - это необычный тип кровеносных сосудов. Его структура отличается от других жил тем, что гладкая мышца в его туника СМИ (средний слой сосуда) расположен заметными продольно ориентированными пучками.[3]
Изменчивость
Надпочечники могут вообще не развиваться или могут слиться по средней линии за спиной. аорта.[12] Они связаны с другими врожденные аномалии, например, отказ почек в развитии или сращение почек.[12] Железа может развиваться при частичном или полном отсутствии коры головного мозга или может развиваться в необычном месте.[12]
Функция

Надпочечник выделяет ряд различных гормонов, которые метаболизируются ферменты либо внутри железы, либо в других частях тела. Эти гормоны участвуют в ряде важных биологических функций.[23]
Кортикостероиды
Кортикостероиды представляют собой группу стероидных гормонов, вырабатываемых корой надпочечников, от которой они и названы.[24]
- Минералокортикоиды, такие как альдостерон регулируют солевой («минеральный») баланс и объем крови.[25]
- Глюкокортикоиды, такие как кортизол влияют на скорость метаболизма белков, жиров и сахаров («глюкозы»).[26]
- Андрогены, такие как дегидроэпиандростерон.
- Минералокортикоиды
Надпочечник производит альдостерон, а минералокортикоид, что важно в регулировании солевого («минерального») баланса и объем крови. В почках альдостерон действует на дистальные извитые канальцы и сборные каналы за счет увеличения реабсорбции натрий и выведение ионов калия и водорода.[18] Альдостерон отвечает за реабсорбцию около 2% отфильтрованных клубочковый фильтрат.[27] Задержка натрия также является ответом дистального отдела толстой кишки и потовых желез на стимуляцию рецептора альдостерона. Ангиотензин II и внеклеточный калий являются двумя основными регуляторами производства альдостерона.[19] Количество натрия в организме влияет на внеклеточный объем, который, в свою очередь, влияет на артериальное давление. Следовательно, влияние альдостерона на задержку натрия важно для регуляции артериального давления.[28]
- Глюкокортикоиды
Кортизол это главный глюкокортикоид в людях. У видов, не вырабатывающих кортизол, эту роль играют кортикостерон вместо. Глюкокортикоиды оказывают большое влияние на метаболизм. Как следует из их названия, они увеличивают уровень циркуляции глюкоза. Это результат увеличения мобилизации аминокислоты от белка и стимуляции синтез глюкозы из этих аминокислот в печени. Кроме того, они повышают уровень свободные жирные кислоты, которые клетки могут использовать в качестве альтернативы глюкозе для получения энергии. Глюкокортикоиды также обладают эффектами, не связанными с регуляцией уровня сахара в крови, включая подавление иммунной системы и мощный противовоспалительное средство эффект. Кортизол снижает способность остеобласты для производства новой костной ткани и уменьшения всасывания кальция в желудочно-кишечный тракт.[28]
Надпочечники секретируют базальный уровень кортизола, но также могут производить выбросы гормона в ответ на адренокортикотропный гормон (ACTH) из передний гипофиз. Кортизол выделяется неравномерно в течение дня - его концентрация в крови наиболее высока ранним утром и минимальна вечером в результате циркадный ритм секреции АКТГ.[28] Кортизон неактивный продукт действия фермента 11β-HSD на кортизол. Реакция, катализируемая 11β-HSD, обратима, что означает, что он может превращать введенный кортизон в кортизол, биологически активный гормон.[28]
- Формирование

Все кортикостероид гормоны делятся холестерин как общий предшественник. Поэтому первый шаг в стероидогенез поглощение или синтез холестерина. Клетки, вырабатывающие стероидные гормоны, могут приобретать холестерин двумя путями. Основным источником является холестерин, поступающий с пищей, который переносится через кровь в виде эфиры холестерина в липопротеины низкой плотности (ЛПНП). ЛПНП попадает в клетки через рецептор-опосредованного эндоцитоза. Другой источник холестерина - синтез в клетках. эндоплазматический ретикулум. Синтез может компенсировать аномально низкий уровень ЛПНП.[4] в лизосома сложные эфиры холестерина превращаются в свободный холестерин, который затем используется для стероидогенеза или сохраняется в клетке.[29]
В начальной стадии превращения холестерина в стероидные гормоны участвует ряд ферментов цитохром P450 семьи, которые расположены во внутренней мембране митохондрии. Транспортировке холестерина от внешней к внутренней мембране способствует стероидогенный белок острой регуляции и является лимитирующей стадией синтеза стероидов.[29]
Слои надпочечников различаются по функциям, каждый из которых имеет разные ферменты, которые производят разные гормоны из общего предшественника.[4] Первым ферментативным шагом в производстве всех стероидных гормонов является расщепление боковой цепи холестерина, реакция, которая формирует прегненолон как продукт и катализируется ферментом P450scc, также известный как холестерин десмолаза. После производства прегненолона определенные ферменты каждого кортикального слоя дополнительно модифицируют его. Ферменты, участвующие в этом процессе, включают митохондрии и микросомальный P450s и гидроксистероиддегидрогеназы. Обычно для образования функциональных гормонов требуется ряд промежуточных этапов, на которых прегненолон модифицируют несколько раз.[5] Ферменты, которые катализируют реакции в этих метаболических путях, участвуют в ряде эндокринных заболеваний. Например, наиболее распространенная форма врожденная гиперплазия надпочечников развивается в результате дефицита 21-гидроксилаза, фермент, участвующий в промежуточной стадии производства кортизола.[30]
- Регулирование
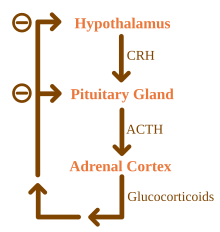
Глюкокортикоиды находятся под регулирующим влиянием ось гипоталамус-гипофиз-надпочечники (HPA). Синтез глюкокортикоидов стимулируется адренокортикотропный гормон (АКТГ), гормон, выделяемый в кровоток передний гипофиз. В свою очередь, производство АКТГ стимулируется присутствием кортикотропин-рилизинг гормон (CRH), который выделяется нейронами гипоталамус. АКТГ сначала действует на клетки надпочечников, увеличивая уровни StAR в клетках, а затем всех стероидогенных ферментов P450. Ось HPA является примером системы отрицательной обратной связи, в которой кортизол сам действует как прямой ингибитор синтеза как CRH, так и ACTH. Ось HPA также взаимодействует с иммунной системой за счет увеличения секреции АКТГ в присутствии определенных молекул воспалительная реакция.[4]
Секреция минералокортикоидов регулируется в основном ренин-ангиотензин-альдостероновая система (РААС), концентрация калий, и в меньшей степени концентрация АКТГ.[4] Датчики артериального давления в юкстагломерулярный аппарат почек выделяют фермент ренин в кровь, что запускает каскад реакций, приводящих к образованию ангиотензин II. Рецепторы ангиотензина в клетках клубочковой оболочки узнают вещество и при связывании стимулируют высвобождение альдостерон.[31]
Андрогены
Ячейки в zona reticularis надпочечников вырабатывают мужские половые гормоны, или андрогены, наиболее важным из которых является DHEA. Как правило, эти гормоны не оказывают общего воздействия на мужской организм и превращаются в более сильные андрогены, такие как тестостерон и DHT или чтобы эстрогены (женские половые гормоны) в гонады, действуя таким образом как промежуточный метаболизм.[32]
Катехоламины
В первую очередь упоминается в США как адреналин и норэпинефрин, адреналин и норадреналин находятся катехоламины, вода соединения которые имеют структуру, состоящую из катехол группа и аминовая группа. Надпочечники отвечают за большую часть циркулирующего в организме адреналина, но только за небольшое количество циркулирующего норадреналина.[23] Эти гормоны выделяются мозговым веществом надпочечников, которое содержит плотную сеть кровеносных сосудов. Адреналин и норадреналин действуют на адренорецепторы по всему телу, с эффектами, которые включают повышение артериального давления и частоты сердечных сокращений.[23] действия адреналина и норадреналина ответственны за борьба или бегство ответ, характеризующийся учащением дыхания и частоты сердечных сокращений, повышением артериального давления и сужением кровеносных сосудов во многих частях тела.[33]
- Формирование
Катехоламины продуцируются в хромаффинных клетках мозгового вещества надпочечников из тирозин, заменимая аминокислота, полученная из пищевых продуктов или произведенная из фенилаланин в печени. Фермент тирозингидроксилаза превращает тирозин в L-ДОПА на первом этапе синтеза катехоламинов. L-ДОПА затем преобразуется в дофамин прежде чем его можно будет превратить в норадреналин. в цитозоль, норадреналин превращается в адреналин под действием фермента фенилэтаноламин N-метилтрансфераза (ПНМТ) и хранится в гранулах. Глюкокортикоиды, продуцируемые в коре надпочечников, стимулируют синтез катехоламинов за счет повышения уровня тирозингидроксилазы и PNMT.[4][13]
Высвобождение катехоламинов стимулируется активацией Симпатическая нервная система. Челюстные нервы из Симпатическая нервная система иннервируют мозговое вещество надпочечника. При активации он вызывает высвобождение катехоламинов из накопительных гранул, стимулируя открытие кальциевые каналы в клеточной мембране.[34]
Экспрессия генов и белков
Вчеловеческий геном включает около 20000 генов, кодирующих белок, и 70% из нихгены выражены в нормальных надпочечниках взрослого человека.[35][36] Только около 250 генов экспрессируются более специфично в надпочечниках по сравнению с другими органами и тканями. Гены, специфичные для надпочечников с наивысшим уровнем экспрессии, включают членов цитохром P450 надсемейство ферментов. Соответствующие белки экспрессируются в различных отделах надпочечников, таких как CYP11A1, HSD3B2 и FDX1 участвует в стероидный гормон синтез и экспрессируется в слоях корковых клеток, и PNMT и DBH участвует в норадреналин и адреналин синтез и выражается в мозговом веществе.[37]
Разработка
Надпочечники состоят из двух гетерогенных типов тканей. В центре находится мозговое вещество надпочечников, который производит адреналин и норадреналин и выпускает их в кровоток, как часть Симпатическая нервная система. Вокруг продолговатого мозга кора, который производит множество стероидные гормоны. Эти ткани происходят из разных эмбриологический предшественники и имеют различные внутриутробное развитие пути. Кора надпочечника происходит от мезодерма, тогда как мозговое вещество происходит от нервный гребень, который из эктодермальный источник.[12]
Надпочечники у новорожденного ребенка намного больше в пропорции к размеру тела, чем у взрослого.[38] Например, в возрасте трех месяцев железы в четыре раза больше почек. Размер желез относительно уменьшается после рождения, в основном из-за сжатия коры. Кора головного мозга, которая почти полностью исчезает к возрасту 1 года, снова развивается с 4–5 лет. При рождении железы весят около 1 г.[12] и развиваться до взрослого веса около 4 граммов каждый.[28] У плода железы впервые обнаруживаются после шестой недели развития.[12]
Кора
Ткань коры надпочечников происходит из промежуточная мезодерма. Впервые появляется через 33 дня после оплодотворение, показывает производство стероидных гормонов способности к восьмой неделе и быстро растет в течение первого триместра беременности. Кора надпочечников плода отличается от своего взрослого аналога, поскольку она состоит из двух отдельных зон: внутренней «фетальной» зоны, которая несет большую часть активности производства гормонов, и внешней «дефинитивной» зоны, которая находится в пролиферативный фаза. Зона плода производит большое количество надпочечников. андрогены (мужские половые гормоны), которые используются плацента за эстроген биосинтез.[39] Корковое развитие надпочечников регулируется в основном АКТГ, гормон, производимый гипофиз это стимулирует кортизол синтез.[40] Во время середины беременности зона плода занимает большую часть объема коры и вырабатывает 100–200 мг / день DHEA-S, андроген и предшественник как андрогенов, так и эстрогены (женские половые гормоны).[41] Гормоны надпочечников, особенно глюкокортикоиды такие как кортизол, необходимы для пренатального развития органов, особенно для созревания легкие. После рождения надпочечник уменьшается в размере из-за быстрого исчезновения зоны плода с соответствующим уменьшением секреции андрогенов.[39]
Адренарх
В раннем детстве синтез и секреция андрогенов остаются на низком уровне, но за несколько лет до полового созревания (в возрасте 6–8 лет) происходят изменения как в анатомических, так и в функциональных аспектах выработки кортикальных андрогенов, что приводит к увеличению секреции стероидов. DHEA и DHEA-S. Эти изменения являются частью процесса, называемого адренархе, который был описан только у людей и некоторых других приматов. Адренархе не зависит от АКТГ или же гонадотропины и коррелирует с прогрессирующим утолщением zona reticularis слой коры. Функционально адренархе является источником андрогенов для развития подмышечных и лобковых волос до начала полового созревания.[42][43]
Медулла
Мозговое вещество надпочечников происходит от клетки нервного гребня, которые происходят из эктодерма слой эмбрион. Эти клетки мигрировать из исходного положения и агрегатируются в непосредственной близости от дорсальная аорта, примитивный кровеносный сосуд, который активирует дифференцировку этих клеток за счет высвобождения белков, известных как БМП. Затем эти клетки претерпевают вторую миграцию из дорсальной аорты с образованием мозгового вещества надпочечников и других органов Симпатическая нервная система.[44] Клетки мозгового вещества надпочечников называются хромаффинные клетки потому что они содержат гранулы, окрашивающие хром соли, характерные не для всех симпатических органов. Глюкокортикоиды Когда-то считалось, что продуцируемые в коре надпочечников ответственны за дифференцировку хромаффинных клеток. Более поздние исследования показывают, что БМП-4 Секретирование в тканях надпочечников является основной причиной этого, и что глюкокортикоиды играют роль только в последующем развитии клеток.[45]
Клиническое значение
Нормальная функция надпочечников может быть нарушена такими состояниями, как инфекции, опухоли, генетические нарушения и аутоиммунные заболевания, или как побочный эффект лечебной терапии. Эти нарушения влияют на железу либо напрямую (как при инфекциях или аутоиммунных заболеваниях), либо в результате нарушения регуляции выработки гормонов (как при некоторых типах синдром Кушинга ), что приводит к избытку или недостаточности гормонов надпочечников и связанным с ними симптомам.
Избыточное производство кортикостероидов
синдром Кушинга
синдром Кушинга является проявлением избытка глюкокортикоидов. Это может быть результатом длительного лечения глюкокортикоидами или вызвано основным заболеванием, которое вызывает изменения в Ось HPA или производство кортизола. Причины можно разделить на АКТГ -зависимый или АКТГ-независимый. Самая частая причина эндогенный Синдром Кушинга - это аденома гипофиза что вызывает чрезмерное производство АКТГ. Заболевание вызывает широкий спектр признаков и симптомов, включая ожирение, диабет, повышенное кровяное давление, чрезмерное оволосение тела (гирсутизм ), остеопороз, депрессия и, что особенно характерно, растяжки в коже, вызванной ее прогрессирующим истончением.[4][6]
Первичный альдостеронизм
Когда клубочковая оболочка производит избыток альдостерон, результат первичный альдостеронизм. Причины этого состояния двусторонние. гиперплазия (чрезмерный рост ткани) желез или продуцирование альдостерона аденомы (состояние называется Синдром Конна ). Первичный альдостеронизм вызывает гипертонию и электролит дисбаланс, увеличение калий истощение удержания натрия.[6]
Надпочечниковая недостаточность
Надпочечниковая недостаточность (дефицит глюкокортикоиды ) встречается примерно у 5 из 10 000 населения в целом.[6] Заболевания классифицируются как первичная надпочечниковая недостаточность (включая Болезнь Эддисона и генетические причины) напрямую влияют на кору надпочечников. Если проблема, которая влияет на гипоталамо-гипофизарно-надпочечниковая система возникает вне железы, это вторичная надпочечниковая недостаточность.
Болезнь Эддисона

Болезнь Аддисона относится к первичному гипоадренализму, который представляет собой дефицит продукции глюкокортикоидов и минералокортикоидов надпочечниками. В западном мире болезнь Аддисона чаще всего аутоиммунный состояние, в котором организм производит антитела против клеток коры надпочечников. Во всем мире болезнь чаще вызывается инфекциями, особенно от туберкулез. Отличительной особенностью болезни Аддисона является гиперпигментация кожи, которая проявляется другими неспецифическими симптомами, такими как усталость.[4]
Осложнение, наблюдаемое при нелеченной болезни Аддисона и других типах первичной недостаточности надпочечников, - это надпочечниковый кризис, а неотложная медицинская помощь при которых низкие уровни глюкокортикоидов и минералокортикоидов приводят к гиповолемический шок и такие симптомы, как рвота и жар. Кризис надпочечников может постепенно привести к ступор и кома.[4] Лечение надпочечникового кризиса включает в себя применение гидрокортизон инъекции.[46]
Вторичная надпочечниковая недостаточность
При вторичной недостаточности надпочечников нарушение функции гипоталамо-гипофизарно-надпочечниковая система приводит к снижению стимуляции коры надпочечников. Помимо подавления оси глюкокортикоидами, наиболее частой причиной вторичной недостаточности надпочечников являются опухоли, которые влияют на выработку адренокортикотропный гормон (ACTH) гипофиз.[6] Этот тип надпочечниковой недостаточности обычно не влияет на выработку минералокортикоиды, которые регулируются ренин-ангиотензиновая система вместо.[4]
Врожденная гиперплазия надпочечников
Врожденная гиперплазия надпочечников это врожденное заболевание в котором мутации ферментов, вырабатывающих стероидные гормоны, приводят к дефициту глюкокортикоидов и нарушению работы цепи отрицательной обратной связи Ось HPA. По оси HPA кортизол (глюкокортикоид) подавляет высвобождение CRH и АКТГ, гормоны, которые, в свою очередь, стимулируют синтез кортикостероидов.Поскольку кортизол не может быть синтезирован, эти гормоны выделяются в больших количествах и вместо этого стимулируют выработку других стероидов надпочечников. Наиболее частая форма врожденной гиперплазии надпочечников возникает из-за: 21-гидроксилаза дефицит. 21-гидроксилаза необходима для производства как минералокортикоидов, так и глюкокортикоидов, но не андрогены. Следовательно, стимуляция коры надпочечников АКТГ вызывает высвобождение чрезмерного количества андрогены надпочечников, что может привести к развитию неоднозначных гениталии и вторичные половые признаки.[30]
Опухоли надпочечников

Опухоли надпочечников обычно встречаются как инциденталомы, непредвиденный бессимптомный опухоли найденный в течение медицинская визуализация. Они встречаются примерно в 3,4% Компьютерная томография,[7] и в большинстве случаев они доброкачественные аденомы.[48] Карциномы надпочечников очень редки, с заболеваемость 1 случай на миллион в год.[4]
Феохромоцитомы опухоли мозгового вещества надпочечников, возникающие из хромаффинные клетки. Они могут вызывать множество неспецифических симптомов, в том числе головные боли, потливость, беспокойство и т. Д. сердцебиение. Общие признаки включают: гипертония и тахикардия. Хирургия, особенно надпочечников лапароскопия, является наиболее распространенным методом лечения небольших феохромоцитом.[49]
История
Бартоломео Евстачи итальянскому анатому приписывают первое описание надпочечников в 1563-15 годах.[50][51] Однако эти публикации были частью папская библиотека и не получил общественного внимания, которое сначала было Каспар Бартолин Старший иллюстрации 1611 г.[51]
Надпочечники названы в честь их расположения относительно почек. Термин «надпочечники» происходит от объявление- (Латинское «рядом») и Renes (Латинское «почка»).[52] Точно так же «надпочечник», как его называют Жан Риолан Младший в 1629 г., происходит от латинский выше (латинский: "над") и Renes (латинский: почка). Надпочечная природа желез не была полностью принята до 19 века, поскольку анатомы прояснили бесконтактную природу желез и их вероятную секреторную роль - до этого были некоторые споры относительно того, действительно ли железы надпочечников или являются частью их. почка.[51]
Одна из самых известных работ по надпочечникам появилась в 1855 году с публикацией О конституциональных и местных эффектах заболевания супраренальной капсулы, английский врач Томас Аддисон. В своей монографии Аддисон описал то, что французский врач Джордж Труссо позже назовет Болезнь Эддисона, эпоним, который до сих пор используется для обозначения состояния надпочечниковая недостаточность и связанные с ним клинические проявления.[53] В 1894 году английские физиологи Джордж Оливер и Эдвард Шафер изучили действие экстрактов надпочечников и наблюдали их прессор последствия. В последующие десятилетия несколько врачей экспериментировали с экстрактами коры надпочечников для лечения болезни Аддисона.[50] Эдвард Кэлвин Кендалл, Филип Хенч и Тадеуш Райхштейн затем были награждены 1950 Нобелевская премия по физиологии и медицине за открытия, касающиеся структуры и действия гормонов надпочечников.[54]
Смотрите также
Рекомендации
- ^ Сантулли Г. MD (2015). Надпочечники: от патофизиологии к клиническим данным. Издательство Nova Science, Нью-Йорк, штат Нью-Йорк. ISBN 978-1-63483-570-1.
- ^ "Надпочечник". Medline Plus / Словарь Merriam-Webster. Получено 11 февраля 2015.
- ^ а б c Росс М, Павлина В (2011). Гистология: текст и атлас (6-е изд.). Липпинкотт Уильямс и Уилкинс. стр.708, 780. ISBN 978-0-7817-7200-6.
- ^ а б c d е ж грамм час я j k л м Мелмед, S; Полонский, К.С.; Ларсен, PR; Кроненберг, HM (2011). Учебник эндокринологии Уильямса (12-е изд.). Сондерс. ISBN 978-1437703245.
- ^ а б Миллер, WL; Auchus, RJ (2011). «Молекулярная биология, биохимия и физиология стероидогенеза человека и его нарушений». Эндокринные обзоры. 32 (1): 81–151. Дои:10.1210 / er.2010-0013. ЧВК 3365799. PMID 21051590.
- ^ а б c d е Лонго, Д; Фаучи, А; Каспер, Д; Хаузер, S; Джеймсон, Дж; Лоскальцо, Дж (2012). Принципы внутренней медицины Харрисона (18-е изд.). Нью-Йорк: Макгроу-Хилл. ISBN 978-0071748896.
- ^ а б Ниман, Л.К. (2010). «Обращение к пациенту с инциденталомой надпочечника». Журнал клинической эндокринологии и метаболизма. 95 (9): 4106–13. Дои:10.1210 / jc.2010-0457. ЧВК 2936073. PMID 20823463.
- ^ а б c d е Томас, под редакцией Пола; Молекулярная школа; Австралия, Биомедицинские науки, Университет Аделаиды, Аделаида, Южная Австралия (2013 г.). Развитие и заболевание эндокринных желез. Берлингтон: Elsevier Science. п. 241. ISBN 9780123914545.CS1 maint: дополнительный текст: список авторов (связь)
- ^ Антонио Карлос А. Вестфален и Бонни Н. Джо (2006). «КТ и МРТ новообразований надпочечников». Appl Radiol. 35 (8): 10–26.
- ^ О'Хара, А. Манро Невилл, Майкл Дж. (1982). Патология и биология коры надпочечников человека - комплексный подход. Springer London. стр. Глава 4: Структура коры взрослого мозга. ISBN 9781447113171.
- ^ а б Мур К.Л., Далли А.Ф., Агур А.М. (2013). Клинически ориентированная анатомия, 7-е изд.. Липпинкотт Уильямс и Уилкинс. С. 294, 298. ISBN 978-1-4511-8447-1.
- ^ а б c d е ж грамм Кей, Саундра. "Надпочечники". Medscape. Получено 1 августа 2015.
- ^ а б Уайтхед, Шафран А .; Насси, Стивен (2001). Эндокринология: комплексный подход. Оксфорд: BIOS. п. 122. ISBN 978-1-85996-252-7.
- ^ Джеффрис, Уильям МакК (2004). Безопасное использование кортизола. Спрингфилд, штат Иллинойс: Чарльз С. Томас. ISBN 978-0-398-07500-2.
- ^ а б c Янг Б., Вудфорд П., О'Дауд Г. (2013). Функциональная гистология Уитера: текстовый и цветной атлас (6-е изд.). Эльзевир. п. 329. ISBN 978-0702047473.
- ^ Curnow KM, Tusie-Luna MT, Pascoe L, Natarajan R, Gu JL, Nadler JL, White PC (октябрь 1991 г.). «Продукт гена CYP11B2 необходим для биосинтеза альдостерона в коре надпочечников человека» (PDF). Мол. Эндокринол. 5 (10): 1513–1522. Дои:10.1210 / mend-5-10-1513. PMID 1775135.
- ^ Чжоу М., Гомес-Санчес CE (июль 1993 г.). «Клонирование и экспрессия крысиного варианта кДНК цитохрома P-450 11 бета-гидроксилазы / альдостерон-синтазы (CYP11B2)». Biochem Biophys Res Commun. 194 (1): 112–117. Дои:10.1006 / bbrc.1993.1792. PMID 8333830.
- ^ а б Marieb, EN; Хоэн, К. (2012). Анатомия и физиология человека (9-е изд.). Пирсон. п. 629. ISBN 978-0321743268.
- ^ а б c d Dunn R. B .; Kudrath W .; Passo S.S .; Уилсон Л.Б. (2011). «10». Kaplan USMLE Step 1 Конспект лекции по физиологии. С. 263–289.
- ^ а б Сапру, Хредай Н .; Сигел, Аллан (2007). Essential Neuroscience. Хагерстаун, Мэриленд: Липпинкотт Уильямс и Уилкинс. ISBN 978-0-7817-9121-2.
- ^ Мирилас П., Скандалакис Дж. Э., Колборн Г. Л., Вайдман Т. А., Фостер Р. С., Кингснорт А., Скандалакис Л. Дж., Скандалакис П. Н. (2004). Хирургическая анатомия: эмбриологическая и анатомическая основа современной хирургии. McGraw-Hill Professional Publishing. ISBN 978-960-399-074-1.
- ^ «OpenStax CNX». cnx.org. Получено 1 августа 2015.
- ^ а б c Бриттон, редакторы Ники Р. Колледж, Брайан Р. Уокер, Стюарт Х. Ральстон; проиллюстрировано Робертом (2010). Принципы Дэвидсона и практика медицины (21-е изд.). Эдинбург: Черчилль Ливингстон / Эльзевьер. С. 768–778. ISBN 978-0-7020-3085-7.
- ^ «Кортикостероид». TheFreeDictionary. Получено 23 сентября 2015.
- ^ Мариеб Анатомия и физиология человека 9-е издание, глава: 16, страница: 629, номер вопроса: 14
- ^ «Кортикостероид». TheFreeDictionary. Получено 23 сентября 2015.
- ^ Шервуд, Лорали (2001). Физиология человека: от клеток к системам. Пасифик Гроув, Калифорния: Брукс / Коул. ISBN 978-0-534-56826-9. OCLC 43702042.
- ^ а б c d е Бор, WF .; Boulapep, EL. (2012). Медицинская физиология (2-е изд.). Филадельфия: Сондерс. ISBN 978-1437717532.
- ^ а б Миллер, WL; Бозе, HS (2011). «Ранние этапы стероидогенеза: внутриклеточный оборот холестерина». Журнал липидных исследований. 52 (12): 2111–2135. Дои:10.1194 / мл. R016675. ЧВК 3283258. PMID 21976778.
- ^ а б Чармандари, E; Брук, CG; Хиндмарш, ПК (2004). «Классическая врожденная гиперплазия надпочечников и половое созревание». Европейский журнал эндокринологии. 151 (Дополнение 3): 77–82. CiteSeerX 10.1.1.613.6853. Дои:10.1530 / eje.0.151U077. PMID 15554890. Архивировано из оригинал 4 февраля 2015 г.
- ^ Кроули, SD; Коффман, TM (2012). «Последние достижения в области ренин-ангиотензиновой системы». Экспериментальные исследования клеток. 318 (9): 1049–1056. Дои:10.1016 / j.yexcr.2012.02.023. ЧВК 3625040. PMID 22410251.
- ^ Холл JE, Guyton AC (2010). Учебник медицинской физиологии Гайтона и Холла, 12-е издание. Сондерс. ISBN 978-1416045748.
- ^ Генри Глейтман, Алан Дж. Фридлунд и Даниэль Райсберг (2004). Психология (6 изд.). W. W. Norton & Company. ISBN 978-0-393-97767-7.
- ^ Гарсия, АГ; Гарсиа де Диего, AM; Gandía, L; Borges, R; Гарсиа Санчо, Дж (2006). «Передача сигналов кальция и экзоцитоз в хромаффинных клетках надпочечников». Физиологические обзоры. 86 (4): 1093–1131. Дои:10.1152 / Physrev.00039.2005. PMID 17015485.
- ^ «Протеом человека в надпочечниках - Атлас белков человека». www.proteinatlas.org. Получено 21 сентября 2017.
- ^ Улен, Матиас; Фагерберг, Линн; Hallström, Björn M .; Линдског, Сесилия; Оксволд, Пер; Мардиноглу, Адиль; Сивертссон, Аса; Кампф, Кэролайн; Шёстедт, Эвелина (23 января 2015 г.). «Тканевая карта протеома человека». Наука. 347 (6220): 1260419. Дои:10.1126 / science.1260419. ISSN 0036-8075. PMID 25613900. S2CID 802377.
- ^ Бергман, Юлия; Ботлинг, Йохан; Фагерберг, Линн; Hallström, Björn M .; Джуреинович, Дияна; Улен, Матиас; Понтен, Фредрик (1 февраля 2017 г.). «Протеом надпочечников человека, определенный с помощью транскриптомики и профилирования на основе антител». Эндокринология. 158 (2): 239–251. Дои:10.1210 / en.2016-1758. ISSN 0013-7227. PMID 27901589.
- ^ Barwick, T.D .; Malhotra, A .; Webb, J.A.W .; Savage, M.O .; Резнек, Р.Х. (сентябрь 2005 г.). «Эмбриология надпочечников и ее значение для диагностической визуализации». Клиническая радиология. 60 (9): 953–959. Дои:10.1016 / j.crad.2005.04.006. PMID 16124976.
- ^ а б Ишимото Х., Яффе РБ (2011). «Развитие и функции коры надпочечников плода человека: ключевой компонент фето-плацентарной единицы». Эндокринные обзоры. 32 (3): 317–355. Дои:10.1210 / er.2010-0001. ЧВК 3365797. PMID 21051591.
- ^ Хефлих А, Белохубий М (2009). «Механизмы роста надпочечников: интеграция сигналов с помощью киназ, регулируемых внеклеточными сигналами 1/2».. Журнал молекулярной эндокринологии. 42 (3): 191–203. Дои:10.1677 / JME-08-0160. PMID 19052254.
- ^ Мезиано С., Яффе РБ (1997). «Биология развития и функциональная биология коры надпочечников плода приматов». Эндокринные обзоры. 18 (3): 378–403. Дои:10.1210 / edrv.18.3.0304. PMID 9183569.
- ^ Хорнсби, П.Дж. (2012). «Адренархе: биологическая перспектива клетки». Журнал эндокринологии. 214 (2): 113–119. Дои:10.1530 / JOE-12-0022. PMID 22573830.
- ^ Рег, Дж; Рейни, WE (2012). «Стероидный метаболом адренархе». Журнал эндокринологии. 214 (2): 133–143. Дои:10.1530 / JOE-12-0183. ЧВК 4041616. PMID 22715193.
- ^ Хубер К. (2006). «Линия симпатоадреналовых клеток: спецификация, диверсификация и новые перспективы». Биология развития. 298 (2): 335–343. Дои:10.1016 / j.ydbio.2006.07.010. PMID 16928368.
- ^ Ансикер К., Хубер К., Шобер А., Калхейм С. (2013). «Решенные и открытые вопросы в развитии хромаффинных клеток». Механизмы развития. 130 (6–8): 324–329. Дои:10.1016 / j.mod.2012.11.004. PMID 23220335.
- ^ Информационный бюллетень по неотложной помощи гидрокортизона для персонала скорой помощи Фонд гипофиза
- ^ Данные и ссылки для круговой диаграммы находятся по адресу страница описания файла на Викискладе?
- ^ Mantero, F; Терцоло, М; Арнальди, G; Оселла, G; Масини, AM; Али, А; Джовагнетти, М; Опочер, Г; Анджели, А (2000). «Исследование инциденталомы надпочечников в Италии. Исследовательская группа по опухолям надпочечников Итальянского общества эндокринологов». Журнал клинической эндокринологии и метаболизма. 85 (2): 637–644. Дои:10.1210 / jcem.85.2.6372. PMID 10690869.
- ^ Martucci, VL; Пакак, К. (2014). «Феохромоцитома и параганглиома: диагностика, генетика, ведение и лечение». Текущие проблемы при раке. 38 (1): 7–41. Дои:10.1016 / j.currproblcancer.2014.01.001. ЧВК 3992879. PMID 24636754.
- ^ а б Шмидт, JE (1959). Медицинские открытия: кто и когда. Томас. С. 9–10.
- ^ а б c О'Хара, А. Манро Невилл, Майкл Дж. (2012). Патология и биология коры надпочечников человека - комплексный подход. Лондон: Springer London. С. Глава 2: Исторические аспекты. ISBN 978-1447113171.
- ^ "Что такое надпочечники?". About.com. Получено 18 сентября 2013.
- ^ Пирс, Дж. М. (2004). "Томас Аддисон (1793–1860)". Журнал Королевского медицинского общества. 97 (6): 297–300. Дои:10.1258 / jrsm.97.6.297. ЧВК 1079500. PMID 15173338.
- ^ "Нобелевская премия по физиологии и медицине 1950 г.". Нобелевский фонд. Получено 10 февраля 2015.
внешняя ссылка
- Надпочечники в Атласе белков человека
- Энциклопедия MedlinePlus: 002219
- Гистология надпочечников
- Анатомические атласы - Микроскопическая анатомия, таблица 15.292 - "Надпочечник"
- Гистологическое изображение: 14501 лоа - Система обучения гистологии в Бостонском университете
- Анатомическое фото: 40: 03-0105 в Медицинском центре SUNY Downstate - "Задняя брюшная стенка: забрюшинный жир и надпочечники"
- Надпочечник из Университета штата Колорадо
- Изображение в разрезе: pembody / body8a —Лаборатория пластики Венского медицинского университета
