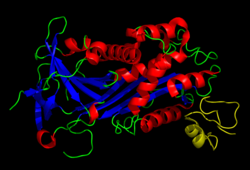
Витронектин - Vitronectin
Витронектин (VTN или же VN) это гликопротеин из семейство гемопексинов который в изобилии содержится в сыворотке, внеклеточный матрикс и кость.[5] У людей это кодируется VTN ген.[6][7]
Витронектин связывается с интегрин альфа-V бета-3 и таким образом продвигает клеточная адгезия и распространение. Он также подавляет повреждающее мембрану действие терминального цитолитического путь комплемента и связывается с несколькими змеи (ингибиторы сериновых протеаз). Это секретируемый белок, существующий либо в одноцепочечной форме, либо в двухцепочечной форме с обрезанными цепями, удерживаемых вместе дисульфидной связью.[6] Предполагается, что витронектин участвует в гемостаз[8] и опухоль злокачественная опухоль.[9][10]
Структура
Витронектин - это гликопротеин 75 кДа, состоящий из 459 аминокислота остатки. Около одной трети протеина молекулярная масса состоит из углеводы. Иногда белок расщепляется после аргинин 379, чтобы произвести двухцепочечный витронектин, где две части связаны дисульфидная связь. Никакая структура с высоким разрешением пока не определена экспериментально, за исключением N-концевого домена.
Белок состоит из трех домены:
- В N-концевой Соматомедин B домен (1-39)
- Центральные домены с гемопексин гомология (131-342)
- А C-терминал домен (остатки 347-459) также с гомологией гемопексина.
Сообщалось о нескольких структурах домена Somatomedin B. Первоначально белок был кристаллизован в комплексе с одним из его физиологических партнеров по связыванию: Ингибитор активатора плазминогена-1 (PAI-1) и структура, решенная для этого комплекса.[11] Впоследствии две группы сообщили Структуры ЯМР домена.[12][13]
Домен соматомедина B представляет собой сплошной дисульфидный узел с 4 дисульфидными связями в пределах 35 остатков. Сообщалось о различных дисульфидных конфигурациях для этого домена.[14][15][16] но эта двусмысленность разрешена кристаллической структурой.[16]
Гомологические модели были построены для центрального и С-концевого доменов.[16]
Функция
Домен соматомедина B витронектина связывается с ингибитор активатора плазминогена-1 (PAI-1) и стабилизирует его.[11] Таким образом, витронектин служит для регулирования протеолиза, инициированного плазминоген активация. Кроме того, витронектин входит в состав тромбоциты и, таким образом, участвует в гемостазе. Витронектин содержит последовательность RGD (45-47), которая является сайтом связывания для мембраносвязанных интегрины, например, рецептор витронектина, которые служат для закрепления клеток на внеклеточном матриксе. Домен соматомедина B взаимодействует с рецептор урокиназы, и это взаимодействие вовлечено в миграцию клеток и передачу сигнала. Было показано, что высокие уровни в плазме как PAI-1, так и рецептора урокиназы коррелируют с отрицательным прогнозом для онкологических больных. Адгезия и миграция клеток непосредственно участвуют в развитии рака метастаз, что дает вероятное механистическое объяснение этому наблюдению.
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000109072 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск ансамбля 89: ENSMUSG00000017344 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Борон, Уолтер Ф. и Боулпаэп, Эмиль Л. "Медицинская физиология". Сондерс, 2012, с.1097.
- ^ а б "Entrez Gene: M Vitronectin".
- ^ Дженн Д., Стэнли К.К. (октябрь 1987 г.). «Нуклеотидная последовательность и организация гена человеческого S-белка: повторяющиеся пептидные мотивы в семействе« пексинов »и модель их эволюции». Биохимия. 26 (21): 6735–42. Дои:10.1021 / bi00395a024. PMID 2447940.
- ^ Прейсснер К.Т., Зайфферт Д. (январь 1998 г.). «Роль витронектина и его рецепторов в гемостазе и ремоделировании сосудов». Исследование тромбоза. 89 (1): 1–21. Дои:10.1016 / S0049-3848 (97) 00298-3. PMID 9610756.
- ^ Фельдинг-Хаберманн Б., Череш Д.А. (октябрь 1993 г.). «Витронектин и его рецепторы». Текущее мнение в области клеточной биологии. 5 (5): 864–8. Дои:10.1016 / 0955-0674 (93) 90036-П. PMID 7694604.
- ^ Больно, Элейн М .; Чан, король; Серрат, Мария Ана Духагон; Thomas, Suneetha B .; Винстра, Тимоти Д .; Фаррар, Уильям Л. (2009). «Идентификация витронектина как внешнего индуктора дифференцировки раковых стволовых клеток и образования опухолей». Стволовые клетки. 28 (3): 390–8. Дои:10.1002 / шток.271. ЧВК 3448441. PMID 19998373.
- ^ а б Чжоу А., Хантингтон Дж. А., Панну Н. С., Каррелл Р. В., Рид Р. Дж. (Июль 2003 г.). «Как витронектин связывает PAI-1, чтобы модулировать фибринолиз и миграцию клеток». Структурная биология природы. 10 (7): 541–4. Дои:10.1038 / nsb943. PMID 12808446. S2CID 26086796.
- ^ Камикубо Ю., Де Гузман Р., Крун Дж., Карриден С., Нилс Дж. Г., Черчилль М.Дж., Доусон П., Олдзей С., Ягельска А., Шерага А.А., Лоскутов DJ, Дайсон HJ (Июнь 2004 г.). «Расположение дисульфидных связей в активных формах домена соматомедина B витронектина человека». Биохимия. 43 (21): 6519–34. Дои:10.1021 / bi049647c. PMID 15157085.
- ^ Mayasundari A, Whittemore NA, Serpersu EH, Peterson CB (июль 2004 г.). «Структура раствора N-концевого домена витронектина человека: проксимальные участки, регулирующие фибринолиз и миграцию клеток». Журнал биологической химии. 279 (28): 29359–66. Дои:10.1074 / jbc.M401279200. PMID 15123712.
- ^ Камикубо Ю., Окумура Ю., Loskutoff DJ (июль 2002 г.). «Идентификация дисульфидных связей в рекомбинантном домене соматомедина B человеческого витронектина». Журнал биологической химии. 277 (30): 27109–19. Дои:10.1074 / jbc.M200354200. PMID 12019263.
- ^ Хорн Н.А., Херст Г.Б., Маясундари А., Виттемор Н.А., Серперсу Е.Н., Петерсон С.Б. (август 2004 г.). «Отнесение четырех дисульфидов к N-концевому домену соматомедина B нативного витронектина, выделенного из плазмы человека». Журнал биологической химии. 279 (34): 35867–78. Дои:10.1074 / jbc.M405716200. PMID 15173163.
- ^ а б c Сюй Д., Бабурадж К., Петерсон С.Б., Сюй Ю. (август 2001 г.). «Модель трехмерной структуры витронектина: прогнозы для многодоменного белка из потоков и стыковки». Белки. 44 (3): 312–20. Дои:10.1002 / prot.1096. PMID 11455604.
дальнейшее чтение
- Сингх Б., Су И.С., Рисбек К. (2010). «Витронектин в бактериальном патогенезе: белок-хозяин, используемый для побега комплемента и клеточной инвазии». Мол. Микробиол. 78 (3): 545–60. Дои:10.1111 / j.1365-2958.2010.07373.x. PMID 20807208. S2CID 24516528.
- Сингх Б., Джалалванд Ф., Мёргелин М., Зипфель П., Блом А.М., Рисбек К. (2011). «Белок Е Haemophilus influenzae распознает С-концевой домен витронектина и модулирует комплекс атаки на мембрану». Мол. Микробиол. 81 (1): 80–98. Дои:10.1111 / j.1365-2958.2011.07678.x. PMID 21542857. S2CID 26484037.
- Су YC, Jalalvand F, Mörgelin M, Blom AM, Singh B, Riesbeck K (2013). «Haemophilus influenzae приобретает витронектин через повсеместно распространенный белок F, чтобы подорвать врожденный иммунитет хозяина». Мол. Микробиол. 87 (6): 1245–66. Дои:10,1111 / ммi.12164. PMID 23387957. S2CID 26923730.
внешняя ссылка
- Витронектин в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)