Эндостатин - Endostatin
Эндостатин представляет собой встречающийся в природе С-концевой фрагмент 20 кДа, полученный из коллаген XVIII типа. Сообщается, что он служит антиангиогенный агент, похожий на ангиостатин и тромбоспондин.
Эндостатин - препарат широкого спектра действия. ангиогенез ингибитор и может препятствовать проангиогенному действию факторов роста, таких как основной фактор роста фибробластов (bFGF / FGF-2) и фактор роста эндотелия сосудов (VEGF).[1]
Фон
Эндостатин - эндогенный ингибитор ангиогенеза. Впервые он был обнаружен секретируемым в среде неметастазирующих клеток мыши из гемангиоэндотелиома клеточная линия в 1997 году и впоследствии была обнаружена у человека.[2][3] Он продуцируется протеолитическим расщеплением коллагена XVIII, члена семейства мультиплексинов, который характеризуется нарушениями в тройная спираль создание множественных доменов протеазами, такими как катепсины.[4] Коллаген входит в состав базальных мембран эпителия и эндотелия. Эндостатин, как фрагмент коллагена 18, демонстрирует роль ECM в подавлении неоангиогенез.[2] Проангиогенные и антиангиогенные факторы также могут создаваться протеолизом во время каскадов коагуляции.[5][6][7] Эндогенные ингибиторы ангиогенеза присутствуют как в нормальной, так и в раковой ткани.[8] В целом, эндостатин подавляет многие сигнальные каскады, такие как передача сигналов эфрина, TNF-α и NFκB, а также каскады коагуляции и адгезии.[9] К другим антиангиогенным факторам, полученным из коллагена, относятся аррестен, канстатин, тумстатин, антиангиогенный фрагмент α6 коллагена IV типа и рестин.[10]
Структура
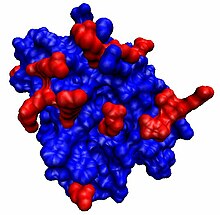
Мономерный эндостатин человека представляет собой глобулярный белок, содержащий две дисульфидные связи: Cys162-302 и Cys264-294.[11] Он плотно сворачивается, имеет цинк-связывающий домен на N-конце белка и имеет высокое сродство к гепарину через основной пластырь из 11 аргинина.[12][13][14] Эндостатин также связывает все протеогликаны гепарансульфата с низким сродством.[15][16] Олигомерный эндостатин (тример или димер) связывается в основном с ламинином базальной пластинки.[17]
Биологическая активность
Исследования in vitro показали, что эндостатин блокирует пролиферацию и организацию эндотелиальных клеток в новые кровеносные сосуды.[18] В исследованиях на животных эндостатин подавлял ангиогенез и рост как первичных опухолей, так и вторичных метастазов.[2]
Механизм
Эндостатин подавляет ангиогенез многими путями, влияющими как на жизнеспособность, так и на движение клеток. Эндостатин подавляет гены контроля клеточного цикла и гены против апоптоза в пролиферирующих эндотелиальных клетках, что приводит к гибели клеток.[19] Эндостатин блокирует экспрессию проангиогенного гена, контролируемую N-концевой киназой c-Jun (JNK), препятствуя активации JNK TNFα.[20] Он снижает рост новых клеток, ингибируя циклин D1. В результате клетки останавливаются во время фазы G1 и вступают в апоптоз.[21][22] Изменение трансдукции сигнала FGF эндостатином ингибирует миграцию эндотелиальных клеток за счет нарушения адгезий клеточного матрикса, межклеточных адгезий и реорганизации цитоскелета.[23] Связывая интегрин α5β1 с клетками эндотелия, он ингибирует сигнальные пути киназ Ras и Raf и снижает активность ERK-1 и p38.[24] Связывание эндостатина и кластеризация интегринов вызывает совместную локализацию с кавеолином-1 и активирует нерецепторные тирозинкиназы семейства Src, участвующие в регуляции пролиферации, дифференцировки и подвижности клеток.[25][26][27][28] Другие рецепторные взаимодействия включают рецептор VEGF-R2 / KDR / Flk-1 на эндотелиальных клетках пупочной вены человека.[29]
Эндостатин может препятствовать активности некоторых металлопротеиназа.[30] Несколько исследований были сосредоточены на последующих эффектах приема эндостатина. Эти исследования показали, что эндостатин может значительно влиять на 12% генов, используемых эндотелиальными клетками человека. Хотя передача сигналов эндостатина может влиять на это огромное количество генов, последующие воздействия оказываются на удивление ограниченными. Прием эндостатина, по-видимому, влияет только на ангиогенез, происходящий из патогенных источников, таких как опухоли. На процессы, связанные с ангиогенезом, такие как заживление ран и размножение, эндостатин, по-видимому, не влияет. Результат возможен, потому что патогенный ангиогенез обычно включает передачу сигналов через интегрины, на которые непосредственно влияет эндостатин.[1]
Рак
Хотя этот процесс, с помощью которого работает эндостатин, полностью не изучен, он включает металлопротеазы и эндопептидазы, которые переваривают компоненты внеклеточный матрикс. Таким образом, из компонентов матрикса получают несколько подобных эндогенных ангиогенных факторов. Например, деградация перлекана может давать эндорепеллин, который действует как антиангиогенный фактор. В совокупности эти продукты, как полагают, балансируют регуляцию между проангиогенными и антиангиогенными факторами вне эпителиального и эндотелиального слоев.[31]
Среди ингибиторов антиангиогенеза эндостатин имеет широкий спектр мишеней противоракового спектра, что увеличивает его значимость, поскольку синтетические ингибиторы обычно имеют одиночные мишени и борются с токсичностью.[32] Эндостатин имеет несколько характеристик, которые могут быть полезны при лечении рака. Прежде всего, эндогенный эндостатин был описан как «наименее токсичный противораковый препарат для мышей». Кроме того, у людей не наблюдается ни устойчивости, ни токсичности к эндостатину.[нужна цитата ] Кроме того, по оценкам, эндостатин влияет на 12% генома человека. Это свидетельствует о широком спектре активности, направленной на предотвращение ангиогенеза. Это сильно отличается от методов лечения с помощью одной молекулы и может изменить то, как разрабатываются методы лечения рака: лекарства могут быть разработаны для воздействия на широкий спектр генов, а не на один конкретный белок. Однако эндостатин влияет не на все опухоли. Например, злокачественные опухоли, которые могут проявлять крайнюю проангиогенную активность через VEGF, могут преодолевать антиангиогенные эффекты эндостатина.[1]
Возможное лечение рака
Эндостатин в настоящее время изучается как часть исследования рака. Предыдущие результаты показали, что эндостатин может быть полезным в сочетании с другими лекарствами, но только эндостатин не дал значительного улучшения в прогрессировании опухоли / заболевания.
Фаза I
В фазе I клинического испытания эндостатина из 19 пролеченных пациентов 12 были исключены из исследования их врачами из-за продолжающегося прогрессирования их заболевания.[33] Два пациента продолжили лечение, а остальные отказались от него самостоятельно. Испытание, направленное в первую очередь на демонстрацию безопасности, действительно показало, что препарат безопасен и хорошо переносится (в используемых дозировках).
Фаза II
В клинических испытаниях фазы II эндостатина 42 пациента с эндокринными опухолями поджелудочной железы или карциноид опухоли лечили.[34] Из 40 пациентов, у которых можно было оценить радиологический ответ, ни у одного не было частичного ответа на терапию, как определено Всемирная организация здоровья критерии.
Заключение исследования заключалось в том, что «лечение эндостатином не привело к значительной регрессии опухоли у пациентов с распространенными нейроэндокринными опухолями».
Фаза III
Клинические испытания III фазы проводились на 493 гистологически или цитологически подтвержденных стадиях IIIB и IV. НМРЛ пациенты с ожидаемой продолжительностью жизни> 3 мес. Пациенты получали эндостар (резус-эндостатин, YH-16), рекомбинантный эндостатиновый продукт, в сочетании с винорелбин и цисплатин (стандартный химиотерапевтический режим ). Добавление Endostar к стандартному режиму химиотерапии у этих пациентов с распространенным НМРЛ привело к значительному и клинически значимому улучшению скорости ответа, среднего времени до прогрессирования и степени клинической пользы по сравнению с химиотерапевтическим режимом только.[35]
Клиническое значение
Эндостатин также может быть полезен в качестве терапевтического средства при воспалительных заболеваниях, таких как ревматоидный артрит а также Болезнь Крона, диабетическая ретинопатия, псориаз, и эндометриоз за счет уменьшения инфильтрации воспалительных клеток за счет вторжения в ангиогенез.[36]Синдром Дауна Кажется, что пациенты защищены от диабетической ретинопатии из-за дополнительной копии хромосомы 21 и повышенной экспрессии эндостатина.[37]
Рекомендации
- ^ а б c Фолкман, Дж. (2006). «Антиангиогенез в терапии рака - эндостатин и механизмы его действия». Exp. Cell Res. 312 (5, часть 2): 594–607. Дои:10.1016 / j.yexcr.2005.11.015. PMID 16376330.
- ^ а б c OReilly, M.S .; Boehm, T .; Shing, Y .; Fukai, N .; Васиос, G .; Lane, W.W .; Flynn, E .; Birkhead, J.R .; Olsen, B.R .; Фолкман, Дж. (1997). «Эндостатин: эндогенный ингибитор ангиогенеза и роста опухоли». Клетка. 88 (2): 277–85. Дои:10.1016 / S0092-8674 (00) 81848-6. PMID 9008168.
- ^ Standker, L; Schrader, M .; Kanse, S.M .; Юргенс, М .; Forssmann, W.G .; Присснер, К. (1997). «Выделение и характеристика циркулирующей формы человеческого эндостатина». FEBS Lett. 420 (2–3): 129–33. Дои:10.1016 / S0014-5793 (97) 01503-2. PMID 9459295.
- ^ Felbor, U; и другие. (2000). «Секретируемый катепсин L генерирует эндостатин из коллагена XVIII». EMBO J. 19 (6): 1187–94. Дои:10.1093 / emboj / 19.6.1187. ЧВК 305660. PMID 10716919.
- ^ Браудер, Т .; Folkman, J .; Пири-Шеперд, С. (2000). «Гемостатическая система как регулятор ангиогенеза». J. Biol. Chem. 275 (3): 1521–4. Дои:10.1074 / jbc.275.3.1521. PMID 10636838.
- ^ Ma, L; Холленберг, доктор медицины; Уоллес, Дж. Л. (2001). «Вызванное тромбином высвобождение эндостатина тромбоцитов блокируется антагонистом рецептора-4, активируемого протеиназой (PAR4)». Br. J. Pharmacol. 134 (4): 701–4. Дои:10.1038 / sj.bjp.0704312. ЧВК 1573005. PMID 11606309.
- ^ Rhim, T.Y .; Park, C.S .; Kim, E .; Ким, С.С. (1998). «Фрагменты протромбина 1 и 2 человека ингибируют bFGF-индуцированный рост клеток BCE». Biochem. Биофиз. Res. Сообщество. 252 (2): 513–6. Дои:10.1006 / bbrc.1998.9682. PMID 9826562.
- ^ Nyberg, P .; Xie, L .; Каллури, Р. (2005). «Эндогенные ингибиторы ангиогенеза». Рак Res. 65 (10): 3967–79. Дои:10.1158 / 0008-5472.CAN-04-2427. PMID 15899784.
- ^ Абдоллахи, А .; Hahnfeldt, P .; Maercker, C .; Grone, H .; Debus, J .; Ansorge, W .; Folman, J .; Глатки, Л .; Хубер, П. (2004). «Антиангиогенная сигнальная сеть эндостатина». Мол. Клетка. 13 (5): 649–63. Дои:10.1016 / S1097-2765 (04) 00102-9. PMID 15023336.
- ^ Assadian, S .; Теодоро, Дж. (2008). «Регулирование антиангиогенных факторов коллагенового происхождения с помощью р53». Мнение эксперта. Биол. Ther. 8 (7): 941–50. Дои:10.1517/14712598.8.7.941. PMID 18549324.
- ^ John, H .; Форссманн, W.G. (2001). «Определение структуры дисульфидной связи эндогенного и рекомбинантного ингибитора ангиогенеза эндостатина с помощью масс-спектрометрии». Rapid Commun. Масс-спектрометрия. 15 (14): 1222–8. Bibcode:2001RCMS ... 15.1222J. Дои:10.1002 / RCM.367. PMID 11445906.
- ^ Hohenester, E .; Сасаки, Т .; Olsen, B.R .; Тимпл Р. (1998). «Кристаллическая структура эндостатина ингибитора ангиогенеза при разрешении 1,5 А». EMBO J. 17 (6): 1656–64. Дои:10.1093 / emboj / 17.6.1656. ЧВК 1170513. PMID 9501087.
- ^ Ding, Y.H .; Javaherian, K .; Lo, K.M .; Chopra, R .; Boehm, T .; Lanciotti, J .; Harris, B.A .; Li, Y .; Шапиро, Р .; Hohenester, E .; и другие. (1998). «Цинк-зависимые димеры, наблюдаемые в кристаллах эндостатина человека». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 95 (18): 10443–8. Bibcode:1998PNAS ... 9510443D. Дои:10.1073 / пнас.95.18.10443. ЧВК 27913. PMID 9724722.
- ^ Dixelius, J .; Крест, М .; Matsumoto, T .; Сасаки, Т .; Timpl, R .; Клаессон-Уэлш Л. (2002). «Эндостатин регулирует адгезию эндотелиальных клеток и организацию цитоскелета». Рак Res. 62 (7): 1944–7. PMID 11929807.
- ^ Karumanchi, S.A .; Jha, V .; Ramchandran, R .; Карихалоо, А .; Циокас, Л .; Чан, Б .; Dhanabal, M .; Hanai, J.I .; Venkataraman, G .; Шрайвер, З .; и другие. (2001). «Глипиканы клеточной поверхности представляют собой рецепторы эндостатина с низким сродством» (PDF). Мол. Клетка. 7 (4): 811–22. Дои:10.1016 / S1097-2765 (01) 00225-8. PMID 11336704.
- ^ Сасаки, Т; Larsson, H .; Kreuger, J .; Салмивирта, М .; Claesson-Welsh, L .; Lindahl, U .; Hohenester, E .; Тимпл Р. (1999). «Структурная основа и потенциальная роль связывания гепарина / гепарансульфата с ингибитором ангиогенеза эндостатином». EMBO J. 18 (22): 6240–8. Дои:10.1093 / emboj / 18.22.6240. ЧВК 1171687. PMID 10562536.
- ^ Javaherian, K .; Park, S.Y .; Pickl, W.F .; LaMontagne, K.R .; Sjin, R.T.T .; Gillies, S .; Ло, К. (2002). «Ламинин модулирует морфогенные свойства домена эндостатина коллагена XVIII». J. Biol. Chem. 277 (47): 45211–8. Дои:10.1074 / jbc.M206358200. PMID 12237301.
- ^ Folkman, J .; Каллури, Р. (2004). «Рак без болезней». Природа. 427 (6977): 787. Bibcode:2004Натура.427..787F. Дои:10.1038 / 427787a. PMID 14985739.
- ^ Shichiri, M .; Хирата (2001). «Y». FASEB J. 15 (6): 1044–53. Дои:10.1096 / fj.99-1083com. PMID 11292666.
- ^ Инь, G; Liu, W .; An, P .; Li, P .; Ding, I .; Planelles, V .; Schwarz, E.M .; Мин, В. (2002). «Перенос гена эндостатина ингибирует ангиогенез суставов и образование паннуса при воспалительном артрите». Мол. Ther. 5 (5, Pt 1): 547–54. Дои:10.1006 / mthe.2002.0590. PMID 11991745.
- ^ Dhanabal, M .; Volk, R .; Ramchandran, R .; Simons, M .; Сухатме, В. (1999). «Клонирование, экспрессия и активность эндостатина человека in vitro». Biochem. Биофиз. Res. Сообщество. 258 (2): 345–52. Дои:10.1006 / bbrc.1999.0595. PMID 10329390.
- ^ Hanai, J .; Dhanabal, M .; Karumanchi, S.A .; Albanese, C .; Waterman, M .; Чан, Б .; Ramchandran, R .; Pestell, R .; Сухатме, В. (2002). «Эндостатин вызывает задержку G1 эндотелиальных клеток за счет ингибирования циклина D1». J. Biol. Chem. 277 (19): 16464–9. Дои:10.1074 / jbc.M112274200. PMID 11815623.
- ^ Дикселиус, Дж; Larsson, H .; Сасаки, Т .; Holmqvist, K .; Lu, L .; Engstrom, A .; Timpl, R .; Валлийский, M .; Клаэссон-Уэлш, Л. (2000). «Эндостатин-индуцированная передача сигналов тирозинкиназы через адаптерный белок Shb регулирует апоптоз эндотелиальных клеток». Кровь. 95 (11): 3403–11. Дои:10.1182 / кровь.V95.11.3403. PMID 10828022.
- ^ Судхакар, А .; Sugimoto, H .; Ян, С .; Лайвли, Дж .; Zeisberg, M .; Каллури, Р. (2003). «Человеческий тумстатин и человеческий эндостатин проявляют различные антиангиогенные активности, опосредованные интегринами альфа v бета 3 и альфа 5 бета 1». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 100 (8): 4766–71. Дои:10.1073 / pnas.0730882100. ЧВК 153630. PMID 12682293.
- ^ Татосян, А.Г .; Мизенина, О.А. (2000). «Киназы семейства Src: структура и функции». Биохимия. 65 (1): 49–58. PMID 10702640.
- ^ Thomas, S.M .; Брюгге, Дж. (1997). «Клеточные функции, регулируемые киназами семейства Src». Анну. Rev. Cell Dev. Биол. 13: 513–609. Дои:10.1146 / annurev.cellbio.13.1.513. PMID 9442882.
- ^ Осторожно, К.К .; Mariotti, A .; Zurzolo, C .; Джанкотти, Ф. (1998). «Необходимость кавеолина-1 и связанной с ним киназы Fyn для передачи сигналов интегрина и роста клеток, зависимых от закрепления». Клетка. 94 (5): 625–34. Дои:10.1016 / S0092-8674 (00) 81604-9. PMID 9741627.
- ^ Wickstrom, S.A .; Alitalo, K .; Кески-Оя, Дж. (2002). «Эндостатин связывается с интегрином альфа5бета1 и кавеолином-1 и активирует Src через тирозилфосфатазозависимый путь в эндотелиальных клетках человека». Рак Res. 62 (19): 5580–9. PMID 12359771.
- ^ Kim, Y .; Hwang, S .; Kim, Y .; Пюн, Б .; Kim, T .; Lee, S .; Gho, Y.S .; Квон, Ю. (2002). «Эндостатин блокирует передачу сигналов, опосредованную фактором роста эндотелия сосудов, посредством прямого взаимодействия с KDR / Flk-1». J. Biol. Chem. 277 (31): 27872–9. Дои:10.1074 / jbc.M202771200. PMID 12029087.
- ^ Felbor, U .; и другие. (2000). «Секретируемый катепсин L генерирует эндостатин из коллагена XVIII». EMBO J. 19 (6): 1187–94. Дои:10.1093 / emboj / 19.6.1187. ЧВК 305660. PMID 10716919.
- ^ Марнерос, А.Г .; Ольсен, Б. (2005). «Физиологическая роль коллагена XVIII и эндостатина». Журнал FASEB. 19 (7): 716–28. Дои:10.1096 / fj.04-2134rev. PMID 15857886.
- ^ Карамузис, М.В .; Moschos, S.J. (2009). «Использование эндостатина в лечении солидных опухолей». Мнение эксперта. Биол. Ther. 9 (5): 641–8. Дои:10.1517/14712590902882118. PMID 19368526.
- ^ «Бостонские больницы сообщают о первых результатах клинических испытаний эндостатина» (Пресс-релиз). ScienceDaily.com: Институт рака Дана-Фарбер. 13 ноября 2000 г.. Получено 2006-07-12.
- ^ Кульке М Н; и другие. (2006). «Фаза II исследования рекомбинантного человеческого эндостатина у пациентов с запущенными нейроэндокринными опухолями». J. Clin. Онкол. 24 (22): 3555–3561. Дои:10.1200 / JCO.2006.05.6762. PMID 16877721.
- ^ Результаты III фазы исследования резус-эндостатина (YH-16) у продвинутых немелкоклеточный рак легкого (NSCLC) пациенты (Ю. Сан, Дж. Ван, Ю. Лю, Х. Сун, Ю. Чжан, К. Ли, Ю. Чжу, К. Чжоу, Л. Ю и К. Яо) [1]
- ^ Инь, G .; Liu, W .; An, P .; Li, P .; ding, I .; Planelles, V .; Schwarz, E.M .; Мин, В. (2002). «Перенос гена эндостатина ингибирует ангиогенез суставов и образование паннуса при воспалительном артрите». Мол. Ther. 5 (5, Пет. 1): 547–54. Дои:10.1006 / mthe.2002.0590. PMID 11991745.
- ^ Райом С., Фолкман Дж. (Март 2009 г.). «Роль эндогенных ингибиторов ангиогенеза при синдроме Дауна». J. Craniofac. Surg. 20 Дополнение 1: 595–6. Дои:10.1097 / SCS.0b013e3181927f47. PMID 19795527.
внешняя ссылка
- Эндостатин в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Программа PBS Nova исследует эндостатин в 2001 году
