Пенициллин - Penicillin
 Структура ядра пенициллина, где "R" - группа переменных. | |
| Клинические данные | |
|---|---|
| AHFS /Drugs.com | Подробная информация для потребителей Micromedex |
| Беременность категория |
|
| Маршруты администрация | Внутривенно, внутримышечный, устно |
| Легальное положение | |
| Легальное положение |
|
| Фармакокинетический данные | |
| Метаболизм | Печень |
| Устранение период полураспада | От 0,5 до 56 часов |
| Экскреция | Почки |
Пенициллин (PCN или же ручка) - это группа антибиотики, происходящий из общего формы известный как Пенициллий формы; который включает пенициллин G (внутривенное использование ), пенициллин V (использовать внутрь), прокаин пенициллин, и бензатин пенициллин (внутримышечное использование ). Антибиотики пенициллина были одними из первых лекарств, которые были эффективны против многих бактериальные инфекции вызванный стафилококки и стрептококки. Они все еще широко используются сегодня, хотя многие типы бактерии разработали сопротивление после широкого использования.
Около 10% людей сообщают, что они аллергический к пенициллину; однако до 90% этой группы на самом деле могут не иметь аллергии.[2] Серьезные аллергии встречаются только у 0,03%.[2] Тем, у кого аллергия на пенициллин, чаще всего назначают цефалоспорин C из-за его функциональных групп.[3] Все пенициллины β-лактамные антибиотики, которые являются одними из самых мощных и успешных достижений современной науки.[3]
Пенициллин был открыт в 1928 году шотландским ученым. Александр Флеминг.[4] Люди начали использовать его для лечения инфекций в 1942 году.[5] Есть несколько расширенных семейств пенициллина, которые эффективны против дополнительных бактерий; к ним относятся антистафилококковые пенициллины, аминопенициллины и антипсевдомонадные пенициллины. Они получены из Пенициллий грибы.[6] Флеминг поделился 1945 годом Нобелевская премия по физиологии и медицине за его открытие, вместе с Оксфордский университет ученые Говард Флори и Эрнст Борис Чейн (который разработал улучшенные способы производства и концентрирования препарата и доказал его антибактериальный эффект).
Медицинское использование
Термин «пенициллин» первоначально использовался для бензилпенициллин, пенициллин G. В настоящее время «пенициллин» используется как общий термин для антибиотиков, содержащих бета-лактам единица в химической структуре. Например, амоксициллин Таблетки могут иметь маркировку «пенициллин». Другие производные, такие как прокаин бензилпенициллин (новокаин пенициллин), бензатин бензилпенициллин (бензатин пенициллин) и феноксиметилпенициллин (пенициллин V) также называют «пенициллинами». Прокаин-пенициллин и бензатин-пенициллин обладают такой же антибактериальной активностью, как бензилпенициллин, но действуют в течение более длительного периода времени. Феноксиметилпенициллин менее активен против грамотрицательный бактерии, чем бензилпенициллин.[7][8] Бензилпенициллин, прокаин-пенициллин и бензатин-пенициллин можно вводить только внутривенно или внутримышечно, но феноксиметилпенициллин можно вводить перорально из-за его кислотной стабильности.[9]
Восприимчивость
Хотя число устойчивых к пенициллину бактерий растет, пенициллин все еще можно использовать для лечения широкого спектра инфекций, вызванных определенными чувствительными бактериями, в том числе бактериями Стрептококк, Стафилококк, Clostridium, Neisseria, и Листерия роды. Следующий список иллюстрирует минимальная ингибирующая концентрация Данные о восприимчивости к нескольким значимым с медицинской точки зрения бактериям:[10][11]
- Listeria monocytogenes: от менее или равного 0,06 мкг / мл до 0,25 мкг / мл
- Neisseria meningitidis: от менее или равного 0,03 мкг / мл до 0,5 мкг / мл
- Золотистый стафилококк: от менее или равного 0,015 мкг / мл до более 32 мкг / мл
Побочные эффекты
Часто (≥ 1% людей) побочные реакции на лекарства связанные с использованием пенициллинов, включают понос, гиперчувствительность, тошнота, сыпь, нейротоксичность, крапивница, и суперинфекция (включая кандидоз ). Нечастые побочные эффекты (0,1–1% людей) включают: высокая температура, рвота, эритема, дерматит, ангионевротический отек, припадки (особенно у людей с эпилепсия ), и псевдомембранозный колит.[12] Пенициллин также может вызывать сывороточная болезнь или реакция, похожая на сывороточную болезнь у некоторых людей. Сывороточная болезнь - это гиперчувствительность III типа реакция, которая возникает через одну-три недели после приема лекарств, включая пенициллин. Это не настоящая лекарственная аллергия, потому что аллергия гиперчувствительность I типа реакции, но повторное воздействие возбудителя может привести к анафилактической реакции.[13][14] Аллергия возникает у 1-10% людей и проявляется в виде кожной сыпи после воздействия. IgE-опосредованный анафилаксия произойдет примерно у 0,01% пациентов.[15][12]
Боль и воспаление в месте инъекции также характерны для парентерально вводили бензатин бензилпенициллин, бензилпенициллин и, в меньшей степени, прокаин бензилпенициллин. Состояние известно как ливедоидный дерматит или синдром Николо.[16][17]
Члены
| Имена | Способ применения | Примечания |
|---|---|---|
| Пенициллин G, бензилпенициллин | IV или IM | Он имеет высокую экскрецию с мочой и вырабатывается в виде соли калия или натрия. |
| Пенициллин V, феноксиметилпенициллин | Устно | Он менее активен, чем бензилпенициллин, в отношении грамотрицательных бактерий. |
| Бензатин бензилпенициллин, бензатин пенициллин G | Я | Бензатин - стабилизатор, который вызывает более медленное высвобождение в течение двух-четырех недель. |
| Прокаин бензилпенициллин, пенициллин G прокаин | Я | Медленный выпуск. |
Природные пенициллины
- Пенициллин G
- Пенициллин К
- Пенициллин N
- Пенициллин О
- Пенициллин V
β-лактамазустойчивый
Аминопенициллины
Карбоксипенициллины
Уреидопенициллины
ингибиторы β-лактамаз
Фармакология
Пенициллин подавляет активность ферментов, необходимых для перекрестного связывания пептидогликаны в стенки бактериальных клеток, который является заключительным этапом биосинтеза клеточной стенки. Это делается путем привязки к связывающие пенициллин белки с бета-лактамным кольцом, структурой, обнаруженной на молекулах пенициллина.[18][19] Это вызывает ослабление клеточной стенки из-за меньшего количества поперечных связей и означает, что вода неконтролируемо течет в клетку, потому что она не может поддерживать правильный осмотический градиент. Это приводит к ячейке лизис и смерть.
Некоторые бактерии вырабатывают ферменты, которые разрушают бета-лактамное кольцо, называемые бета-лактамазами, которые делают бактерии устойчивыми к пенициллину. Поэтому некоторые пенициллины модифицируются или вводятся вместе с другими лекарствами для использования против устойчивых к антибиотикам бактерий или у пациентов с ослабленным иммунитетом. Использование клавулановой кислоты или тазобактама, ингибиторов бета-лактамаз, вместе с пенициллином дает пенициллиновую активность против бактерий, продуцирующих бета-лактамазы. Ингибиторы бета-лактамазы необратимо связываются с бета-лактамазой, предотвращая расщепление бета-лактамных колец на молекуле антибиотика. В качестве альтернативы флуклоксациллин представляет собой модифицированный пенициллин, который обладает активностью против бактерий, продуцирующих бета-лактамазы, за счет ацильной боковой цепи, которая защищает бета-лактамное кольцо от бета-лактамазы.[15]
Механизм действия


Бактерии постоянно переделывают свои пептидогликан клеточные стенки, одновременно создавая и разрушая части клеточной стенки по мере их роста и деления. β-Лактамные антибиотики подавляют образование пептидогликана перекрестные ссылки в бактериальном клеточная стенка; это достигается за счет связывания четырехчленного β-лактам звенеть пенициллина в фермент DD-транспептидаза. Как следствие, DD-транспептидаза не может катализировать образование этих поперечных связей, и возникает дисбаланс между образованием и деградацией клеточной стенки, что приводит к быстрой гибели клетки.[21]
Ферменты, которые гидролизовать поперечные связи пептидогликана продолжают функционировать, даже если те, которые образуют такие поперечные связи, не функционируют. Это ослабляет клеточную стенку бактерии, и осмотическое давление становится все более некомпенсированным, что в конечном итоге приводит к гибели клеток (цитолиз ). Кроме того, накопление предшественников пептидогликанов запускает активацию гидролаз и автолизинов клеточной стенки бактерий, которые дополнительно переваривают пептидогликаны клеточной стенки. Небольшой размер пенициллинов увеличивает их эффективность, позволяя им проникать на всю глубину клеточной стенки. Это в отличие от гликопептидные антибиотики ванкомицин и тейкопланин, которые намного больше, чем пенициллины.[22]
Грамположительные бактерии называются протопласты когда они теряют свои клеточные стенки. Грамотрицательный бактерии не теряют полностью свои клеточные стенки и называются сферопласты после лечения пенициллином.[20]
Пенициллин проявляет синергетический эффект с аминогликозиды, поскольку ингибирование синтеза пептидогликана позволяет аминогликозидам легче проникать через стенку бактериальной клетки, что приводит к нарушению синтеза бактериального белка внутри клетки. Это приводит к снижению MBC для восприимчивых организмов.[23]
Пенициллины, как и другие β-лактамные антибиотики, блокируют не только деление бактерий, в том числе цианобактерии, но и деление цианелл, фотосинтетический органеллы из глаукофиты, и разделение хлоропласты из мохообразные. Напротив, они не влияют на пластиды высокоразвитых сосудистые растения. Это поддерживает эндосимбиотическая теория из эволюция пластидного деления наземных растений.[24]
Химическая структура пенициллина запускается очень точным, зависящим от pH направленным механизмом, осуществляемым за счет уникальной пространственной сборки молекулярных компонентов, которые могут активироваться протонированием. Он может путешествовать через физиологические жидкости, нацеливая и инактивируя ферменты, ответственные за синтез клеточной стенки у грамположительных бактерий, избегая при этом окружающих нецелевых. Пенициллин может защищать себя от спонтанного гидролиза в организме в своей анионной форме, сохраняя при этом свой потенциал как сильного ацилирующего агента, активируемого только при приближении к ферменту-мишени транспептидазы и протонируемого в активном центре. Это целевое протонирование нейтрализует фрагмент карбоновой кислоты, который ослабляет связь N – C (= O) β-лактамного кольца, что приводит к самоактивации. Конкретные конструктивные требования связаны с созданием идеальной мышеловки для поимки целевой добычи.[25]
Фармакокинетика
Пенициллин имеет низкое связывание с белками плазмы. Биодоступность пенициллина зависит от типа: пенициллин G имеет низкую биодоступность, менее 30%, тогда как пенициллин V имеет более высокую биодоступность, от 60 до 70%. Пенициллин имеет короткий период полураспада и выводится через почки.[26]
Структура
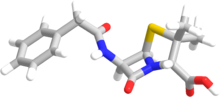
Период, термин "пенам "используется для описания общего каркаса ядра члена пенициллинов. Это ядро имеет молекулярную формулу R-C9ЧАС11N2О4S, где R - вариабельная боковая цепь, которая отличает пенициллины друг от друга. Ядро пенама имеет молярная масса 243 г / моль, с более крупными пенициллинами, имеющими молярную массу около 450, например, клоксациллин имеет молярную массу 436 г / моль. Ключевой структурной особенностью пенициллинов является четырехчленный β-лактамное кольцо; этот структурный часть необходим для антибактериальной активности пенициллина. В β-лактамное кольцо само слито с пятичленным тиазолидин звенеть. Слияние этих двух колец вызывает β-лактамное кольцо должно быть более реактивным, чем моноциклическое β-лактамы, потому что два слившихся кольца искажают β-лактам амидная связь и поэтому удалите резонансная стабилизация обычно содержится в этих химических связях.[27]
История
Открытие


Начиная с конца 19 века появились сообщения об антибактериальных свойствах Пенициллий плесени, но ученые не смогли определить, какой процесс вызвал эффект.[28] Шотландский врач Александр Флеминг в Больница Святой Марии в Лондоне (ныне часть Имперский колледж ) был первым, кто показал, что Penicillium rubens в 1928 г. обладал антибактериальными свойствами.[29] 3 сентября 1928 г. он заметил, что грибковое заражение бактериальной культуры (Золотистый стафилококк ) убивает бактерии. Он подтвердил это наблюдение новым экспериментом 28 сентября 1928 г.[30] Он опубликовал свой эксперимент в 1929 году и назвал антибактериальное вещество (экстракт грибов) пенициллином.[31]
К. Ж. Ла Туш идентифицировал гриб как Penicillium rubrum (позже реклассифицирован Чарльз Том в качестве P. notatum и P. chrysogenum, но позже исправлено как П. Рубенс ).[32] Флеминг выразил первоначальный оптимизм по поводу того, что пенициллин будет полезным антисептиком из-за его высокой активности и минимальной токсичности по сравнению с другими антисептиками того времени, и отметил его лабораторную ценность для выделения Bacillus influenzae (теперь называется Haemophilus influenzae ).[33][34]
Флеминг никого не убедил в важности своего открытия.[33] Во многом это было связано с тем, что пенициллин было настолько трудно изолировать, что его разработка как лекарство казалась невозможной. Предполагается, что если бы Флеминг добился большего успеха в привлечении внимания других ученых к своей работе, пенициллин, возможно, был бы разработан на несколько лет раньше.[33]
Важность его работы была признана помещением Международная историческая химическая достопримечательность в Музее лаборатории Александра Флеминга в Лондоне 19 ноября 1999 г.[35]
Медицинское приложение

В 1930 году Сесил Джордж Пейн, патолог на Королевский лазарет в Шеффилд, успешно вылечили офтальмия новорожденных, гонококковая инфекция у младенцев, с пенициллином (грибковый экстракт) 25 ноября 1930 года.[36][37][38]
В 1940 году австралийский ученый Говард Флори (позже барон Флори) и группа исследователей (Эрнст Борис Чейн, Эдвард Абрахам, Артур Дункан Гарднер, Норман Хитли, Маргарет Дженнингс, Дж. Орр-Юинг и Дж. Сандерс) в Школе патологии сэра Уильяма Данна, Оксфордский университет добились успехов в производстве концентрированного пенициллина из культурального бульона грибов, что in vitro и in vivo бактерицидное действие.[39][40] В 1941 году лечили милиционера, Альберт Александр, с тяжелой инфекцией лица; его состояние улучшилось, но потом закончились запасы пенициллина, и он умер. Впоследствии еще несколько пациентов были успешно вылечены.[41] В декабре 1942 г. выжившие Огонь кокосовой рощи в Бостоне были первыми ожоговыми пациентами, которые успешно прошли курс лечения пенициллином.[42]
Массовое производство

Когда медицинское приложение было установлено, оксфордская команда обнаружила, что невозможно получить полезное количество из их лаборатории.[41] В 1941 году Флори и Хитли отправились в США, чтобы заинтересовать фармацевтические компании в производстве препарата и проинформировать их о своем процессе.[41]
14 марта 1942 г. первый пациент прошел курс лечения от стрептококкового сепсиса американским пенициллином производства Merck & Co.[43] Половина всей продукции, произведенной в то время, была израсходована на одну пациентку, Энн Миллер.[44] К июню 1942 года американского пенициллина было достаточно для лечения десяти пациентов.[45] В июле 1943 г. Совет по военному производству разработал план массового распределения запасов пенициллина среди войск союзников, сражающихся в Европе.[46] Результаты исследования ферментации на кукурузный крепкий ликер на Северная региональная научно-исследовательская лаборатория в Пеории, штат Иллинойс, позволил Соединенным Штатам произвести 2,3 миллиона доз вовремя для вторжение в Нормандию весной 1944 года. После всемирных поисков в 1943 году заплесневелый мускусная дыня в Пеория, Иллинойс было обнаружено, что на рынке содержится лучший штамм плесени для производства кукурузного настоя.[47] Pfizer ученый Джаспер Х. Кейн предложили использовать метод ферментации в глубоких резервуарах для производства больших количеств пенициллина фармацевтического качества.[48][49] Крупномасштабное производство стало результатом разработки завода по ферментации в глубоких резервуарах. инженер-химик Маргарет Хатчинсон Руссо.[50] В результате войны и Управления военного производства к июню 1945 года производилось более 646 миллиардов единиц в год.[46]


Г. Раймонд Реттью внес значительный вклад в американские военные усилия, используя свои методы производства пенициллина в промышленных количествах, при этом он объединил свои знания о грибной икре с функцией сепаратора сливок Шарплса.[51]К 1943 году лаборатория Реттью производила большую часть пенициллина в мире. В течение Вторая Мировая Война, пенициллин существенно повлиял на количество смертей и ампутаций, вызванных инфицированными ранами среди Союзник сил, спасая примерно 12–15% жизней.[нужна цитата ] Однако доступность была сильно ограничена из-за сложности производства больших количеств пенициллина и быстрого почечный клиренс препарата, что требует частого приема. Методы для массовое производство пенициллина были запатентованы Эндрю Джексон Мойер в 1945 г.[52][53][54] Флори не запатентовал пенициллин, по совету сэра Генри Дейл это было бы неэтично.[41]
Пенициллин активно выводится из организма, и около 80% дозы пенициллина выводится из организма в течение трех-четырех часов после приема. Действительно, в раннюю эру пенициллина препарат был настолько дефицитным и высоко ценимым, что стало обычным делом собирать мочу у пациентов, проходящих лечение, чтобы пенициллин в моче можно было выделить и повторно использовать.[55] Это не было удовлетворительным решением, поэтому исследователи искали способ замедлить выведение пенициллина. Они надеялись найти молекулу, которая могла бы конкурировать с пенициллином за переносчик органической кислоты, ответственный за выведение, таким образом, чтобы переносчик преимущественно выводил из организма конкурирующую молекулу, а пенициллин сохранялся. В урикозурический агент пробенецид оказался подходящим. Когда пробенецид и пенициллин вводятся вместе, пробенецид конкурентно ингибирует выведение пенициллина, увеличивая концентрацию пенициллина и продлевая его активность. В конце концов, с появлением технологий массового производства и полусинтетических пенициллинов были решены проблемы с поставками, поэтому использование пробенецида сократилось.[55] Однако пробенецид по-прежнему полезен при некоторых инфекциях, требующих особенно высоких концентраций пенициллинов.[12][нуждается в обновлении ]
После Второй мировой войны Австралия стала первой страной, сделавшей препарат доступным для использования в гражданских целях. В США пенициллин стал доступен широкой публике 15 марта 1945 года.[56]
Флеминг, Флори и Чейн разделили Нобелевскую премию по физиологии и медицине 1945 года за разработку пенициллина.

Определение структуры и полный синтез

В химическая структура пенициллина был впервые предложен Эдвард Абрахам в 1942 г.[39] и позже было подтверждено в 1945 году с использованием Рентгеновская кристаллография к Дороти Кроуфут Ходжкин, который также работал в Оксфорде.[57] Позже она получила Нобелевскую премию за это и другие определения структуры.
Химик Джон С. Шиэн на Массачусетский Институт Технологий (MIT) завершил первый химический синтез пенициллина в 1957 г.[58][59][60] Шихан начал свои исследования синтеза пенициллина в 1948 году, и в ходе этих исследований разработал новые методы синтеза пенициллина. пептиды, а также новые защитные группы - группы, маскирующие реактивность определенных функциональных групп.[60][61] Хотя первоначальный синтез, разработанный Шиханом, не подходил для массового производства пенициллинов, одним из промежуточных соединений в синтезе Шихана было 6-аминопеницилановая кислота (6-APA), ядро пенициллина.[60][62][63][страница нужна ] Присоединение различных групп к «ядру» 6-APA пенициллина позволило создать новые формы пенициллина.
Разработки от пенициллина
Узкий диапазон поддающихся лечению заболеваний или «спектр активности» пенициллинов, наряду с низкой активностью перорально активного феноксиметилпенициллина, привели к поиску производных пенициллина, которые могли бы лечить более широкий спектр инфекций. Выделение 6-APA, ядра пенициллина, позволило получить полусинтетические пенициллины с различными улучшениями по сравнению с бензилпенициллин (биодоступность, спектр, стабильность, переносимость).
Первым крупным событием было ампициллин в 1961 году. Он обладал более широким спектром действия, чем любой из исходных пенициллинов. Дальнейшее развитие привело к появлению устойчивых к β-лактамазам пенициллинов, в том числе флуклоксациллин, диклоксациллин, и метициллин. Они были значительными из-за их активности против видов бактерий, продуцирующих β-лактамазы, но были неэффективны против метициллин-устойчивый Золотистый стафилококк (MRSA), которые возникли впоследствии.[64]
Другим развитием линии настоящих пенициллинов были антипсевдомонадные пенициллины, такие как карбенициллин, тикарциллин, и пиперациллин, полезны для их деятельности против Грамотрицательный бактерии. Однако полезность бета-лактамного кольца была такова, что родственные антибиотики, включая мециллинамы, то карбапенемы и, самое главное, цефалоспорины, по-прежнему сохраняют его в центре своих структур.[65]
Производство

Пенициллин - это вторичный метаболит некоторых видов Пенициллий и образуется, когда рост грибка подавляется стрессом. Во время активного роста не вырабатывается. Производство также ограничено обратной связью в пути синтеза пенициллина.[нужна цитата ]
Побочный продукт, л-лизин подавляет выработку гомоцитрата, поэтому при производстве пенициллина следует избегать присутствия экзогенного лизина.
В Пенициллий клетки выращиваются с использованием техники, называемой партия с кормлением культура, в которой клетки постоянно подвергаются стрессу, необходимому для индукции выработки пенициллина. Имеющиеся источники углерода также важны: глюкоза подавляет выработку пенициллина, тогда как лактоза не. В pH также необходимо тщательно контролировать уровни азота, лизина, фосфата и кислорода в партиях.[нужна цитата ]
В биотехнологический метод направленная эволюция был применен для получения путем мутации большого количества Пенициллий штаммы. Эти методы включают подверженная ошибкам ПЦР, Перетасовка ДНК, ЗУДЯЩИЙ, и ПЦР с перекрыванием цепей.
Полусинтетические пенициллины получают, начиная с ядра пенициллина. 6-АПА.
Биосинтез

В целом, есть три основных и важных этапа биосинтеза пенициллин G (бензилпенициллин).
- Первый шаг - это конденсация трех аминокислот -L-α-аминоадипиновая кислота, L-цистеин, L-валине в трипептид.[66][67][68] Перед конденсацией в трипептид аминокислота L-валин должен подвергнуться эпимеризации, чтобы стать D-валин.[69][70] Конденсированный трипептид называется δ- (L-α-аминоадипил) -L-цистеин-D-валин (ACV). И реакция конденсации, и эпимеризация катализируются ферментом δ- (L-α-аминоадипил) -L-цистеин-D-валин синтетаза (ACVS), a негрибосомный пептид синтетаза или NRPS.
- Второй этап биосинтеза пенициллина G - это окислительный преобразование линейного ACV в бициклический промежуточный изопенициллин N по изопенициллин-N-синтаза (IPNS), который кодируется геном pcbC.[66][67] Изопенициллин N является очень слабым промежуточным звеном, потому что он не проявляет сильной антибиотической активности.[69]
- Последний шаг - это переамидирование к изопенициллин N N-ацилтрансфераза, в котором α-аминоадипильная боковая цепь изопенициллина N удалена и заменена на фенилацетил боковая цепь. Эта реакция кодируется геном penDE, что является уникальным в процессе получения пенициллинов.[66]
Смотрите также
Рекомендации
- ^ Уоллинг А.Д. (15 сентября 2006 г.). «Советы из других журналов - Использование антибиотиков во время беременности и кормления грудью». Американский семейный врач. 74 (6): 1035. Получено 25 сентября, 2015.
- ^ а б Гонсалес-Эстрада А., Радойич С. (май 2015 г.). «Аллергия на пенициллин: практическое руководство для врачей». Кливлендский медицинский журнал клиники. 82 (5): 295–300. Дои:10.3949 / ccjm.82a.14111. PMID 25973877. S2CID 6717270.
- ^ а б Кардос Н., Демейн А.Л. (ноябрь 2011 г.). «Пенициллин: лекарство, оказывающее наибольшее влияние на результаты лечения». Прикладная микробиология и биотехнология. 92 (4): 677–87. Дои:10.1007 / s00253-011-3587-6. PMID 21964640. S2CID 39223087.
- ^ «Открытие и разработка пенициллина». Американское химическое общество. Получено 30 августа 2015.
- ^ Оксфордский справочник по инфекционным болезням и микробиологии. ОУП Оксфорд. 2009. с. 56. ISBN 978-0-19-103962-1.
- ^ "пенициллин" - через The Free Dictionary.
- ^ Гаррод LP (февраль 1960 г.). «Относительная антибактериальная активность трех пенициллинов». Британский медицинский журнал. 1 (5172): 527–9. Дои:10.1136 / bmj.1.5172.527. ЧВК 1966560. PMID 13826674.
- ^ Гаррод LP (декабрь 1960 г.). «Относительная антибактериальная активность четырех пенициллинов». Британский медицинский журнал. 2 (5214): 1695–6. Дои:10.1136 / bmj.2.5214.1695. ЧВК 2098302. PMID 13703756.
- ^ «Пенициллин G и пенициллин V». ivertox.nih.gov. Получено 2016-09-25.
- ^ «Пенициллин (бензилпенициллин, пенициллин G, бициллин C-R / L-A, Pfizerpen, Wycellin)». Антимикробный индекс. База знаний. Получено 4 марта 2014.
- ^ «Данные о восприимчивости и устойчивости к натриевой соли пенициллина G» (PDF). ТОКУ-Э. Получено 4 марта 2014.
- ^ а б c Росси С., изд. (2006). Австралийский справочник по лекарствам. Аделаида: Австралийский справочник по лекарственным средствам. ISBN 978-0-9757919-2-9.
- ^ Бхаттачарья, Санджиб (2010). «Факты об аллергии на пенициллин: обзор». Журнал передовых фармацевтических технологий и исследований. 1 (1): 11–17. ЧВК 3255391. PMID 22247826.
- ^ Блюменталь, Кимберли Дж .; Питер, Джонни Дж .; Trubiano, Jason A .; Филлипс, Элизабет Дж. (2019). «Аллергия на антибиотики». Ланцет. 393 (10167): 183–198. Дои:10.1016 / S0140-6736 (18) 32218-9. ЧВК 6563335. PMID 30558872.
- ^ а б Хитчингс А, Лонсдейл Д., Беррейдж D, Бейкер Э (2015). 100 лучших лекарств: клиническая фармакология и практическое назначение. С. 174–181. ISBN 978-0-7020-5516-4.
- ^ Ким, Кван-Кюн (2015). «Синдром Николо: обзор литературы». Всемирный журнал дерматологии. 4 (2): 103. Дои:10.5314 / wjd.v4.i2.103.
- ^ Сапуто, В .; Бруни, Г. (1998). «Синдром Николау, вызванный препаратами пенициллина: обзор литературы в поисках потенциальных факторов риска». La Pediatria Medica e Chirurgica: Медицинская и хирургическая педиатрия. 20 (2): 105–123. PMID 9706633.
- ^ Йокум Р. Р., Расмуссен Дж. Р., Строминджер Дж. Л. (май 1980 г.). «Механизм действия пенициллина. Пенициллин ацилирует активный центр D-аланин карбоксипептидазы Bacillus stearothermophilus». Журнал биологической химии. 255 (9): 3977–86. PMID 7372662.
- ^ «Бензилпенициллин». www.drugbank.ca. Получено 22 января 2019.
- ^ а б Кушни Т.П., О'Дрисколл Н.Х., Лэмб А.Дж. (декабрь 2016 г.). «Морфологические и ультраструктурные изменения бактериальных клеток как показатель антибактериального механизма действия». Клеточные и молекулярные науки о жизни. 73 (23): 4471–4492. Дои:10.1007 / s00018-016-2302-2. HDL:10059/2129. PMID 27392605. S2CID 2065821.
- ^ Гордон Э., Муз Н., Дуэ Э, Дидеберг О. (июнь 2000 г.). «Кристаллическая структура пенициллин-связывающего белка 2x из Streptococcus pneumoniae и его ацил-ферментная форма: влияние на лекарственную устойчивость». Журнал молекулярной биологии. 299 (2): 477–85. Дои:10.1006 / jmbi.2000.3740. PMID 10860753.
- ^ Ван Бамбек Ф., Ламберт Д., Мингеот-Леклерк М., Тулкенс П. (1999). Механизм действия (PDF).
- ^ Winstanley TG, Hastings JG (февраль 1989 г.). «Пенициллин-аминогликозидный синергизм и постантибиотический эффект в отношении энтерококков». Журнал антимикробной химиотерапии. 23 (2): 189–99. Дои:10.1093 / jac / 23.2.189. PMID 2708179.
- ^ Кастен Б, Рески Р (30 марта 1997 г.). «β-лактамные антибиотики ингибируют деление хлоропластов в мхе (Physcomitrella patens), но не в томате (Lycopersicon esculentum)». Журнал физиологии растений. 150 (1–2): 137–140. Дои:10.1016 / S0176-1617 (97) 80193-9.
- ^ Mucsi Z, Chass GA, Ábrányi-Balogh P, Jójárt B, Fang DC, Ramirez-Cuesta AJ, et al. (Декабрь 2013). «Каталитический механизм пенициллина, раскрытый неупругими нейтронами и квантовой химической теорией». Физическая химия Химическая физика. 15 (47): 20447–20455. Bibcode:2013PCCP ... 1520447M. Дои:10.1039 / c3cp50868d. PMID 23760063.
- ^ Левисон М.Э., Левисон Дж. Х. (декабрь 2009 г.). «Фармакокинетика и фармакодинамика антибактериальных средств». Клиники инфекционных болезней Северной Америки. 23 (4): 791–815, vii. Дои:10.1016 / j.idc.2009.06.008. ЧВК 3675903. PMID 19909885.
- ^ Николау (1996), стр. 43.
- ^ Томас Дж. Догерти, Майкл Дж. Пуччи. Открытие и разработка антибиотиков. Springer Science & Business Media (2011). страницы 79–80
- ^ Ральф Ландау, Василий Ахилладелис, Александр Скрябин. Фармацевтические инновации: революция в здоровье человека. Фонд химического наследия (1999 г.). стр.162
- ^ Хейвен К.Ф. (1994). Чудеса науки: 50 увлекательных 5-минутных чтений. Литтлтон, Колорадо: Библиотеки без ограничений. п. 182. ISBN 978-1-56308-159-0.
- ^ Александр Флеминг (1929). «Об антибактериальном действии культур Penicillium с особым упором на их использование для выделения B. influenz». Британский журнал экспериментальной патологии. 10 (3): 226–236. ЧВК 2048009.Печатается как Флеминг, А. (1980). «Классика по инфекционным болезням». Отзывы об инфекционных заболеваниях. 2 (1): 129–39. Дои:10.1093 / Clinids / 2.1.129. ЧВК 2041430. PMID 6994200.
- ^ Houbraken J, Frisvad JC, Samson RA (июнь 2011 г.). «Пенициллин-продуцентный штамм Флеминга - это не Penicillium chrysogenum, а P. rubens». IMA грибок. 2 (1): 87–95. Дои:10.5598 / imafungus.2011.02.01.12. ЧВК 3317369. PMID 22679592.
- ^ а б c Лакс Э (2004). Плесень на пальто доктора Флори: история пенициллинового чуда. Холт в мягкой обложке. ISBN 978-0-8050-7778-0.
- ^ Крылов А.К. (1991). «Гастроэнтерологические аспекты клинической картины внутренних болезней». Терапевтический Архив. 63 (2): 139–41. PMID 2048009.
- ^ «Открытие и разработка пенициллина». Международные исторические химические достопримечательности. Американское химическое общество. Получено 21 августа, 2018.
- ^ Wainwright M, Swan HT (январь 1986 г.). «К.Г. Пейн и самые ранние сохранившиеся истории болезни пенициллина». История болезни. 30 (1): 42–56. Дои:10.1017 / S0025727300045026. ЧВК 1139580. PMID 3511336.
- ^ Хауи Дж. (Июль 1986 г.). «Пенициллин: 1929-40». Британский медицинский журнал. 293 (6540): 158–9. Дои:10.1136 / bmj.293.6540.158. ЧВК 1340901. PMID 3089435.
- ^ Уэйнрайт М. (январь 1987 г.). «История терапевтического использования сырого пенициллина». История болезни. 31 (1): 41–50. Дои:10,1017 / с0025727300046305. ЧВК 1139683. PMID 3543562.
- ^ а б Джонс Д.С., Джонс Д.Х. (01.12.2014). "Сэр Эдвард Пенли Абрахам CBE. 10 июня 1913 - 9 мая 1999". Биографические воспоминания членов Королевского общества. 60: 5–22. Дои:10.1098 / rsbm.2014.0002. ISSN 0080-4606.
- ^ "Эрнст Б. Чейн - Нобелевская лекция: химическая структура пенициллинов". www.nobelprize.org. Получено 2017-05-10.
- ^ а б c d «Сделать пенициллин возможным: вспоминает Норман Хитли». ScienceWatch. Thomson Scientific. 2007. Архивировано с оригинал 21 февраля 2007 г.. Получено 2007-02-13.
- ^ Леви С.Б. (2002). Парадокс антибиотиков: как неправильное использование антибиотиков разрушает их лечебные свойства. Da Capo Press. С. 5–7. ISBN 978-0-7382-0440-6.
- ^ Гроссман CM (июль 2008 г.). «Первое применение пенициллина в США». Анналы внутренней медицины. 149 (2): 135–6. Дои:10.7326/0003-4819-149-2-200807150-00009. PMID 18626052. S2CID 40197907.
- ^ Ротман Л. (14 марта 2016 г.). «История пенициллина: что случилось с первым американским пациентом». Время. Получено 12 марта 2019.
- ^ Mailer JS, Мейсон Б. «Пенициллин: лекарство-чудо медицины военного времени и его производство в Пеории, штат Иллинойс». lib.niu.edu. Получено 11 февраля, 2008.
- ^ а б Параскандола Дж. (1980). История антибиотиков: симпозиум. Американский институт истории фармации № 5. ISBN 978-0-931292-08-8.
- ^ Беллис М. «История пенициллина». Изобретатели. About.com. Получено 30 октября, 2007.
- ^ Лерер С (2006). Исследователи тела: драматические открытия в медицине от древних времен до современной науки (2-е изд.). Нью-Йорк: iUniverse. С. 329–330. ISBN 978-0-595-40731-6.
- ^ Гринвуд Д. (2008). Противомикробные препараты: хроника триумфа медицины двадцатого века. Оксфорд: Издательство Оксфордского университета. п. 109. ISBN 978-0-19-953484-5.
- ^ Мадхаван Джи (20 августа 2015 г.). Думай как инженер. Публикации Oneworld. С. 83–85, 91–93. ISBN 978-1-78074-637-1. Получено 20 ноября 2016.
- ^ «Исторический маркер Г. Раймонда Реттью». ИсследуйтеPAhistory.com. Получено 27 июня, 2019.
- ^ Эндрю Джексон Мойер, Метод получения пенициллина, Патентное ведомство США, патент США 2442141, поданный 11 мая 1945 г., выданный 25 марта 1948 г.
- ^ Эндрю Джексон Мойер, Метод производства пенициллина, Патентное ведомство США, патент США 2443 989, поданный 11 мая 1945 г., выданный 22 июня 1948 г.
- ^ Эндрю Джексон Мойер, Метод производства пенициллина, Патентное ведомство США, патент США 2 476 107, поданный 11 мая 1945 г., выданный 12 июля 1949 г.
- ^ а б Silverthorn DU (2004). Физиология человека: комплексный подход (3-е изд.). Река Верхний Сэдл (Нью-Джерси): Пирсон Образование. ISBN 978-0-8053-5957-2.
- ^ «Открытие и разработка пенициллина». Американское химическое общество. 1999.
- ^ Нобелевская премия по химии 1964 г., перспективы. Проверено 14 июля 2012 года.
- ^ Шихан Дж. К., Хэнери-Логан К. Р. (5 марта 1957 г.). «Полный синтез пенициллина V». Журнал Американского химического общества. 79 (5): 1262–1263. Дои:10.1021 / ja01562a063.
- ^ Шихан Дж. К., Хенери-Логан КР (20 июня 1959 г.). «Полный синтез пенициллина V». Журнал Американского химического общества. 81 (12): 3089–3094. Дои:10.1021 / ja01521a044.
- ^ а б c Кори ЭДжей, Робертс Дж. Д.. «Биографические воспоминания: Джон Кларк Шиэн». Национальная академия прессы. Получено 28 января, 2013.
- ^ Николау KC, Вурлумис Д., Винссингер Н., Баран П.С. (Январь 2000 г.). «Искусство и наука полного синтеза на заре двадцать первого века». Angewandte Chemie. 39 (1): 44–122. Дои:10.1002 / (SICI) 1521-3773 (20000103) 39: 1 <44 :: AID-ANIE44> 3.0.CO; 2-L. PMID 10649349.
- ^ "Профессор Джон С. Шихан умер в 76 лет". Новости MIT. 1 апреля 1992 г.. Получено 28 января, 2013.
- ^ Шихан JC (1982). Зачарованное кольцо: невыразимая история пенициллина. MIT Press. ISBN 978-0-262-19204-0.
- ^ Колли EW, Mcnicol MW, Bracken PM (март 1965 г.). «Метициллин-резистентные стафилококки в больнице общего профиля». Ланцет. 1 (7385): 595–7. Дои:10.1016 / S0140-6736 (65) 91165-7. PMID 14250094.
- ^ Джеймс CW, Гурк-Тернер C (январь 2001 г.). «Перекрестная реактивность бета-лактамных антибиотиков». Труды. 14 (1): 106–7. Дои:10.1080/08998280.2001.11927741. ЧВК 1291320. PMID 16369597.
- ^ а б c Аль-Абдалла К., Брахаге А.А., Герке А., Платтнер Х., Спроте П., Тунчер А. (2004). «Регуляция биосинтеза пенициллина в нитчатых грибах». В Брахаге А.А. (ред.). Молекулярная биотехнология грибковых бета-лактамных антибиотиков и родственных пептидных синтетаз. Достижения в области биохимической инженерии / биотехнологии. 88. С. 45–90. Дои:10.1007 / b99257. ISBN 978-3-540-22032-9. PMID 15719552.
- ^ а б Брахейдж А.А. (сентябрь 1998 г.). «Молекулярная регуляция биосинтеза бета-лактама в мицелиальных грибах». Обзоры микробиологии и молекулярной биологии. 62 (3): 547–85. Дои:10.1128 / MMBR.62.3.547-585.1998. ЧВК 98925. PMID 9729600.
- ^ Шофилд С.Дж., Болдуин Дж.Э., Байфорд М.Ф., Клифтон И., Хайду Дж., Хенсгенс С., Роуч П. (декабрь 1997 г.). «Белки пути биосинтеза пенициллина». Текущее мнение в структурной биологии. 7 (6): 857–64. Дои:10.1016 / s0959-440x (97) 80158-3. PMID 9434907.
- ^ а б Мартин Дж. Ф., Гутьеррес С., Фернандес Ф. Дж., Веласко Дж., Фиерро Ф., Маркос А. Т., Косалькова К. (сентябрь 1994 г.). «Экспрессия генов и процессинг ферментов биосинтеза пенициллинов и цефалоспоринов». Антони ван Левенгук. 65 (3): 227–43. Дои:10.1007 / BF00871951. PMID 7847890. S2CID 25327312.
- ^ Baker WL, Lonergan GT (декабрь 2002 г.). «Химия некоторых производных флуорескамина и амина, имеющих отношение к биосинтезу бензилпенициллина путем ферментации». Журнал химической технологии и биотехнологии: международные исследования процессов, окружающей среды и чистых технологий. 77 (12): 1283–8. Дои:10.1002 / jctb.706.
дальнейшее чтение
- Николау KC, Кори ЭДжей (1996). Классика в полном синтезе: цели, стратегии, методы (5-е изд.). Вайнхайм: ВЧ. ISBN 978-3-527-29284-4.
- Dürckheimer W, Blumbach J, Lattrell R, Scheunemann KH (1 марта 1985 г.). «Последние разработки в области β-лактамных антибиотиков». Angewandte Chemie International Edition на английском языке. 24 (3): 180–202. Дои:10.1002 / anie.198501801.
- Хамед РБ, Гомес-Кастелланос-младший, Генри Л., Дучо К., Макдоно, Массачусетс, Шофилд CJ (Январь 2013). «Ферменты биосинтеза β-лактамов». Отчеты о натуральных продуктах. 30 (1): 21–107. Дои:10.1039 / c2np20065a. PMID 23135477.
внешняя ссылка
- Модель структуры пенициллина, Дороти Ходжкин и др., Музей истории науки, Оксфорд.
- Открытие пенициллина, правительство сняло фильм об открытии пенициллина сэром Александром Флемингом и продолжающемся развитии его использования в качестве антибиотика Говардом Флори и Эрнстом Борисом Чейном. на YouTube.
- Пенициллин в Периодическая таблица видео (Ноттингемский университет)
- Пенициллин, пропущенный гражданским лицам, будет стоить 35 долларов на пациента Популярная наука, Август 1944 г., статья внизу страницы
