Мускимол - Википедия - Muscimol
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК 5- (Аминометил) -1,2-оксазол-3 (2H) -он | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.018.574 |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики[1] | |
| C4ЧАС6N2О2 | |
| Молярная масса | 114.104 г · моль−1 |
| Температура плавления | От 184 до 185 ° C (от 363 до 365 ° F, от 457 до 458 K) |
| очень растворимый | |
| Растворимость в этаноле | слабо растворимый |
| Растворимость в метанол | очень растворимый |
| Фармакология | |
| Легальное положение |
|
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Muscimol (также известный как агарин или же пантера) является одним из основных психоактивный составляющие Мухомор мухомор и родственные виды грибов. Мусцимол является сильнодействующим селективным агонист для ГАМКА рецепторы[нужна цитата ] и отображает успокаивающе-снотворное, депрессант и галлюциногенный психоактивность. Это бесцветное или белое твердое вещество классифицируется как изоксазол.
Мусцимол проходил фазу клинических испытаний I по поводу эпилепсии, но исследование было прекращено.[2]
Биохимия
Мусцимол - одно из психоактивных соединений, ответственных за действие Мухомор мухомор интоксикация. Иботеновая кислота, а нейротоксичный вторичный метаболит из Мухомор мухомор, служит пролекарство в мусцимол при употреблении в пищу или сушке, преобразование в мусцимол через декарбоксилирование.[нужна цитата ]
Мускимол производится из грибов. Мухомор мухомор (мухомор) и Мухомор пантера, вместе с мускарин (который присутствует в следовых количествах и не активен), Muscazone, и иботеновая кислота.[3][4] A. muscaria и А. пантера следует есть с осторожностью и должным образом подготовить, чтобы уменьшить последствия тошноты. В A. muscaria, слой чуть ниже кожи шляпки содержит наибольшее количество мусцимола и, следовательно, является наиболее психоактивный часть.[5]

Фармакология

Мусцимол - сильнодействующий ГАМКА агонист, активируя рецептор для главного тормозящий нейротрансмиттер, ГАМК. Мускимол связывается с тем же сайтом на ГАМКА рецепторный комплекс как сама ГАМК, в отличие от других ГАМКергических препаратов, таких как барбитураты и бензодиазепины которые связываются с отдельными регулирующими сайтами.[6] ГАМКА рецепторы широко распространены в головном мозге, поэтому при введении мусцимола он изменяет активность нейронов во многих областях, включая кора головного мозга, гиппокамп, и мозжечок. В то время как мусцимол обычно считается селективным ГАМКА агонист с исключительно высоким сродством к ГАМКА-дельта-рецепторы,[7][8][9] он также является частичным агонистом ГАМКА-ро рецептор, и поэтому спектр его эффектов является результатом комбинированного действия более чем на одну ГАМКА подтип рецептора.[10]
Психоактивная доза мусцимола составляет около 10-15 мг для нормального человека.[11] Руководство по британским псилоцибиновым грибам Ричард Купер, опубликованный в 1977 году, рекомендует меньшую дозу, 8,5 мг, и предполагает, что это количество может присутствовать всего в 1 г сушеного A. muscaria[12] но это не согласуется с большинством других отчетов, которые предполагают, что 5–10 мг необходимо. Трудно определить правильную дозу, потому что эффективность сильно варьируется от одного гриба к другому.[11]
При употреблении значительный процент мусцимола не метаболизируется и, таким образом, выводится с мочой - феномен, используемый практиками традиционной медицины. энтеогенный использование Мухомор мухомор.[13]
У пациентов с болезнь Хантингтона и хронический шизофрения было обнаружено, что пероральные дозы мусцимола вызывают повышение как пролактина, так и гормона роста.[14]
Во время теста с участием кроликов, подключенных к ЭЭГ мусцимол имеет отчетливо выраженную синхронизированный ЭЭГ отслеживание. Это существенно отличается от серотонинергические психоделики, с которыми паттерны мозговых волн обычно демонстрируют десинхронизацию. В более высоких дозах (2 мг / кг через IV ) ЭЭГ покажет характерные всплески.[15]
Последствия
Действие мусцимола начинается через 30–120 минут после приема и длится 5–10 часов.[нужна цитата ] К ним относятся эйфория, сказочный (ясный ) душевное состояние, внетелесный опыт и синестезия.[нужна цитата ] Отрицательные эффекты включают от легких до умеренных. тошнота, дискомфорт в животе, повышенный слюноотделение и мышечные подергивания или тремор. В больших дозах сильное диссоциация или же бред может ощущаться.[нужна цитата ]
Многие из эффектов мусцимола согласуются с его фармакологией как ГАМКА рецептор агонист, представляя многие депрессант или же успокаивающее -гипнотический последствия. Нетипичный профиль действия седативных препаратов в целом, однако мусцимол, как и Z-препараты, может вызвать галлюциногенный изменения в восприятии. Галлюциногенный эффект мусцимола наиболее близко сопоставим с галлюциногенными побочными эффектами, вызываемыми некоторыми другими препаратами. ГАМКергический наркотики, такие как золпидем.[нужна цитата ]
Химия
Структура
Мускимол был впервые выделен из Мухомор пантера Онда в 1964 году,[16] и считался аминокислота или же пептид. Структура была затем разъяснена Такемото,[17] Эугстер,[18] и Боуден.[19] Мусцимол - полужесткий изоксазол содержащий оба алкоголь и аминометил заместители.[20] Мускимол обычно изображается как таутомер, где он принимает амид -подобная конфигурация.[21] Также обычно отображается как цвиттерион.[22]
Изоляция
Мускимол можно извлечь из мякоти Мухомор мухомор обработкой кипятком с последующим быстрым охлаждением и последующей обработкой базовый смола. Его промывают водой и элюированный с уксусная кислота с помощью колоночная хроматография. В элюировать сушат вымораживанием, растворяют в воде и пропускают через столбец фосфат целлюлозы.[23] Последующее элюирование гидроксид аммония и перекристаллизация из алкоголя приводит к чистому мусцимолу.[24]
В случаях, когда чистый мусцимол не требуется, например, для рекреационных или духовных целей, неочищенный экстракт часто готовят путем кипячения сушеного Мухомор мухомор в воде на тридцать минут.[25]
Химический синтез
Мусцимол был синтезирован в 1965 году Gagneux,[26] которые использовали исходный бромизоксазол в двухстадийной реакции. 3-бром-5-аминометилизоксазол (1) кипятили с обратным холодильником в смеси Метанол и Гидроксид калия в течение 30 часов с получением 3-метокси-5-аминометилизоксазола (2) с выходом 60%.

(2) затем кипятили с обратным холодильником в концентрированном соляная кислота к гидролизовать в метокси группа, а цвиттерион кристаллизовался из раствора метанол и тетрагидрофуран после добавления триэтиламин, что дает доходность 50%.[26]

Химики сообщают, что им не удалось воспроизвести эти результаты.[27][28] Были разработаны более надежные и масштабируемые процедуры, двумя примерами которых являются синтезы МакКарри.[29] и Вараси.[30]
Синтез Маккарри представляет собой трехэтапный синтез, включающий литий ацетилид произведено из пропаргил хлорид. Ацетилид (3) растворяли в эфир, охладили до -40 ° С и обработали избытком пропаргил хлорид с получением этил-4-хлортетролата (4) с выходом 70%. (4) затем добавляли к раствору воды, метанол и гидроксиламин при -35 ° C. На pH между 8,5 и 9 изоксазол (5) был извлечен с выходом 41%. Мускимол образовывался с выходом 65%, когда (5) растворяли в насыщенном растворе метанол и безводный аммиак и нагревают от 0 ° C до 50 ° C. Общая доходность составила 18,7%.[31]

Синтез Вараси отличается недорогими исходными материалами и мягкими условиями. Он начинается с комбинации 2,3-дихлор-1-пропена (6), бикарбонат калия, воды, и дибромформальдоксим (7), все растворенные в ацетат этила. 5-Хлорметил-3-бромизоксазол (8) экстрагировали с экспериментальным выходом 81%. 5-Аминометил-3-бромизоксазол (9) был получен с выходом 90% комбинацией (8) и гидроксид аммония в диоксан.[32]
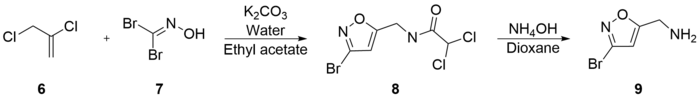
(9) затем кипятили с обратным холодильником гидроксид калия в метанол с получением 5-аминометил-3-метоксиизоксазола (10) с выходом 66%. Последующий отлив (10) с бромистоводородная кислота и уксусная кислота произвел мусцимол с выходом 62%. Общий синтетический выход составил 30%.[33]

Токсичность
В средняя смертельная доза у мышей - 3,8 мг / кг подкожно, 2,5 мг / кг внутрибрюшинно. LD50 у крыс - 4,5 мг / кг в / в, 45 мг / кг перорально.[34]
Смертельные случаи среди людей случаются редко, главным образом среди детей раннего возраста, пожилых людей или людей с серьезными хроническими заболеваниями.[35]
Легальное положение
Австралия
Мусцимол считается запрещенным веществом Списка 9 в Австралии в соответствии с Стандарт ядов (Октябрь 2015 г.). Вещество из Списка 9 - это вещество, «которым можно злоупотреблять или использовать не по назначению, производство, владение, продажа или использование которого должны быть запрещены законом, за исключением случаев, когда это требуется для медицинских или научных исследований, или для аналитических, учебных или учебных целей с одобрения Органы здравоохранения Содружества и / или штата или территории ".[36]
Соединенные Штаты
Ни один Мухомор мухомор ни мусцимол не считается контролируемым веществом Федеральное правительство США. Это означает, что выращивание, хранение и распространение не регулируются федеральным правительством США.[37][38]
Мусцимол может регулироваться на государственном уровне. Закон штата Луизиана 159 запретил владение и выращивание Мухомор мухомор кроме декоративных или эстетических целей. Этот закон ставит вне закона подготовку Мухомор мухомор предназначен для употребления в пищу, включая мусцимол.[39]
Смотрите также
Рекомендации
- ^ Индекс Merck, 12-е издание
- ^ Lonser, Russell R .; Олдфилд, Эдвард Х .; Сато, Сусуму; Рене Смит, Р. Н .; Уолбридж, Стюарт; Хейсс, Джон Д. (2012-08-01). «174 Конвекционно-усиленная доставка Muscimol в эпилептический центр. Доклинические и клинические исследования». Нейрохирургия. 71 (2): E568. Дои:10.1227 / 01.neu.0000417764.02569.dc. ISSN 0148-396X.
- ^ Чилтон, WS; Отт, Дж (1976). «Токсичные метаболиты Мухомор пантера, А. Котурната, А. Мускария и другие Мухомор разновидность". Ллойдия. 39 (2–3): 150–7. PMID 985999.
- ^ а б Michelot, D; Мелендес-Хауэлл, LM (2003). "Мухомор мухомор: химия, биология, токсикология, этномикология ». Микологические исследования. 107 (Чт 2): 131–46. Дои:10.1017 / S0953756203007305. PMID 12747324.
- ^ Чилтон, WS (1978). «Химия и механизм действия грибных токсинов». In Rumack, BH; Зальцман, Э (ред.). Отравление грибами: диагностика и лечение. Палм-Бич: CRC Press. С. 87–124. ISBN 9780849351853.
- ^ Frølund, B; Эберт, B; Kristiansen, U; Liljefors, T; Крогсгаард-Ларсен, П. (2002). «Лиганды рецепторов ГАМК-А и их терапевтические возможности». Актуальные темы медицинской химии. 2 (8): 817–32. Дои:10.2174/1568026023393525. PMID 12171573.
- ^ Quirk, K .; Whiting, P.J .; Ragan, C.I .; МакКернан, Р. М. (1995-08-15). «Характеристика дельта-субъединицы, содержащей рецепторы GABAA из головного мозга крысы». Европейский журнал фармакологии. 290 (3): 175–181. Дои:10.1016/0922-4106(95)00061-5. ISSN 0014-2999. PMID 7589211.
- ^ Chandra, D .; Jia, F .; Liang, J .; Peng, Z .; Сурьянараянан, А .; Вернер, Д. Ф .; Spigelman, I .; Houser, C.R .; Олсен, Р. В. (2006-10-10). «Субъединицы альфа-4 рецептора ГАМКА опосредуют внесинаптическое торможение в таламусе и зубчатой извилине, а также действие габоксадола». Труды Национальной академии наук Соединенных Штатов Америки. 103 (41): 15230–15235. Bibcode:2006PNAS..10315230C. Дои:10.1073 / pnas.0604304103. ISSN 0027-8424. ЧВК 1578762. PMID 17005728.
- ^ Benkherouf, Ali Y .; Тайна, Кайса-Риитта; Мира, Пратап; Аалто, Аско Дж .; Ли, Сян-Го; Soini, Sanna L .; Валлнер, Мартин; Ууси-Оукари, Микко (06.03.2019). «Внесинаптические рецепторы δ-ГАМК А представляют собой высокоаффинные рецепторы мусцимола». Журнал нейрохимии. 149 (1): 41–53. Дои:10.1111 / jnc.14646. ЧВК 6438731. PMID 30565258.
- ^ Вудворд, РМ; Polenzani, L; Миледи, Р. (1993). «Характеристика нечувствительных к бикукуллину / баклофену (ро-подобных) рецепторов гамма-аминомасляной кислоты, экспрессируемых в ооцитах Xenopus. II. Фармакология агонистов и антагонистов рецепторов гамма-аминомасляной кислоты А и гамма-аминомасляной кислоты В». Молекулярная фармакология. 43 (4): 609–25. PMID 8386310.
- ^ а б "Erowid Psychoactive Amanitas Vault: дозировка". www.erowid.org. Получено 2018-04-05.
- ^ Ричард., Купер (1979). Путеводитель по британским псилоцибиновым грибам (Ред. Ред.). Лондон (BCM Box 311, London, WC1V, 6XX): Hassle Free Press. ISBN 9780861660049. OCLC 7605366.CS1 maint: location (связь)
- ^ Гольдштейн А. (2001). Зависимость: от биологии к наркополитике. Издательство Оксфордского университета. п. 228. ISBN 978-0-19-514664-6.
- ^ Тамминга, Калифорния; Неофитиды, А; Чейз, штат Теннесси; Фроман, Л.А. (1978). «Стимуляция секреции пролактина и гормона роста мусцимолом, агонистом гамма-аминомасляной кислоты». Журнал клинической эндокринологии и метаболизма. 47 (6): 1348–51. Дои:10.1210 / jcem-47-6-1348. PMID 162520.
- ^ Каролис, А. Скотти Де; Lipparini, F .; Лонго, В. Г. (1969-01-01). «Нейрофармакологические исследования мусцимола, психотропного препарата, извлекаемого из мухомора мухомора». Психофармакология. 15 (3): 186–195. Дои:10.1007 / BF00411168. ISSN 0033-3158. PMID 5389124.
- ^ Онда, Масаюки; Фукусима, Хироши; Акагава, Масуко (1964). "Мухоловая составляющая Amanita pantherina (DC.) FR". Химико-фармацевтический бюллетень. 12 (6): 751. Дои:10.1248 / cpb.12.751. PMID 14199180.
- ^ Такемото, Т. (1964). J. Pharm. Soc. Япония. 84: 1232. Отсутствует или пусто
| название =(помощь) - ^ Эустер, С. (1965). «Активные ингредиенты из Amanita muscaria: иботеновая кислота и мусказон». Буквы Тетраэдра (23): 1813–5. Дои:10.1016 / S0040-4039 (00) 90133-3. PMID 5891631.
- ^ Боуден, К. (1965). «Составляющие Amanita muscaria». Природа. 206 (991): 1359–60. Bibcode:1965Натура.206.1359Б. Дои:10.1038 / 2061359a0. PMID 5891274.
- ^ Брем, Лотте; Фриденванг, Карла; Хансен, Лене Мерете; Норрби, Пер-Ола; Крогсгаард-Ларсен, Повл; Лильефорс, Томми (декабрь 1997 г.). «Структурные особенности мусцимола, сильнодействующего агониста рецепторов ГАМК, кристаллическая структура и расчеты квантового химического ab initio». Структурная химия. 8 (6): 443–451. Дои:10.1007 / BF02311703.
- ^ «Мускимол». pubchem.ncbi.nlm.nih.gov.
- ^ «Улучшенный синтез мускимола». Синтетические коммуникации. 22 (13): 1939–1948. 1992. Дои:10.1080/00397919208021324.
- ^ «Фосфат целлюлозы: информация о продукте» (PDF). Сигма Олдрич. Получено 23 апреля 2020.
- ^ Bowden, K .; Дрисдейл, А.С. (январь 1965 г.). "Новая составляющая". Буквы Тетраэдра. 6 (12): 727–728. Дои:10.1016 / S0040-4039 (01) 83973-3. PMID 14291871.
- ^ Генрих, Кларк. "Erowid Psychoactive Amanitas (A. muscaria & A. pantherina) Vault: Amanita muscaria Preparation for Beginners". erowid.org. Получено 6 мая 2020.
- ^ а б Gagneux, A.R .; Häfliger, F .; Eugster, C.H .; Гуд Р. (январь 1965 г.). «Синтез пантерина (агарина)». Буквы Тетраэдра. 6 (25): 2077–2079. Дои:10.1016 / S0040-4039 (00) 90157-6.
- ^ Chiarino, D .; Наполетано, М .; Сала, А. (1986). «Удобный синтез мусцимола по реакции 1,3-диполярного циклоприсоединения». Буквы Тетраэдра. 27 (27): 3181–3182. Дои:10.1016 / S0040-4039 (00) 84748-6.
- ^ Bowden, K .; Crank, G .; Росс, В. Дж. (1968). «Синтез пантерина и родственных ему соединений». Журнал химического общества C: Органический: 172. Дои:10.1039 / j39680000172.
- ^ Маккарри, Брайан Э .; Савар, Марк (январь 1981). «Легкий синтез мусцимола». Буквы Тетраэдра. 22 (51): 5153–5156. Дои:10.1016 / S0040-4039 (01) 92445-1.
- ^ Вараси, М. (июль 1992 г.). «Улучшенный синтез мускимола». Синтетические коммуникации. 22 (13): 1939–1948. Дои:10.1080/00397919208021324.
- ^ Маккарри, Брайан Э .; Савар, Марк (январь 1981). «Легкий синтез мусцимола». Буквы Тетраэдра. 22 (51): 5153–5156. Дои:10.1016 / S0040-4039 (01) 92445-1.
- ^ «Улучшенный синтез мускимола». Синтетические коммуникации. 22 (13): 1939–1948. Июль 1992 г. Дои:10.1080/00397919208021324.
- ^ «Улучшенный синтез мускимола». Синтетические коммуникации. 22 (13): 1939–1948. Июль 1992 г. Дои:10.1080/00397919208021324.
- ^ "Erowid Psychoactive Amanitas Vault: Химия". www.erowid.org. Получено 2018-04-05.
- ^ Сперк, Дэвид (Эд) (1994). Справочник при отравлении грибами: диагностика и лечение. Бока-Ратон: CRC Press. п. 269. ISBN 978-0-8493-0194-0. OCLC 29913834.CS1 maint: дополнительный текст: список авторов (связь), Предварительный просмотр Google Книг.
- ^ Стандарт ядов, октябрь 2015 г. https://www.comlaw.gov.au/Details/F2015L01534
- ^ «Таблицы контролируемых веществ». www.deadiversion.usdoj.gov. Министерство юстиции США. Получено 6 мая 2020.
- ^ Эровид. «Хранилище Erowid Psychoactive Amanitas: правовой статус». erowid.org. Получено 6 мая 2020.
- ^ "Закон Луизианы № 159". Законодательство.la.gov. Законодательное собрание штата Луизиана. Получено 6 мая 2020.

