Валиномицин - Valinomycin
 | |
 | |
| Имена | |
|---|---|
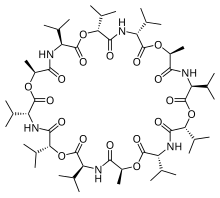
| Название ИЮПАК цикло [N-окса-D-аланил-D-валил-N-окса-L-валил-D-валил-N-окса-D-аланил-D-валил-N-окса-L-валил-L-валил- N-окса-L-аланил-L-валил-N-окса-L-валил-L-валил] | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.016.270 |
| UNII | |
| |
| |
| Характеристики | |
| C54ЧАС90N6О18 | |
| Молярная масса | 1111,32 г / моль |
| Внешность | Белое твердое вещество |
| Температура плавления | 190 ° С (374 ° F, 463 К) |
| Растворимость | Метанол, этанол, этилацетат, петролейный эфир, дихлорметан |
| УФ-видимый (λМаксимум) | 220 нм |
| Опасности | |
| Главный опасности | Нейротоксикант |
| Смертельная доза или концентрация (LD, LC): | |
LD50 (средняя доза ) | 4 мг / кг (перорально, крыса)[2] |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Валиномицин является естественным додекадепсипептид используется при транспортировке калий и как антибиотик. Валиномицин получают из клеток нескольких Streptomyces разновидность, S. fulvissimus быть заметным.
Входит в группу естественных нейтральных ионофоры потому что в нем нет остаточного заряда. Это состоит из энантиомеры D- и L-валин (Val), D-альфа-гидроксиизовалериановая кислота, и я-молочная кислота. Структуры попеременно связываются через амид и сложный эфир мосты. Валиномицин обладает высокой селективностью к калий ионы над натрий ионы внутри клеточная мембрана.[3] Он действует как специфический переносчик калия и способствует перемещению ионов калия через липидные мембраны «вниз» по градиенту электрохимического потенциала.[4] В константа стабильности K для комплекса калий-валиномицин почти в 100000 раз больше, чем K для комплекса натрий-валиномицин.[5]Это различие важно для поддержания селективности валиномицина в отношении транспорта ионов калия (а не ионов натрия) в биологических системах.
Классифицируется как чрезвычайно опасное вещество в Соединенных Штатах, как определено в Разделе 302 США Закон о чрезвычайном планировании и праве общества на информацию (42 U.S.C. 11002), и к ним предъявляются строгие требования к отчетности со стороны предприятий, которые производят, хранят или используют его в значительных количествах.[6]
Структура
Валиномицин - додекадепсипептид, то есть он состоит из двенадцати чередующихся аминокислоты и сложные эфиры с образованием макроциклической молекулы. Двенадцать карбонил группы необходимы для связывания ионов металлов, а также для сольватация в полярный растворитель. В изопропил и метил группы отвечают за сольватацию в неполярные растворители.[7] Наряду с его формой и размером эта молекулярная двойственность является основной причиной его связывающих свойств. Ионы К должны отказаться от своей гидратной воды, чтобы пройти через поры. K+ ионы октаэдрически координированы в квадратной бипирамидальной геометрии 6 карбонильными связями от Val. В этом пространстве 1,33 Ангстрема, Na+ с радиусом 0,95 Ангстрема значительно меньше канала, а это означает, что Na+ не может образовывать ионные связи с аминокислотами поры с энергией, эквивалентной той, которую он отдает с молекулами воды. Это приводит к 10,000-кратной селективности для K+ ионы над Na+. В случае полярных растворителей валиномицин в основном подвергает карбонилы действию растворителя, а в неполярных растворителях изопропильные группы расположены преимущественно на внешней стороне молекулы. Эта конформация изменяется, когда валиномицин связывается с ионом калия. Молекула «заперта» в конформации с изопропильными группами снаружи. На самом деле он не привязан к конфигурации, потому что размер молекулы делает его очень гибким, но ион калия придает макромолекуле некоторую степень координации.
Приложения
Недавно сообщалось, что валиномицин является наиболее мощным средством против коронавируса тяжелого острого респираторного синдрома (SARS-CoV) у инфицированных Клетки Vero E6.[нужна цитата ]
Валиномицин действует как неметаллическое изоформирующее средство в калиевые селективные электроды.[8][9]
Этот ионофор используется для изучения мембранные везикулы, где он может быть выборочно применен в соответствии с планом эксперимента для уменьшения или устранения электрохимического градиента через мембрану.[нужна цитата ]
Рекомендации
- ^ "ChemIDplus - 2001-95-8 - FCFNRCROJUBPLU-DNDCDFAISA-N - Валиномицин - Поиск похожих структур, синонимов, формул, ссылок на ресурсы и другой химической информации".
- ^ «ChemIDplus - 2001-95-8 - FCFNRCROJUBPLU-DNDCDFAISA-N - Валиномицин - Поиск похожих структур, синонимов, формул, ссылок на ресурсы и другой химической информации».
- ^ Ларс, Роза; Дженкинс АТА (2007). «Влияние ионофора валиномицина на биомиметические твердые липидные мембраны DPPTE / EPC». Биоэлектрохим. 70 (2): 387–393. Дои:10.1016 / j.bioelechem.2006.05.009. PMID 16875886.
- ^ Камманн К. (1985). «Ионоселективные объемные мембраны как модели». Вершина. Curr. Chem. Темы современной химии. 128: 219–258. Дои:10.1007/3-540-15136-2_8. ISBN 978-3-540-15136-4.
- ^ Rose, M.C .; Хенкенс, Р.В. (1974). «Устойчивость натриевых и калиевых комплексов валиномицина». Biochimica et Biophysica Acta (BBA) - Общие предметы. 372 (2): 426–435. Дои:10.1016/0304-4165(74)90204-9.
- ^ «40 C.F.R .: Приложение A к Части 355 - Список особо опасных веществ и их планируемые пороговые количества» (PDF) (1 июля 2008 г. ред.). Государственная типография. Получено 29 октября, 2011. Цитировать журнал требует
| журнал =(помощь) - ^ Томпсон М., Крулл У. Дж. (1982). «Электроаналитический ответ двухслойной липидной мембраны на валиномицин: содержание холестерина в мембране». Анальный. Чим. Acta. 141: 33–47. Дои:10.1016 / S0003-2670 (01) 95308-5.
- ^ Сафиулина Д., Векслер В., Жарковский А., Каасик А. (2006). «Потеря митохондриального мембранного потенциала связана с увеличением объема митохондрий: физиологическая роль в нейронах». J. Cell. Physiol. 206 (2): 347–353. Дои:10.1002 / jcp.20476. PMID 16110491.
- ^ Бюллетень по ионофору калия
внешняя ссылка
- Правила химической безопасности из Департамент здравоохранения Нью-Джерси.
- Информация о здоровье на карте показателей.
- Валиномицин из Ферментек.
- Валиномицин в базе данных о свойствах пестицидов (PPDB)
