Ферредоксин - Ferredoxin
Ферредоксины (из латинский железо: утюг + редокс, часто сокращенно "fd") являются железо-серные белки это посредник перенос электронов в ряде метаболических реакций. Термин «ферредоксин» был введен Д. К. Уортоном из DuPont Co. и применен к «железному белку», впервые очищенному в 1962 г. Мортенсоном, Валентином и Карнаханом из анаэробный бактерия Clostridium pasteurianum.[1][2]
Еще один редокс-белок, выделенный из шпината хлоропласты, получил название «хлоропластный ферредоксин».[3] Ферредоксин хлоропласта участвует как в циклическом, так и в нециклическом фотофосфорилирование реакции фотосинтез. При нециклическом фотофосфорилировании ферредоксин является последним акцептором электронов, уменьшая таким образом фермент НАДФ.+ редуктаза. Он принимает электроны, полученные из Солнечный свет -в восторге хлорофилл и передает их ферменту ферредоксину: НАДФ+ оксидоредуктаза EC 1.18.1.2.
Ферредоксины - это небольшие белки, содержащие утюг и сера атомы организованы как железо-серные кластеры. Эти биологические "конденсаторы «может принимать или разряжать электроны с эффектом изменения степени окисления атомов железа от +2 до +3. Таким образом, ферредоксин действует как агент переноса электронов в биологических редокс реакции.
Другой биоинорганический системы транспорта электронов включают рубредоксины, цитохромы, белки голубой меди, а структурно связанные Белки Риске.
Ферредоксины можно классифицировать по природе их железо-серных кластеров и по сходству последовательностей.
Fe2S2 ферредоксины
| 2Fe-2S связывающий домен железо-серного кластера | |||||||||
|---|---|---|---|---|---|---|---|---|---|
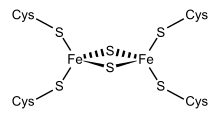 Структурное представление Fe2S2 ферредоксин. | |||||||||
| Идентификаторы | |||||||||
| Символ | Fer2 | ||||||||
| Pfam | PF00111 | ||||||||
| Pfam клан | CL0486 | ||||||||
| ИнтерПро | IPR001041 | ||||||||
| PROSITE | PDOC00642 | ||||||||
| SCOP2 | 3fxc / Объем / СУПФАМ | ||||||||
| Белок OPM | 1kf6 | ||||||||
| |||||||||
Члены суперсемейства 2Fe – 2S ферредоксинов (ИнтерПро: IPR036010 ) имеют общую структуру ядра, состоящую из бета (2) -альфа-бета (2), которая включает путидаредоксин, терпредоксин и адренодоксин.[4][5][6][7] Это белки, состоящие примерно из ста аминокислот с четырьмя консервативными остатками цистеина, с которыми лигируется кластер 2Fe – 2S. Эта консервативная область также обнаруживается в качестве домена в различных метаболических ферментах и в мультидоменных белках, таких как альдегид-оксидоредуктаза (N-концевой), ксантиноксидаза (N-концевой), редуктазы фталатдиоксигеназы (C-терминал), сукцинатдегидрогеназа железо-серный белок (N-концевой) и редуктазы метанмонооксигеназы (N-Терминал).
Ферредоксины растительного типа
Одна группа ферредоксинов, первоначально обнаруженных в хлоропласт мембраны, был назван «хлоропластным» или «растительным» (ИнтерПро: IPR010241 ). Его активный центр - [Fe2S2] кластер, в котором атомы железа тетраэдрически координированы как атомами неорганической серы, так и серами четырех консервативных цистеин (Cys) остатки.
В хлоропластах Fe2S2 ферредоксины функционируют как переносчики электронов в фотосинтетическая цепь переноса электронов и в качестве доноров электронов для различных клеточных белков, таких как глутаматсинтаза, нитритредуктаза, сульфитредуктаза и циклаза биосинтеза хлорофилла.[8] Поскольку циклаза является ферредоксин-зависимым ферментом, это может обеспечить механизм координации между фотосинтезом и потребностью хлоропластов в хлорофилле, связывая биосинтез хлорофилла с цепью транспорта электронов фотосинтеза. В системах гидроксилирования бактериальной диоксигеназы они служат промежуточными переносчиками электронов между флавопротеинами редуктазы и оксигеназой.
Тиоредоксиноподобные ферредоксины
Fe2S2 ферредоксин из Clostridium pasteurianum (Cp2FeFd; P07324) был признан отдельным семейством белков на основе его аминокислотной последовательности, спектроскопических свойств его кластера железо-сера и уникальной способности двух цистеиновых лигандов к замене лигандов на [Fe2S2] кластер. Хотя физиологическая роль этого ферредоксина остается неясной, сильное и специфическое взаимодействие Cp2FeFd с молибден-железным белком нитрогеназа было обнаружено. Гомологические ферредоксины из Azotobacter vinelandii (Средний2FeFdI; P82802) и Aquifex aeolicus (АаFd; O66511) были охарактеризованы. Кристаллическая структура АаFd была решена. АаFd существует в виде димера. Структура АаМономер Fd отличается от других Fe2S2 ферредоксины. Складка принадлежит к классу α + β, при этом первые четыре β-тяжи и две α-спирали принимают вариант тиоредоксин складывать.[9] UniProt относит их к семейству «ферредоксинов 2Fe2S шетна-типа».[10]
Ферредоксины адренодоксинового типа
| ферредоксин 1 | |||||||
|---|---|---|---|---|---|---|---|
 Кристаллическая структура ферредоксина-1 человека (FDX1).[11] | |||||||
| Идентификаторы | |||||||
| Символ | FDX1 | ||||||
| Альт. символы | FDX | ||||||
| Ген NCBI | 2230 | ||||||
| HGNC | 3638 | ||||||
| OMIM | 103260 | ||||||
| RefSeq | NM_004109 | ||||||
| UniProt | P10109 | ||||||
| Прочие данные | |||||||
| Locus | Chr. 11 q22.3 | ||||||
| |||||||
Адренодоксин (ферредоксин надпочечников; ИнтерПро: IPR001055 ), путидаредоксин и терпредоксин составляют семейство растворимых Fe2S2 белки, которые действуют как переносчики одиночных электронов, в основном эукариотический митохондрии и Протеобактерии. Человеческий вариант адренодоксина упоминается как ферредоксин-1 и ферредоксин-2. В митохондриальных монооксигеназных системах адренодоксин переносит электрон от НАДФН: адренодоксинредуктаза к мембранно-связанным цитохром P450. У бактерий путидаредоксин и терпредоксин переносят электроны между соответствующими НАДН-зависимыми ферредоксинредуктазами и растворимыми P450.[12][13] Точные функции других членов этого семейства неизвестны, хотя кишечная палочка Показано, что Fdx участвует в биогенезе кластеров Fe – S.[14] Несмотря на низкое сходство последовательностей между ферредоксинами адренодоксинового типа и растительного типа, эти два класса имеют сходную топологию складывания.
Ферредоксин-1 в организме человека участвует в синтезе гормонов щитовидной железы. Он также переносит электроны от адренодоксинредуктазы к CYP11A1, фермент CYP450, ответственный за расщепление боковой цепи холестерина. FDX-1 обладает способностью связываться с металлами и белками.[15] Ферредоксин-2 участвует в синтезе гема А и железо-серного белка.[16]
Fe4S4 и Fe3S4 ферредоксины
[Fe4S4] ферредоксины можно разделить на низкопотенциальные (бактериального типа) и высокопотенциальные (HiPIP) ферредоксины.
Ферредоксины с низким и высоким потенциалом связаны следующей окислительно-восстановительной схемой:

Формальная степень окисления ионов железа может быть [2Fe3+, 2Fe2+] или [1Fe3+, 3Fe2+] в ферредоксинах с низким потенциалом. Степени окисления ионов железа в высокопотенциальных ферредоксинах могут быть [3Fe3+, 1Fe2+] или [2Fe3+, 2Fe2+].
Ферредоксины бактериального типа
| Связывающий домен 3Fe-4S | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
 Структурное представление Fe3S4 ферредоксин. | |||||||||||
| Идентификаторы | |||||||||||
| Символ | Fer4 | ||||||||||
| Pfam | PF00037 | ||||||||||
| ИнтерПро | IPR001450 | ||||||||||
| PROSITE | PDOC00176 | ||||||||||
| SCOP2 | 5fd1 / Объем / СУПФАМ | ||||||||||
| Белок OPM | 1ккф | ||||||||||
| |||||||||||
Группа Fe4S4 ферредоксины, первоначально обнаруженные в бактериях, получили название «бактериального типа». Ферредоксины бактериального типа, в свою очередь, можно подразделить на дополнительные группы на основе их свойств последовательности. Большинство из них содержат по крайней мере один консервативный домен, включая четыре остатка цистеина, которые связываются с [Fe4S4] кластер. В Pyrococcus furiosus Fe4S4 ферредоксин, один из консервативных остатков Cys замещен аспарагиновой кислотой.
Во время эволюции ферредоксинов бактериального типа происходили внутрипоследовательные события дупликации, транспозиции и слияния генов, что приводило к появлению белков с множественными центрами железо-сера. В некоторых бактериальных ферредоксинах один из дублированных доменов потерял один или несколько из четырех консервативных остатков Cys. Эти домены либо утратили способность связывать железо-серу, либо связываются с [Fe3S4] вместо кластера [Fe4S4] кластер[17] и дикластерного типа.[18]
Трехмерные структуры известны для ряда монокластерных и дикластерных ферредоксинов бактериального типа. Складка принадлежит к классу α + β, с 2-7 α-спиралями и четырьмя β-цепями, образующими бочкообразную структуру, и выдавленной петлей, содержащей три «проксимальных» лиганда Cys кластера железо-сера.
Белки железо-сера с высоким потенциалом
Белки с высоким потенциалом железо-сера (HiPIP) образуют уникальное семейство Fe4S4 ферредоксины, которые функционируют в анаэробных цепях переноса электронов. Некоторые HiPIP имеют окислительно-восстановительный потенциал выше, чем любой другой известный белок железо-сера (например, HiPIP от Rhodopila globiformis имеет окислительно-восстановительный потенциал ок. 450 мВ). Некоторые HiPIP до сих пор были охарактеризованы структурно, их складки принадлежат классу α + β. Как и в других бактериальных ферредоксинах, [Fe4S4] единица образует кластер кубанового типа и лигируется с белком через четыре остатка Cys.
Белки человека из семейства ферредоксинов
Эволюция ферредоксинов
Этот раздел пуст. Вы можете помочь добавляя к этому. (Июль 2020 г.) |
Рекомендации
- ^ Мортенсон Л. Е., Валентайн Р. К., Карнахан Дж. Э. (июнь 1962 г.). «Фактор переноса электронов из Clostridium pasteurianum». Сообщения о биохимических и биофизических исследованиях. 7 (6): 448–52. Дои:10.1016 / 0006-291X (62) 90333-9. PMID 14476372.
- ^ Валентина RC (декабрь 1964 г.). «Бактериальный ферредоксин». Бактериологические обзоры. 28 (4): 497–517. Дои:10.1128 / MMBR.28.4.497-517.1964. ЧВК 441251. PMID 14244728.
- ^ Тагава К., Арнон Д.И. (август 1962 г.). «Ферредоксины как переносчики электронов в фотосинтезе и в биологическом производстве и потреблении газообразного водорода». Природа. 195 (4841): 537–43. Bibcode:1962Натура.195..537Т. Дои:10.1038 / 195537a0. PMID 14039612. S2CID 4213017.
- ^ Арменгауд Дж, Сайнс Дж., Жуанно Й., Зикер Л.С. (февраль 2001 г.). «Кристаллизация и предварительный рентгеноструктурный анализ [2Fe-2S] ферредоксина (FdVI) из Rhodobacter capsulatus». Acta Crystallographica Раздел D. 57 (Чт 2): 301–3. Дои:10.1107 / S0907444900017832. PMID 11173487.
- ^ Севрюкова И.Ф. (апрель 2005 г.). «Редокс-зависимая структурная реорганизация в путидаредоксине, ферредоксине типа [2Fe-2S] позвоночных из Pseudomonas putida». Журнал молекулярной биологии. 347 (3): 607–21. Дои:10.1016 / j.jmb.2005.01.047. PMID 15755454.
- ^ Мо Х, Почапский С.С., Почапский ТЦ (апрель 1999 г.). «Модель для структуры раствора окисленного терпредоксина, ферредоксина Fe2S2 из Pseudomonas». Биохимия. 38 (17): 5666–75. CiteSeerX 10.1.1.34.4745. Дои:10.1021 / bi983063r. PMID 10220356.
- ^ Beilke D, Weiss R, Löhr F, Pristovsek P, Hannemann F, Bernhardt R, Rüterjans H (июнь 2002 г.). «Новый механизм переноса электронов в стероид-гидроксилазных системах митохондрий, основанный на структурных изменениях при восстановлении адренодоксина». Биохимия. 41 (25): 7969–78. Дои:10.1021 / bi0160361. PMID 12069587.
- ^ Стюарт, Дэвид; Сандстрём, Малин; Юссеф, Хельми М .; Захрабекова, Шахира; Дженсен, Пол Эрик; Болливар, Дэвид У .; Ханссон, Матс (сентябрь 2020 г.). "Аэробная циклаза монометилового эфира Mg-протопорфирина IX ячменя питается от ферредоксина электронами". Растения. 9 (9): 1157. Дои:10.3390 / растения9091157. PMID 32911631.
- ^ Yeh AP, Ambroggio XI, Andrade SL, Einsle O, Chatelet C, Meyer J, Rees DC (сентябрь 2002 г.). «Кристаллические структуры с высоким разрешением дикого типа и вариантов Cys-55 -> Ser и Cys-59 -> Ser тиоредоксин-подобного [2Fe-2S] ферредоксина из Aquifex aeolicus». Журнал биологической химии. 277 (37): 34499–507. Дои:10.1074 / jbc.M205096200. PMID 12089152.
- ^ семейство: "2fe2s семейство ферредоксинов шетна"
- ^ PDB: 3П1М; Чайкуад А, Йоханссон, Ц, Кройер, Т, Юэ, WW, Филлипс, Ц, Брей, Дж. Э., Пайк, ACW, Мунис, JRC, Фоллмар, М, Вайгельт, Дж, Эроусмит, СН, Эдвардс, AM, Баунтра, Ц , Кавана, К., Опперманн, У (2010). «Кристаллическая структура человеческого ферредоксина-1 (FDX1) в комплексе с железо-серным кластером». Будут опубликованы. Дои:10.2210 / pdb3p1m / pdb.
- ^ Петерсон Дж. А., Лоренс М. С., Амарне Б. (апрель 1990 г.). «Путидаредоксинредуктаза и путидаредоксин. Клонирование, определение последовательности и гетерологичная экспрессия белков». Журнал биологической химии. 265 (11): 6066–73. PMID 2180940.
- ^ Петерсон Дж. А., Лу Дж. Й., Гайссельсодер Дж., Грэм-Лоренс С., Кармона С., Уитни Ф., Лоренс М. С. (июль 1992 г.). «Цитохром P-450terp. Выделение и очистка белка, а также клонирование и секвенирование его оперона». Журнал биологической химии. 267 (20): 14193–203. PMID 1629218.
- ^ Токумото Ю., Такахаши Ю. (июль 2001 г.). «Генетический анализ оперона isc в Escherichia coli, участвующего в биогенезе клеточных железо-серных белков». Журнал биохимии. 130 (1): 63–71. Дои:10.1093 / oxfordjournals.jbchem.a002963. PMID 11432781.
- ^ «Энтрез Ген: ферредоксин 1 FDX1».
- ^ «Ферредоксин 2 FDX2 [Homo sapiens (человек)] - Ген - NCBI». www.ncbi.nlm.nih.gov. Получено 8 апреля 2019.
- ^ Фукуяма К., Мацубара Х., Цукихара Т., Кацубе Й. (ноябрь 1989 г.). "Структура [4Fe-4S] ферредоксина из Bacillus thermoproteolyticus уточнена с разрешением 2,3 A. Структурные сравнения бактериальных ферредоксинов". Журнал молекулярной биологии. 210 (2): 383–98. Дои:10.1016/0022-2836(89)90338-0. PMID 2600971.
- ^ Duée ED, Fanchon E, Vicat J, Sieker LC, Meyer J, Moulis JM (ноябрь 1994 г.). «Уточненная кристаллическая структура 2 [4Fe-4S] ферредоксина из Clostridium acidurici с разрешением 1,84 A». Журнал молекулярной биологии. 243 (4): 683–95. Дои:10.1016/0022-2836(94)90041-8. PMID 7966291.
дальнейшее чтение
- Бруски М, Герлескен Ф (1988). «Структура, функция и эволюция бактериальных ферредоксинов». Обзор микробиологии FEMS. 4 (2): 155–75. Дои:10.1111 / j.1574-6968.1988.tb02741.x. PMID 3078742.
- Чурли С, Мусиани Ф (2005). «Высокопотенциальные железо-серные белки и их роль в качестве растворимых переносчиков электронов в бактериальном фотосинтезе: рассказ об открытии». Фотосинтез Исследования. 85 (1): 115–31. Дои:10.1007 / s11120-004-6556-4. PMID 15977063. S2CID 27768048.
- Фукуяма К. (2004). «Структура и функции ферредоксинов растительного типа». Фотосинтез Исследования. 81 (3): 289–301. Дои:10.1023 / B: PRES.0000036882.19322.0a. PMID 16034533. S2CID 24574958.
- Гринберг А.В., Ханнеманн Ф., Шиффлер Б., Мюллер Дж., Хайнеманн Ю., Бернхардт Р. (сентябрь 2000 г.). «Адренодоксин: структура, стабильность и свойства электронного переноса». Белки. 40 (4): 590–612. Дои:10.1002 / 1097-0134 (20000901) 40: 4 <590 :: AID-PROT50> 3.0.CO; 2-P. PMID 10899784.
- Холден Х.М., Якобсон Б.Л., Херли Дж. К., Толлин Дж., О Б. Х., Скьелдал Л., Чэ Ю. К., Ченг Х., Ся Б., Маркли Дж. Л. (февраль 1994 г.). «Структурно-функциональные исследования [2Fe-2S] ферредоксинов». Журнал биоэнергетики и биомембран. 26 (1): 67–88. Дои:10.1007 / BF00763220. PMID 8027024. S2CID 12560221.
- Мейер Дж. (Ноябрь 2001 г.). «Ферредоксины третьего вида». Письма FEBS. 509 (1): 1–5. Дои:10.1016 / S0014-5793 (01) 03049-6. PMID 11734195. S2CID 8101608.
внешняя ссылка
- ИнтерПро: IPR006057 - Субдомен 2Fe – 2S ферредоксина
- ИнтерПро: IPR001055 - Адренодоксин
- ИнтерПро: IPR001450 - 4Fe – 4S ферредоксин, связывание железо-сера
- ИнтерПро: IPR000170 - Белок железо-сера с высоким потенциалом
- PDB: 1F37- Рентгеноструктура тиоредоксиноподобного ферредоксина из Aquifex aeolicus (АаFd)
