Ретиноид - Retinoid
В ретиноиды являются классом химические соединения которые витамеры из витамин А или химически связаны с ним. Ретиноиды нашли применение в медицине, где они регулируют клетка эпителия рост.
Ретиноиды выполняют множество важных функций во всем организме, включая роль в зрении,[1] регулирование пролиферации и дифференцировки клеток, роста костной ткани, иммунной функции и активации гены-супрессоры опухолей.
Также проводятся исследования их способности лечить рак кожи. В настоящее время, алитретиноин (9-СНГ-ретиноевую кислоту) можно использовать местно для лечения кожных повреждений Саркома Капоши, и третиноин (все-транс- ретиноевая кислота) применяется для лечения острый промиелоцитарный лейкоз.
Типы
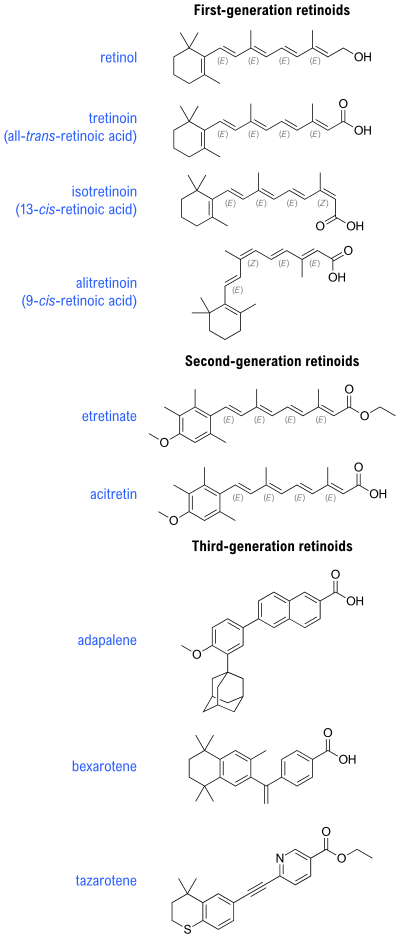
Есть три поколения ретиноидов:
- Первое поколение включает ретинол, сетчатка, третиноин (ретиноевая кислота ), изотретиноин, и алитретиноин
- Второе поколение включает этретинат и его метаболит ацитретин
- Третье поколение включает адапален, бексаротен, и тазаротен
- Четвертое поколение включает Трифаротен
Некоторые авторы считают ретиноиды производными от пираноны как четвертое поколение. Одним из таких соединений является селетиноид G.[2]
Структура
Основная структура гидрофобной молекулы ретиноида состоит из циклической концевой группы a полиен боковая цепь и полярная концевая группа. В сопряженная система образованные чередующимися двойными связями C = C в боковой цепи полиена, ответственны за цвет ретиноидов (обычно желтый, оранжевый или красный). Следовательно, многие ретиноиды хромофоры. Чередование боковых цепей и концевых групп создает различные классы ретиноидов.
Ретиноиды первого и второго поколения способны связываться с несколькими ретиноидные рецепторы благодаря гибкости, обеспечиваемой их чередующимися одинарными и двойными связями.
Ретиноиды третьего поколения менее гибкие, чем ретиноиды первого и второго поколения, и поэтому взаимодействуют с меньшим количеством рецепторов ретиноидов.
Ретиноид четвертого поколения, трифаротен, избирательно связывается с рецептором RAR-y. Он был одобрен для использования в США в 2019 году.[нужна цитата ]
Абсорбция
Основным источником ретиноидов в рационе являются растительные пигменты, такие как каротины и сложные эфиры ретинила, полученные из животных источников. Ретиниловые эфиры гидролизуются в просвете кишечника с образованием свободного ретинола и соответствующей жирной кислоты (например, пальмитата или стеарата). После гидролиза ретинол поглощается энтероцитами. Гидролиз ретинилового эфира требует присутствия солей желчных кислот, которые служат для солюбилизации ретиниловых эфиров в смешанных мицеллы и для активации гидролизующих ферментов [3]
Некоторые ферменты, присутствующие в просвете кишечника, могут участвовать в гидролизе пищевых эфиров ретинила. Холестеринэстераза секретируется в просвет кишечника из поджелудочной железы и, как было показано in vitro, проявляет активность гидролазы ретинилового эфира. Кроме того, гидролаза ретинилового эфира, которая присуща мембране щеточной каймы тонкого кишечника, была охарактеризована как у крысы, так и у человека. Различные гидролизующие ферменты активируются разными типами солей желчных кислот и обладают различными субстратными специфичностями. Например, в то время как эстераза поджелудочной железы является селективной в отношении эфиров ретинила с короткой цепью, фермент мембраны щеточной каймы предпочтительно гидролизует эфиры ретинила, содержащие длинноцепочечные жирные кислоты, такие как пальмитат или стеарат. Ретинол проникает в абсорбирующие клетки тонкой кишки, предпочтительно в форме полностью транс-ретинола.
Использует
Ретиноиды используются при лечении множества разнообразных заболеваний и эффективны при лечении ряда дерматологических состояний, таких как воспалительные заболевания кожи,[нужна цитата ] рак кожи,[нужна цитата ] нарушения увеличения клеточного обмена (например, псориаз),[4] фотостарение,[5] и морщины на коже.[6]
Общие кожные заболевания, которые лечат ретиноидами, включают: угревая сыпь и псориаз.[7]
Изотретиноин не только считается единственно возможным лекарством от прыщей у некоторых пациентов, но и изначально представлял собой химиотерапевтическое лечение некоторых видов рака, таких как лейкемия.
Эмбриональные стволовые клетки человека также легче дифференцируются в корковые стволовые клетки в присутствии ретиноидов.[8]
Известно, что ретиноиды снижают риск рака головы и шеи.[9][10]
Синтез
Ретиноиды можно синтезировать разными способами. Обычной процедурой для снижения токсичности ретиноидов и улучшения активности ретиноидов является глюкуронизация. Walker et al. предложили новый синтез для осуществления глюкуронизации.[11]
Токсичность
Токсические эффекты возникают при длительном приеме в больших количествах. Специфическая токсичность зависит от времени воздействия и концентрации воздействия. А медицинский знак хронического отравления - наличие болезненных болезненных опухолей на длинных костях. Анорексия, поражения кожи, потеря волос, гепатоспленомегалия, папиллоэдема, кровотечение, Общее недомогание, псевдоопухоль головного мозга, и смерть также может произойти.[требуется медицинская цитата ]
Хроническая передозировка также вызывает повышенную лабильность биологических мембран и внешнего слоя кожи к отслаиванию.[12]
Недавнее исследование[нужна цитата ] предположил роль ретиноидов в кожных побочных эффектах различных препаратов, включая противомалярийный препарат прогуанил. Предлагается, чтобы такие препараты, как прогуанил действовать, чтобы разрушить ретиноид гомеостаз.
Системные ретиноиды (изотретиноин, этретинат) противопоказаны во время беременности, так как они могут вызывать дефекты ЦНС, черепно-лицевые, сердечно-сосудистые и другие дефекты.
Смотрите также
Рекомендации
- ^ Кисер, Филип Д .; Гольчак, Марцин; Пальчевский, Кшиштоф (11 июля 2013 г.). «Химия ретиноидного (зрительного) цикла». Химические обзоры. 114 (1): 194–232. Дои:10.1021 / cr400107q. ЧВК 3858459. PMID 23905688.

- ^ Мукерджи, S; Дата, А; Патравале, V; Кортинг, ХК; Рёдер, А; Weindl, G (2006). «Ретиноиды в лечении старения кожи: обзор клинической эффективности и безопасности». Клинические вмешательства при старении. 1 (4): 327–48. Дои:10.2147 / ciia.2006.1.4.327. ЧВК 2699641. PMID 18046911.
- ^ Ной, Н. (2006) «Витамин А», «Биохимические, физиологические и молекулярные аспекты питания человека», М. Х. Стипанук, 2-е изд.
- ^ «Псориаз - Диагностика и лечение - Клиника Мэйо». www.mayoclinic.org. В архиве из оригинала 7 мая 2017 г.. Получено 16 марта 2018.
- ^ Стефанаки С., Стратигос А., Кацамбас А. (июнь 2005 г.). «Актуальные ретиноиды в лечении фотостарения». J Cosmet Dermatol. 4 (2): 130–4. Дои:10.1111 / j.1473-2165.2005.40215.x. PMID 17166212.
- ^ Кафи, Р.; Квак, HS; Шумахер, МЫ; Чо, S; Hanft, VN; Гамильтон, TA; Король, AL; Neal, JD; Варани, Дж; Фишер, ГДж; Вурхиз, Джей Джей; Канг, S (2007). «Улучшение естественно состарившейся кожи витамином А (ретинолом)». Арка Дерматол. 143 (5): 606–12. Дои:10.1001 / archderm.143.5.606. PMID 17515510.
- ^ «Национальный фонд псориаза». psoriasis.org. Архивировано из оригинал 13 июня 2010 г.. Получено 16 марта 2018.
- ^ http://www.nature.com/neuro/journal/vaop/ncurrent/fig_tab/nn.3041_F1.html В архиве 5 ноября 2014 г. Wayback Machine
- ^ Смит, Вт; Саба, Н. (2005). «Ретиноиды как химиопрофилактика рака головы и шеи: куда мы идем отсюда?». Критические обзоры в онкологии / гематологии. 55 (2): 143–52. Дои:10.1016 / j.critrevonc.2005.02.003. PMID 15886010.
- ^ Вопросы и ответы в стиле Совета по внутренней медицине 2009 г. В архиве 2012-09-19 в Wayback Machine, Q: 378, p.232; А: 378, стр.125
- ^ Уокер, младший; Альшафи, G; Абу-Исса, H; Керли, Р.В. (12 сентября 2002 г.). "Улучшенный синтез C-связанного глюкуронида N- (4-Гидроксифенил) ретинамид ». Письма по биоорганической и медицинской химии. 12 (17): 2447–50. Дои:10.1016 / s0960-894x (02) 00427-4. PMID 12161154.
- ^ «Актуальные ретиноиды - DermNet New Zealand». dermnetnz.org. В архиве из оригинала 29 июля 2016 г.. Получено 16 марта 2018.
- Фармакологическая основа терапии, 10-е издание, Goodman & Gilman.
- Клиническая фармакология, П. Беннет и М.Дж. Браун.
внешняя ссылка
- Ретиноиды в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
