Парекоксиб - Википедия - Parecoxib
 | |
| Клинические данные | |
|---|---|
| AHFS /Drugs.com | Международные названия лекарств |
| Данные лицензии | |
| Беременность категория |
|
| Маршруты администрация | Внутривенно и внутримышечный |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетический данные | |
| Биодоступность | 100% |
| Связывание с белками | 98% |
| Метаболизм | Печеночный к валдекоксиб и пропионовая кислота CYP широко вовлечены (в основном CYP3A4 и 2C9 ) |
| Устранение период полураспада | 22 минуты (парекоксиб) 8 часов (вальдекоксиб) |
| Экскреция | Почечный (70%, метаболиты) |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.230.078 |
| Химические и физические данные | |
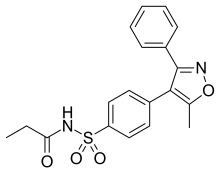
| Формула | C19ЧАС18N2О4S |
| Молярная масса | 370.42 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| | |
Парекоксиб, продается под торговой маркой Династат среди прочего, является водорастворимым и инъекционный пролекарство из валдекоксиб. Парекоксиб - это Селективный ингибитор ЦОГ2. Это инъекционный. Он одобрен во многих странах Европы для краткосрочного периоперационного обезболивания.
Он был запатентован в 1996 году и разрешен для медицинского применения в 2002 году.[1]
Одобрение
В 2005 г. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) выпустило письмо об отказе в одобрении парекоксиба в США. Причины отказа никогда не были публично задокументированы, хотя в одном исследовании отмечалось увеличение числа случаев сердечные приступы следующий операция по шунтированию сердца по сравнению с плацебо, когда для купирования боли после операции использовались высокие дозы парекоксиба. Также важно помнить, что редкие, но серьезные аллергические реакции (Синдром Стивенса-Джонсона, Синдром Лайелла ) были описаны с валдекоксиб, то молекула в который преобразуется парекоксиб.[2] Препарат не разрешен к применению после кардиохирургических операций в Европе.
Все противовоспалительные препараты в США имеют одинаковое предупреждение относительно кожных реакций, и ни один из них не одобрен для использования во время операции АКШ, поэтому причина отказа FDA в одобрении парекоксиба остается неизвестной, но, вероятно, была связана с политическим давлением со стороны США. Конгресс не одобряет другого Селективный ингибитор ЦОГ-2 вслед за Vioxx Роман. С тех пор ни один селективный ингибитор ЦОГ-2 не был одобрен в США, независимо от профиля безопасности парекоксиба в Европе. Попытки выяснить научное обоснование или, что более вероятно, его отсутствие, которое FDA использовало для оправдания отказа в одобрении парекоксиба в США, оказались тщетными из-за проблем секретности.[3][4]
Политическая мотивация не одобрять парекоксиб была дополнительно подтверждена объединенным анализом данных о безопасности в 28 опубликованных исследованиях, который показал, что после 69 567 300 единиц парекоксиба кожная сыпь и сердечные осложнения были минимальными, если вообще были, по сравнению с плацебо.[5]
Парекоксиб, наряду с другими селективными ингибиторами ЦОГ-2, целекоксиб, валдекоксиб, и мавакоксиб, были обнаружены командой в Searle отдел Monsanto во главе с Джон Тэлли.[6][7]
Парекоксиб - первый парентеральный селективный ингибитор ЦОГ-2, доступный для клинического применения при обезболивании. Из предыдущих клинических испытаний хорошо известно, что его пиковые концентрации в сыворотке наблюдаются примерно через 30 минут после внутривенного (IV) введения и через 1 час после внутримышечной (IM) инъекции. Его первый ощутимый обезболивающий эффект наступает в течение 7-13 минут, с клинически значимой анальгезией, демонстрируемой в течение 23-39 минут, и максимальным эффектом в течение 2 часов после введения однократных доз 40 мг внутривенно или внутримышечно.[8]
Смотрите также
Рекомендации
- ^ Фишер Дж, Ганеллин ЧР (2006). Открытие лекарств на основе аналогов. Джон Вили и сыновья. п. 522. ISBN 9783527607495.
- ^ Здоровье «Ассоциация Bextra (Valdecoxib) с серьезными побочными реакциями на лекарства». Министерство здравоохранения Канады. 21 апреля 2005 г.
- ^ Гаджрадж Н.М. (2007). «Ингибиторы ЦОГ-2 целекоксиб и парекоксиб: ценные варианты лечения послеоперационной боли». Актуальные темы медицинской химии. 7 (3): 235–49. Дои:10.2174/156802607779941323. PMID 17305567.
- ^ Kiehl S (13 марта 2005 г.). "Секретность на подъеме". Балтимор Сан.
- ^ Шуг С.А., Парсонс Б., Ли К., Ся Ф. (2017). «Профиль безопасности парекоксиба для лечения послеоперационной боли: объединенный анализ 28 рандомизированных двойных слепых плацебо-контролируемых клинических испытаний и обзор данных, полученных за более чем 10 лет после авторизации». Журнал исследований боли. 10: 2451–2459. Дои:10.2147 / jpr.s136052. ЧВК 5644539. PMID 29066931.
- ^ Лангрет Р. (23 июня 2003 г.). "Химический сапожник". Forbes.
- ^ "Доктор Джон Талли: лауреат Сент-Луиса 2001 г." (PDF). Химическая связь. Секция Сент-Луиса, Американское химическое общество. 52 (5): 2 мая 2001 г. Архивировано с оригинал (PDF) 15 апреля 2018 г.
- ^ Mulita, Francesk; Карпетас, Георгиос; Лиолис, Элиас; Вайлас, Михаил; Чабашвили, Леван; Марулис, Иоаннис (2021 г.). «Сравнение анальгетической эффективности монотерапии ацетаминофеном и комбинаций парацетамола с петидином или парекоксибом у пациентов, перенесших лапароскопическую холецистэктомию: рандомизированное проспективное исследование». Medicinski Glasnik Ljekarske komore Zenicko-dobojskog kantona (1). Дои:10.17392/1245-21. ISSN 1840-0132.
дальнейшее чтение
- Вилласис-Кивер, Массачусетс, Рендон-Масиас, ME, Эскамилья-Нуньес, А (2009). «[Систематический обзор для оценки эффективности и безопасности парекоксиба]». Acta Ortopedica Mexicana (на испанском). 23 (6): 342–50. PMID 20377000.
- Ллойд Р., Дерри С., Мур Р.А., МакКуэй Х.Дж. (апрель 2009 г.). «Парекоксиб для внутривенного или внутримышечного введения при острой послеоперационной боли у взрослых». Кокрановская база данных систематических обзоров (2): CD004771. Дои:10.1002 / 14651858.CD004771.pub4. ЧВК 6540719. PMID 19370610.
