Открытие и разработка ингибиторов циклооксигеназы 2 - Discovery and development of cyclooxygenase 2 inhibitors
Циклооксигеназы представляют собой ферменты, которые участвуют в сложном биосинтетическом каскаде, который приводит к превращению полиненасыщенные жирные кислоты к простагландины и тромбоксан (s).[1]Их основная роль - катализировать трансформацию арахидоновая кислота в промежуточный простагландин H2, который является поставщиком множества простаноиды с разнообразным и мощным биологическим действием.[2]Циклооксигеназы имеют две основные изоформы, которые называются СОХ-1 и СОХ-2 (также как и СОХ-3 ). ЦОГ-1 отвечает за синтез простагландина и тромбоксана во многих типах клеток, включая желудочно-кишечный тракт и тромбоциты крови. ЦОГ-2 играет важную роль в биосинтезе простагландинов в воспалительных клетках и в центральной нервной системе. Простагландин синтез в этих участках является ключевым фактором в развитии воспаления и гипералгезия.[3]Ингибиторы ЦОГ-2 обладают анальгетической и противовоспалительной активностью, избирательно блокируя превращение арахидоновой кислоты в простагландин Н2.[4]
Рост разработки селективных ингибиторов ЦОГ-2
 |
| ДуП-697 |
Толчком к разработке селективных ингибиторов ЦОГ-2 послужили побочные эффекты со стороны желудочно-кишечного тракта. НПВП. Вскоре после открытия механизма действия НПВП появились убедительные показания для альтернативных форм ЦОГ, но было найдено мало подтверждающих доказательств. Фермент ЦОГ оказалось трудно очистить, и его последовательность не проводилась до 1988 года.[5] В 1991 году существование фермента ЦОГ-2 было подтверждено клонированием доктором Дж. Дэн Симмонс в Университет Бригама Янга. До подтверждения существования ЦОГ-2 компания Dupont разработала соединение, ДуП-697, который был эффективен во многих противовоспалительных тестах, но не имел ульцерогенных эффектов НПВП. Как только фермент ЦОГ-2 был идентифицирован, Dup-697 стал строительным блоком для синтеза ингибиторов ЦОГ-2. Целекоксиб и рофекоксиб, первые ингибиторы ЦОГ-2, появившиеся на рынке, были основаны на DuP-697.[5][6] На разработку и продвижение на рынок первого ингибитора ЦОГ-2, Целебрекса (целекоксиб ) выпущен в декабре 1998 года, а Vioxx (рофекоксиб ) запущен в мае 1999 года.[7][8] Целекоксиб и другие селективные ингибиторы ЦОГ-2, валдекоксиб, парекоксиб, и мавакоксиб, были обнаружены командой в Searle отдел Monsanto во главе с Джон Тэлли.[9][10]
Разработка ингибиторов ЦОГ-2
Ранние исследования показали, что при индуцировании воспаления пораженный орган неожиданно развивает огромную способность вырабатывать простагландины. Было продемонстрировано, что это увеличение связано с синтезом свежего фермента de novo. В 1991 г. при исследовании экспрессии генов раннего ответа у фибробласты трансформированный вирусом саркомы Рауса, был идентифицирован новый транскрипт мРНК, который был подобен, но не идентичен семенному ферменту ЦОГ. Было высказано предположение, что был открыт изофермент ЦОГ. Другая группа обнаружила новый вид кДНК, кодирующий белок со структурой, аналогичной СОХ-1, при изучении генов, индуцированных сложным эфиром форбола, в клетках Swiss 3T3. Та же лаборатория показала, что этот ген действительно экспрессирует новый фермент ЦОГ. Два фермента были переименованы в СОХ-1, что означает исходный фермент и СОХ-2.[5]Основываясь на этих результатах, ученые сосредоточили внимание на селективном COX-2. ингибиторы. Огромные усилия были потрачены на разработку НПВП между 1960-ми и 1980-ми годами, поэтому было множество фармакофоров для тестирования, когда был открыт ЦОГ-2. Первые усилия были сосредоточены на модификации двух соединений свинца, DuP-697 и НС-398. Эти соединения сильно отличаются от НПВП, являющихся аналогами арилалконовых кислот. Ободренный "концептуальное тестирование "эксперименты с селективными ингибиторами, вооруженные несколькими надежными выводами и четким представлением о природе сайт привязки, развитие этого направления было стремительным.[3] Тесты рекомбинантных ферментов in vitro предоставили мощные средства для оценки селективности ЦОГ и потенция и привел к открытию и клинической разработке первого рационально разработанного селективного ингибитора ЦОГ-2, целекоксиба. Были предприняты попытки превратить НПВП в селективные ингибиторы ЦОГ-2, такие как индометацин за счет удлинения боковой цепи алкилкарбоновой кислоты, но в продажу они не поступали.[1]
Взаимосвязь структуры и деятельности (SAR)
DuP-697 был строительным блоком для синтеза ингибиторов ЦОГ-2 и служил базовой химической моделью для коксибов, которые являются единственными селективными ингибиторами ЦОГ-2 на рынке сегодня. DuP-697 представляет собой диарильный гетероцикл с цис-стильбен часть. Исследования зависимости структурной активности (SAR) для диарилгетероциклических соединений показали, что цис-стильбеновая составляющая и изменения пара-положения одного из арильных колец играют важную роль в селективности COX-2.[1][11] Целекоксиб и парекоксиб имеют сульфонамидный заместитель (SO2NH2) в пара-положении на одном из арильных колец, в то время как эторикоксиб и рофекоксиб имеют метилсульфон (SO2CH3).[12] Степень окисления серы важна для селективности; сульфоны и сульфонамиды являются селективными для COX-2, но сульфоксиды и сульфиды не. Кольцевая система, которая слита в этой стильбеновой системе, подверглась обширным манипуляциям, чтобы включить в нее любой вообразимый гетероциклический и карбоциклический скелет с различными размерами кольца. Известно, что SO2NHCOCH3 часть, как в парекоксибе, который является пролекарством валдекоксиба, составляет 105 – 106 более активный ацетилирующий агент гидроксильных групп фермента серина, чем простые амиды.[11] В связи с тем, что различные кинетические механизмы влияют на эффективность ЦОГ-1 по сравнению с ЦОГ-2, многие группы используют достоверную эффективность и селективность в цельной крови человека, и это было принято в качестве стандартной оценки активности и селективности ЦОГ-2.
Взаимосвязь между аминокислотным профилем фермента ЦОГ-2 и механизмом ингибирования
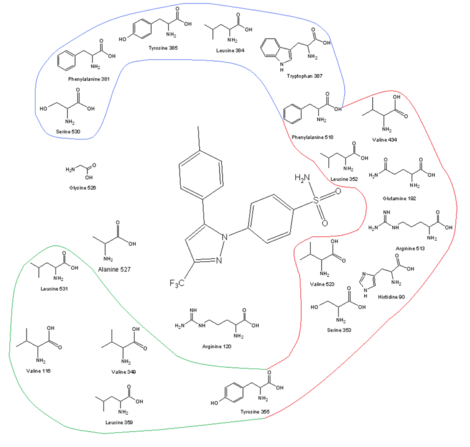 |
| Сайт рецептора ЦОГ-2 и его аминокислотный профиль вместе с целекоксибом в сайте связывания |
Одним из ключей к разработке селективных препаратов на ЦОГ-2 является более крупный активный сайт ЦОГ-2, что позволяет делать молекулы слишком большими, чтобы соответствовать активному центру ЦОГ-1, но все же способными соответствовать ЦОГ-2. Более крупный активный центр COX-2 частично обусловлен полярным гидрофильный боковой карман, который образуется из-за замены Иль 523, Его 513 и Ile434 в COX-1 Вал 523, Arg 513 и Val434 в СОХ-2. Val523 менее громоздок, чем Ile523, что увеличивает объем активного сайта. Замена Ile434 на Val434 позволяет боковой цепи Phe 518, чтобы отойти назад и освободить дополнительное место. Этот боковой карман позволяет взаимодействовать с Arg513, который является заменой His513 из COX-1. Считается, что Arg513 является ключевым остатком для ингибиторов диарилгетероциклов, таких как коксибы. Боковая цепь Лея 384, наверху рецепторного канала, ориентирован в активный сайт СОХ-1, но в СОХ-2 он ориентирован от активного сайта и оставляет больше места на вершине сайта связывания.[13][14]Громоздкий сульфонамид группа в ингибиторах ЦОГ-2, таких как целекоксиб и рофекоксиб предотвращают попадание молекулы в канал ЦОГ-1. Для оптимальной активности и селективности коксибов требуется 4-метилсульфонилфенил, присоединенный к ненасыщенному (обычно) пятичленному кольцу с вицинальной липофильной группой (рофекоксиб). SO2CH3 можно заменить на SO2NH2, где липофильный карман занят необязательно замещенным фенильным кольцом или объемным алкоксизаместителем (целекоксиб). В рамках гидрофильный боковой карман ЦОГ-2, кислород сульфонамида (или сульфон ) группа взаимодействует с Hist90, Arg513 и Gln 192 и формы водородные связи. Замещенный фенильная группа в верхней части канала взаимодействует с боковыми цепями аминокислотных остатков посредством гидрофобных и электростатических взаимодействий. Тюр 385 марок для некоторых стерический ограничения этой стороны сайта связывания, поэтому небольшой заместитель фенильной группы способствует лучшему связыванию. Степень свободы также важна для связывания. Центральное кольцо коксибов определяет ориентацию ароматические кольца и, следовательно, связывание с ферментом ЦОГ, даже если он часто не имеет электростатических взаимодействий ни с одним из аминокислотных остатков. Высота липофильность активного сайта требует низкого полярность центрального каркаса коксибов.[14][15]
Механизм привязки
Исследования механизма связывания селективных ингибиторов ЦОГ-2 показывают, что у них есть две обратимые стадии как с ЦОГ-1, так и с ЦОГ-2, но селективность по ЦОГ-2 обусловлена другим этапом, который является медленным и необратимым и наблюдается только в ингибирование ЦОГ-2, а не ЦОГ-1. Необратимый шаг объясняется наличием сульфонамид (или же сульфон ), который помещается в боковой карман COX-2. Это было изучено с использованием SC-58125 (аналог целекоксиба) и мутированного СОХ-2, в котором остаток валина 523 был заменен на изолейцин 523. Необратимого ингибирования не произошло, но было замечено обратимое ингибирование. Модель была создана для объяснения этого трехступенчатого механизма подавляющего действия селективных ингибиторов ЦОГ-2. На первом этапе учитывается контакт ингибитора с затвором гидрофобный канал (так называемый вестибюль). Второй шаг может объяснить перемещение ингибитора из области вестибюля в активный центр фермента ЦОГ. Последний этап, вероятно, представляет собой изменение положения ингибитора в активном центре, что приводит к сильным взаимодействиям фенилсульфонамидной или фенилсульфоновой группы ингибитора и аминокислот бокового кармана.[16] Это прямое торможение посадки.
Фармакокинетика коксибов
Коксибы широко распространены по организму. Все коксибы достигают достаточной концентрации в мозге, чтобы иметь центральную обезболивающее эффект, и все это снижает образование простагландинов в воспаленных суставах. Все они хорошо всасываются, но пиковая концентрация коксибов может различаться. Коксибы сильно связываются с белками, и опубликованная оценка период полураспада является переменной между коксибами.[17]
Целекоксиб
Целекоксиб был первым специфическим ингибитором ЦОГ-2, одобренным для лечения пациентов с ревматизм и остеоартроз. Исследование показало, что скорость абсорбции при пероральном приеме умеренная, а максимальная концентрация в плазме крови наступает примерно через 2–4 часа. Однако степень поглощение малоизвестно. Целекоксиб имеет близость широко связываться с белками плазмы, особенно с плазмой альбумин. Имеет кажущийся объем распределения (VD) 455 +/- 166 л у человека и площадь под кривой зависимости концентрации в плазме от времени (AUC ) увеличивается пропорционально увеличению пероральных доз, от 100 до 800 мг. Целекоксиб - это метаболизируется в первую очередь за счет изофермента CYP2C9 в карбоновую кислоту, а также за счет не-зависимой от CYP глюкуронизации до глюкуронид метаболиты. Метаболиты выводятся с мочой и калом, небольшая часть неизмененного препарата (2%) - с мочой. Его период полувыведения составляет около 11 часов (6–12 часов) у здоровых людей, но расовые различия в распределении лекарств и фармакокинетический не сообщалось об изменениях в пожилом возрасте. Люди с хроническая болезнь почек По-видимому, концентрация в плазме крови на 43% ниже, чем у здоровых людей, с увеличением очевидного клиренса на 47%, и можно ожидать, что у пациентов с нарушением функции печени от легкой до умеренной степени AUC в равновесном состоянии будет увеличиваться.[18]
| Целекоксиб | ||
|---|---|---|
| Пик [наркотик] | 2–4 часа |  |
| Связывание с белками | 97% | |
| Метаболиты | Конъюгаты карбоновой кислоты и глюкуронида | |
| Период полураспада [т1/2] | 6–12 часов | |
Парекоксиб и вальдекоксиб
Парекоксиб натрий представляет собой водорастворимый неактивный амид сложного эфира пролекарство из валдекоксиб, новый ингибитор ЦОГ-2 второго поколения и первый такой агент, который будет разработан для инъекций. Он быстро преобразуется печеночными ферментными гидролиз к активной форме валдекоксиб. Затем соединение претерпевает другое превращение, которое включает как путь, опосредованный цитохромом P450 (CYP2C9, CYP3A4), так и путь, не опосредованный цитохромом P450, в гидроксилированный метаболит и метаболит глюкуронида. Гидроксилированный метаболит, который также обладает слабыми ингибирующими свойствами, специфичными для ЦОГ-2, далее метаболизируется нецитохромным путем P450 до метаболита глюкуронида. Эти метаболиты выводятся с мочой.[17]После внутримышечного введения Парекоксиба концентрация натрия в плазме достигается в течение 15 минут. Концентрация в плазме быстро снижается после приема из-за довольно короткого периода полувыведения из сыворотки, который составляет около 15–52 минут. Это можно объяснить быстрым образованием вальдекоксиба. В отличие от быстрого клиренса Парекоксиба, концентрация вальдекоксиба в плазме медленно снижается из-за более длительного периода полувыведения.[19] С другой стороны, когда вальдекоксиб принимают перорально, он быстро всасывается (1-2 часа), но присутствие пищи может задерживать пиковую концентрацию в сыворотке крови. Затем он подвергается тому же метаболизму, который описан выше. Он сильно связан с белками (98%), а период полувыведения из плазмы составляет около 7–8 часов. Обратите внимание, что период полувыведения может быть значительно увеличен у пожилых людей или людей с печеночной недостаточностью и может привести к накоплению лекарственного средства.[17]Максимальная средняя концентрация гидроксильного метаболита в плазме достигается в течение 3-4 часов после приема, но она значительно ниже, чем у вальдекоксиба, или примерно 1/10 от уровня вальдекоксиба в плазме.[19]
| Парекоксиб | ||
|---|---|---|
| Пик [наркотик] | В течение 15 минут |  |
| Связывание с белками | Нет данных | |
| Метаболиты | Вальдекоксиб, после ферментативного гидролиза печени | |
| Период полураспада [т1/2] | 15–52 минут | |
| Валдекоксиб | ||
|---|---|---|
| Пик [наркотик] | 2–4 часа, задержка из-за еды |  |
| Связывание с белками | 98% | |
| Метаболиты | Гидроксильные производные и метаболит глюкуронида | |
| Период полураспада [т1/2] | 7–8 часов | |
Эторикоксиб
Эторикоксиб, который используется для пациентов с хроническим артропатии и скелетно-мышечная и зубная боль, умеренно абсорбируется при пероральном применении. Исследование его фармакокинетики показало, что пиковая концентрация эторикоксиба в плазме достигается примерно через 1 час. Было показано, что он широко связан с альбумином плазмы (около 90%) и имеет видимый объем распределения (VD) 120 л у человека. Площадь под кривой зависимости концентрации в плазме от времени (AUC) увеличивается пропорционально увеличению дозировки (5–120 мг). Период полувыведения составляет около 20 часов у здоровых людей, и такой длительный период полувыведения позволяет выбрать дозировку один раз в день. Эторикоксиб, как и другие коксибы, выводится с мочой и калом, а также метаболизируется аналогичным образом. CYP3A4 в основном отвечает за биотрансформацию эторикоксиба в метаболит карбоновой кислоты, но не CYP450 Путь метаболизма до метаболита глюкуронида также находится под рукой. Очень небольшая часть эторикоксиба (<1%) выводится в неизмененном виде с мочой. Пациенты с хроническая болезнь почек кривая концентрации в плазме (AUC) не отличается от кривой у здоровых людей. Однако сообщалось, что у пациентов с умеренной печеночной недостаточностью кривая концентрации в плазме (AUC) увеличилась примерно на 40%. Было заявлено, что необходимы дальнейшие исследования, чтобы точно описать релевантность фармакокинетических свойств с точки зрения клинических преимуществ и рисков эторикоксиба по сравнению с другими клиническими вариантами.[20][21]
| Эторикоксиб | ||
|---|---|---|
| Пик [наркотик] | 1 час |  |
| Связывание с белками | 90% | |
| Метаболиты | Метаболит карбоновой кислоты и метаболит глюкуронида | |
| Период полураспада [т1/2] | 20 часов | |
Люмиракоксиб
Люмиракоксиб среди коксибов уникален тем, что является слабой кислотой. Он был разработан для лечения остеоартрита, ревматоидного артрита и острой боли. Кислая природа люмиракоксиба позволяет ему хорошо проникать в очаги воспаления. Было показано, что он быстро и хорошо всасывается, при этом максимальная концентрация в плазме достигается примерно через 1-3 часа.[17] Исследование показало, что когда субъекту вводили дозу 400 мг, количество неизмененного лекарственного средства в плазме через 2,5 часа после введения дозы предполагает умеренное эффект первого прохода. Конечный период полувыведения в плазме колеблется от 5,4 до 8,6 часов (среднее значение = 6,5 часов). Период полувыведения в синовиальной жидкости значительно больше, чем в плазме, и концентрация в синовиальная жидкость Ожидается, что через 24 часа после введения произойдет значительное ингибирование ЦОГ-2. Этот факт может объяснить, почему некоторым пользователям может хватить дозы один раз в день, несмотря на короткий период полувыведения из плазмы. Основными метаболитами плазмы являются производные 5-карбокси, 4’-гидрокси и 4’-гидрокси-5-карбокси. Люмиракоксиб интенсивно метаболизируется до того, как вывести из организма, и пути выведения - с мочой или калом. Пиковые концентрации в плазме превышают те, которые необходимы для максимального ингибирования ЦОГ-2, и это соответствует более длительному фармакодинамический период полураспада. Люмиракоксиб in vitro продемонстрировал более высокую избирательность к ЦОГ-2, чем любой из других коксибов.[22]
| Люмиракоксиб | ||
|---|---|---|
| Пик [наркотик] | 1–3 часа |  |
| Связывание с белками | 90% | |
| Метаболиты | 5-карбокси, 4’-гидрокси и 4’-гидрокси-5-карбоксипроизводные | |
| Период полураспада [т1/2] | 6,5 часов | |
Рофекоксиб
Рофекоксиб был вторым селективным ингибитором ЦОГ-2, который поступил на рынок, и первым, который был снят с рынка.[8] Когда фармакокинетика изучалась на здоровых людях, пиковая концентрация была достигнута через 9 часов с эффективным периодом полувыведения примерно 17 часов. Наблюдается вторичный пик, который может свидетельствовать о том, что абсорбция рофекоксиба зависит от перистальтики кишечника, что приводит к высокой вариабельности во времени до достижения максимальной концентрации. Семьдесят один с половиной% дозы было выделено с мочой (менее 1% неметаболизировано) и 14,2% - с калом (примерно 1,8% с желчью). Среди метаболитов были рофекоксиб-3 ', 4'-дигидродиол, 4'-гидроксирофекоксиб-O-β-D-глюкуронид, 5-гидроксирофекоксиб-O-β-D-глюкуронид, 5-гидроксирофекоксиб, рофекоксиб-эритро-3,4. -дигидрогидроксикислота, рофекоксиб-трео-3,4-дигидрогидроксикислота, цис-3,4-дигидророфекоксиб и транс-3,4-дигидророфекоксиб.[23]
| Рофекоксиб | ||
|---|---|---|
| Пик [наркотик] | 9 часов |  |
| Связывание с белками | Нет данных | |
| Метаболиты | Основные: рофекоксиб-трео-3,4-дигидроксикислота и рофекоксиб-эритро-3,4-дигидрогидроксикислота | |
| Период полураспада [т1/2] | 17 часов | |
Сердечно-сосудистые события, связанные с селективными ингибиторами ЦОГ-2
Еще до появления на рынке первого селективного ингибитора ЦОГ-2 специалисты начали подозревать, что с этим классом лекарств может быть связан сердечно-сосудистый риск. В исследовании VIGOR (Vioxx Gastrointestinal Outcomes Research) рофекоксиб (Vioxx ) сравнивали с напроксен. Через короткое время стало очевидно, что риск заражения увеличивается в пять раз. инфаркт миокарда в группе рофекоксиба по сравнению с группой, получавшей напроксен. Авторы предположили, что разница была связана с кардиозащитным действием напроксена.[24] Исследование APPROVe (Adenomatous Poly Prevention on Vioxx) представляло собой многоцентровое рандомизированное плацебо-контролируемое двойное слепое исследование, направленное на оценку влияния трехлетнего лечения рофекоксибом на рецидив опухолевых полипов у лиц с колоректальными аденомами в анамнезе.[25][26] В 2000 и 2001 годах было набрано и под наблюдением 2587 пациентов с колоректальными аденомами в анамнезе. Исследование было остановлено досрочно (за 2 месяца до предполагаемого завершения) по рекомендациям совета по безопасности данных и мониторингу из-за опасений по поводу сердечно-сосудистой токсичности.[25] При рассмотрении результатов исследования было выявлено статистически значимое увеличение сердечно-сосудистого риска при приеме рофекоксиба по сравнению с плацебо.[25][26] начало после 18 месяцев лечения.[25][26][27] Затем 30 сентября Merck выпустила пресс-релиз, в котором объявила о своем добровольном прекращении использования Vioxx во всем мире.[27]Некоторые исследования других коксибов также показали увеличение риска сердечно-сосудистых событий, а другие - нет. Например, исследование «Профилактика аденомы с помощью целекоксиба» (APC) показало дозозависимое увеличение риска смерти от сердечно-сосудистых заболеваний, инфаркта миокарда, инсульта или сердечной недостаточности при приеме целекоксиба по сравнению с плацебо; и последовательное исследование эффективности и безопасности целекоксиба I (SUCCESS-I) показало повышенный риск инфаркта миокарда при приеме целекоксиба в дозе 100 мг два раза в день по сравнению с диклофенаком и напроксеном; но прием 200 мг два раза в день приводил к меньшему риску инфаркта миокарда по сравнению с диклофенаком и напроксеном. Nussmeier et al. (2005) показали в исследовании увеличение частоты сердечно-сосудистых событий при приеме парекоксиба и вальдекоксиба (по сравнению с плацебо) после операции аортокоронарного шунтирования.[26]
Возможные механизмы
Было высказано предположение, что избирательность ЦОГ-2 может вызвать дисбаланс простагландинов в сосудистой сети. Если бы это было объяснением повышенного риска сердечно-сосудистых заболеваний, то низкие дозы аспирина должны свести на нет этот эффект.[26][28] чего не было в процессе APPROVe.[28] Кроме того, неселективные ингибиторы ЦОГ также показали увеличение сердечно-сосудистых событий.[29]Другое возможное объяснение было изучено Li H. et al. (2008). Они показали, что в спонтанно гипертонические крысы (SHR) неизбирательный НПВП и коксибы производить окислительный стресс, на что указывает усиление сосудистой супероксид (O2−) содержание и повышенное перекись в плазме, что согласуется с повышенной экспрессией НАДФН-оксидазы, отмеченной при применении диклофенака и напроксена и, в меньшей степени, рофекоксиба и целекоксиба. Нитриты в плазме также снизился, что свидетельствует о снижении синтеза сосудистых оксид азота (НЕТ). Это снижение синтеза NO не является результатом снижения экспрессии эндотелиальный синтаза оксида азота (eNOS ) потому что выражение eNOS мРНК не было сокращено, и даже усиленный для некоторых продуктов. Снижение синтеза NO, скорее, можно объяснить потерей функции eNOS.[29] Для нормальной работы eNOS необходимо сформировать димер и иметь свой кофактор BH4, который является одним из самых сильнодействующих восстановителей природного происхождения. BH4 чувствителен к окисление к пероксинитрит (ONOO−), который образуется, когда NO реагирует с O2−, поэтому была выдвинута гипотеза, что истощение BH4 может возникать при чрезмерном окислительном стрессе (который может быть вызван НПВП) и, следовательно, быть причиной дисфункции eNOS. Эта дисфункция, называемая разобщением eNOS, вызывает выработку O2− eNOS, что приводит к усилению окислительного стресса, вызываемого eNOS.[30] В одном исследовании как селективные ингибиторы ЦОГ-2, так и неселективные НПВП вызывали окислительный стресс, с более сильным эффектом при использовании неселективных НПВП. Это могло соответствовать гипотезе о дисбалансе простациклин / тромбоксан. То есть, хотя неселективные НПВП вызывают больший окислительный стресс, они предотвращают агрегацию тромбоцитов, тогда как ингибиторы ЦОГ-2 снижают простациклин выработка и, следовательно, сердечно-сосудистый риск для неселективных НПВП не выше, чем для коксибов.[29]Среди других гипотез - повышение артериального давления, снижение выработки эпилипоксинов (обладающих противовоспалительным действием) и ингибирование ремоделирования сосудов при использовании селективных ингибиторов ЦОГ-2.[26]
Смотрите также
Рекомендации
- ^ а б c Marnett, L.J .; Калгуткар А. С. (1999). «Ингибиторы циклооксигеназы 2: открытие, селективность и будущее». Тенденции в фармакологических науках. 20 (11): 465–9. Дои:10.1016 / s0165-6147 (99) 01385-1. PMID 10542447.
- ^ Mardini, I.A .; Фитцджеральд, Г. А. (2001). «Селективные ингибиторы циклооксигеназы-2: растущий класс противовоспалительных препаратов». Молекулярные вмешательства. 1 (1): 30–8. PMID 14993336.
- ^ а б Marnett, L.J .; Калгуткар А.С. (1998). «Дизайн селективных ингибиторов циклооксигеназы-2 в качестве неульцерогенных противовоспалительных средств». Современное мнение в области химической биологии. 2 (4): 482–90. Дои:10.1016 / с 1367-5931 (98) 80124-5. PMID 9736921.
- ^ King, F. D., Ed. (2002). Принципы и практика медицинской химии. Кембридж, Королевское химическое общество.
- ^ а б c Цветок, Р. Дж. (2003). «Разработка ингибиторов ЦОГ2». Обзоры природы Drug Discovery. 2 (3): 179–91. Дои:10.1038 / nrd1034. PMID 12612644.
- ^ Dannhardt, G; Кифер, W (2001). «Ингибиторы циклооксигеназы - состояние и перспективы на будущее». Европейский журнал медицинской химии. 36 (2): 109–26. Дои:10.1016 / s0223-5234 (01) 01197-7. PMID 11311743.
- ^ FDA, Центр оценки и исследований лекарственных средств (2008 г.). «Одобренный FDA лекарственный препарат - Целебрекс». Проверено 18.10.2008 г., из [1]
- ^ а б FDA, Центр оценки и исследований лекарственных средств (2008 г.). «Одобренный FDA лекарственный препарат - Vioxx». Проверено 18.10.2008 г., из [2]
- ^ Лангрет, Роберт (23 июня 2003 г.). "Химический сапожник". Forbes.
- ^ "Доктор Джон Талли: лауреат Сент-Луиса 2001 г." (PDF). Химическая связь. Секция Сент-Луиса, Американское химическое общество. 52 (5): 2 мая 2001 г. Архивировано с оригинал (PDF) 15 апреля 2018 г.
- ^ а б Зарги, А; Rao, P.N .; Кнаус, Э. Э. (2007). «Разработка и синтез новых аналогов рофекоксиба в качестве селективных ингибиторов циклооксигеназы-2 (ЦОГ-2): замена метансульфонильного фармакофора на биоизостер N-ацетилсульфонамидо». Журнал фармации и фармацевтических наук. 10 (2): 159–67. PMID 17706175.
- ^ Маттиа, К; Колуцци, Ф (2005). «Ингибиторы ЦОГ-2: фармакологические данные и побочные эффекты». Минерва Анестезиологическая. 71 (7–8): 461–70. PMID 16012420.
- ^ Llorens, O; Perez, J. J .; Паломер, А; Маулеон, Д. (1999). «Структурные основы динамического механизма связывания лиганда с циклооксигеназой». Письма по биоорганической и медицинской химии. 9 (19): 2779–84. Дои:10.1016 / s0960-894x (99) 00481-3. PMID 10522690.
- ^ а б Michaux, C; Шарлье, С. (2004). «Структурный подход к ингибированию ЦОГ-2». Мини-обзоры по медицинской химии. 4 (6): 603–15. Дои:10.2174/1389557043403756. PMID 15279594.
- ^ Эрмонди, G; Caron, G; Лоуренс, Р. Лонго, Д. (2004). «Докинг-исследования изоферментных комплексов NSAID / COX-2 с использованием анализа контактной статистики». Журнал компьютерного молекулярного дизайна. 18 (11): 683–96. Дои:10.1007 / s10822-004-6258-1. PMID 15865061.
- ^ Уокер, М. С .; Kurumbail, R.G .; Kiefer, J. R .; Moreland, K. T .; Koboldt, C.M .; Isakson, P.C .; Зайберт, К; Герсе, Дж. К. (2001). «Трехступенчатый кинетический механизм селективного ингибирования циклооксигеназы-2 диарилгетероциклическими ингибиторами». Биохимический журнал. 357 (Pt 3): 709–18. Дои:10.1042 / bj3570709. ЧВК 1222000. PMID 11463341.
- ^ а б c d Берк А., Смит Э. и др. (2005). Глава 26: Анальгетики-жаропонижающие средства; фармакотерапия подагры. Фармакологические основы терапии. Л. Л. Брантон, Дж. С. Лазо и К. Л. Паркер, компании McGraw-Hill: 679-680 и 702-705.
- ^ Дэвис, Н. М .; McLachlan, A.J .; Day, R.O .; Уильямс, К. М. (2000). «Клиническая фармакокинетика и фармакодинамика целекоксиба: селективный ингибитор циклооксигеназы-2». Клиническая фармакокинетика.. 38 (3): 225–42. Дои:10.2165/00003088-200038030-00003. PMID 10749518.
- ^ а б Карим, А; Лоран, А; Слейтер, М. Э .; Кусс, М. Э .; Цянь, Дж; Crosby-Sessoms, S.L .; Хаббард, Р. К. (2001). «Фармакокинетическое исследование парекоксиба натрия внутримышечно у здоровых людей». Журнал клинической фармакологии. 41 (10): 1111–9. Дои:10.1177/00912700122012607. PMID 11583480.
- ^ Takemoto, J. K .; Reynolds, J. K .; Remsberg, C.M .; Вега-Вилла, К. Р .; Дэвис, Н. М. (2008). «Клинический фармакокинетический и фармакодинамический профиль эторикоксиба». Клиническая фармакокинетика.. 47 (11): 703–20. Дои:10.2165/00003088-200847110-00002. PMID 18840026.
- ^ Agrawal, N.G .; Porras, A. G .; Matthews, C. Z .; Rose, M.J .; Woolf, E.J .; Musser, B.J .; Dynder, A. L .; Mazina, K. E .; Лассетер, К. С .; Hunt, T. L .; Schwartz, J. I .; McCrea, J. B .; Готтесдинер, К. М. (2003). «Фармакокинетика однократных и многократных доз эторикоксиба, селективного ингибитора циклооксигеназы-2, у человека». Журнал клинической фармакологии. 43 (3): 268–76. Дои:10.1177/0091270003251122. PMID 12638395.
- ^ Mangold, J. B .; Гу, Н; Rodriguez, L.C .; Боннер, Дж; Диксон, Дж; Рордорф, С (2004). «Фармакокинетика и метаболизм люмиракоксиба у здоровых мужчин». Метаболизм и утилизация лекарств. 32 (5): 566–71. Дои:10.1124 / dmd.32.5.566. PMID 15100180.
- ^ Halpin, R.A .; Geer, L.A .; Zhang, K. E .; Маркс, Т. М .; Dean, D.C .; Jones, A.N .; Melillo, D; Досс, G; Вяс, К. П. (2000). «Поглощение, распределение, метаболизм и выведение рофекоксиба, мощного и селективного ингибитора циклооксигеназы-2, у крыс и собак». Метаболизм и утилизация лекарств. 28 (10): 1244–54. PMID 10997947.
- ^ Якш, Вт; Dejaco, C; Ширмер, М. (2008). «4 года после отмены рофекоксиба: что мы находимся сегодня?». Rheumatology International. 28 (12): 1187–95. Дои:10.1007 / s00296-008-0650-4. PMID 18663451.
- ^ а б c d Барон, Дж. А .; Sandler, R. S .; Bresalier, R. S .; Ланас, А; Morton, D.G .; Ридделл, Р. Iverson, E. R .; Демец Д. Л. (2008). «Сердечно-сосудистые события, связанные с рофекоксибом: окончательный анализ исследования APPROVe». Ланцет. 372 (9651): 1756–64. Дои:10.1016 / S0140-6736 (08) 61490-7. PMID 18922570.
- ^ а б c d е ж Салинас, G; Рангасетти, США; Урецкий, Б. Ф .; Бирнбаум, Y (2007). «История циклоксигеназы 2 (ЦОГ-2): пора объяснять, а не разгораться». Журнал сердечно-сосудистой фармакологии и терапии. 12 (2): 98–111. Дои:10.1177/1074248407301172. PMID 17562780.
- ^ а б «Архивная копия» (PDF). Архивировано из оригинал (PDF) 17 апреля 2012 г.. Получено 4 января 2015.CS1 maint: заархивированная копия как заголовок (связь)
- ^ а б Феррарио, К. М. (2008). «О селективных ингибиторах циклооксигеназы-2: у нас есть последнее слово?». Терапевтические достижения в области сердечно-сосудистых заболеваний. 2 (2): 75–8. Дои:10.1177/1753944708091000. PMID 19124410.
- ^ а б c Ли, Н; Hortmann, M; Дайбер, А; Эльзе, М; Остад, М. А .; Schwarz, P.M .; Сюй, Н; Ся, Н; Клещев, А.Л .; Mang, C; Warnholtz, A; Münzel, T; Фёрстерманн, У (2008). «Селективные по отношению к циклооксигеназе 2 и неселективные нестероидные противовоспалительные препараты вызывают окислительный стресс за счет активации сосудистых НАДФН-оксидаз». Журнал фармакологии и экспериментальной терапии. 326 (3): 745–53. Дои:10.1124 / jpet.108.139030. PMID 18550689.
- ^ Förstermann, U; Мюнцель, Т. (2006). «Эндотелиальная синтаза оксида азота при сосудистых заболеваниях: от чуда к угрозе». Тираж. 113 (13): 1708–14. Дои:10.1161 / CIRCULATIONAHA.105.602532. PMID 16585403.
