Бергаптен - Bergapten
 | |
 | |
| Имена | |
|---|---|
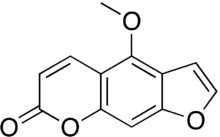
| Название ИЮПАК 4-метокси-7ЧАС-фуро [3,2-грамм] хромен-7-он | |
Другие имена
| |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.006.913 |
| Номер ЕС |
|
| КЕГГ | |
PubChem CID | |
| UNII | |
| Номер ООН | 1759 |
| |
| |
| Характеристики | |
| C12ЧАС8О4 | |
| Молярная масса | 216,192 г / моль |
| Фармакология | |
| D05BA03 (ВОЗ) | |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Бергаптен (5-метоксипсорален) представляет собой естественное органическое химическое соединение, вырабатываемое многими видами растений, особенно из семейства морковных. Apiaceae и семья цитрусовых Rutaceae. Например, бергаптен был извлечен из 24 видов рода Гераклеум в семействе Apiaceae.[1][2] В семействе Rutaceae различные Цитрусовые виды содержат значительное количество бергаптена,[3] особенно папеда Цитрусовая микранта, то бергамот апельсин (C. бергамия), и некоторые разновидности Лайм и Горький апельсин.
Бергаптен принадлежит к классу химических соединений, известных как фуранокумарины. В 1834 г. Кальбруннер выделил 5-метоксипсорален из эфирное масло бергамота,[4] отсюда и общее название «бергаптен». Это был первый фуранокумарин, который был выделен и идентифицирован.
Токсичность
Бергаптен является производным от псорален, исходное соединение семейства природных органических соединений, известных как линейные фуранокумарины (так называемые, поскольку они обладают линейной химической структурой). Некоторые линейные фуранокумарины, включая бергаптен, действуют как сильные фотосенсибилизаторы при местном применении на кожу.
Бергаптен часто встречается в растениях, связанных с фитофотодерматит,[5] потенциально серьезное воспаление кожи. Контакт с частями растений, содержащими бергаптен (и другие линейные фуранокумарины), с последующим воздействием ультрафиолетовый свет может привести к фитофотодерматиту. В частности, бергаптен является основным фототоксичный соединение, ответственное за Цитрусовые -индуцированный фитофотодермит.[3]
Бергаптен и другие линейные фуранокумарины вызывают потерю матричной активности для синтеза РНК. 5-метоксипсорален также известен своим мутагенный эффекты, а также его способность быть очень мощным средством для индукции хромосомные аберрации. При достаточно высокой концентрации наблюдалось полное митотическое ингибирование.[4]
Существует достаточно доказательств того, что бергаптен способствует развитию рака у животных, но таких доказательств канцерогенности у людей нет. Согласно Международное агентство по изучению рака, бергаптен это вероятно канцерогенное для человека.[6]
Медицинское использование
Бергаптен помогает коже поглощать больше света, а при пигментных заболеваниях, таких как витилиго (лейкодермия) и псориаз проходите лечение с использованием фуранокумаринов, часто в сочетании с воздействием солнца или солнечного излучения. У людей, которые легко обгорают, фуранокумарины могут также повышать устойчивость кожи к солнечному излучению.[4] Было показано, что бергаптен вызывает определенные кожные реакции для выравнивания осветления пигментации у пациентов с витилиго в зависимости от различных факторов, таких как восприимчивость субъекта, дозировка и влажность, но эффекты могут быть несовместимыми.[7]
При псориазе бергаптен ценится как пероральный фотохимиотерапия лечение из-за его эффективности и отсутствия фототоксических и лекарственно-нечувствительных реакций. Он действует как фотосенсибилизирующий препарат, который столь же эффективен или, при достаточно высокой дозировке, более эффективен, чем 8-метоксипсорален, в лечении псориазных поражений.[8] Было показано, что он является ценной альтернативой 8-метоксипсоралену из-за относительного отсутствия побочных эффектов во время лечения, таких как эритмия, зуд и тошнота.[9]
Бергаптен также считается потенциальным методом профилактики рака кожи, вызванного солнечным светом. Особое исследование показало, что загар, полученный с помощью бергаптена, имел меньше повреждений ДНК у людей.[10] Было показано, что бергаптен обладает противоопухолевым действием, например, благодаря его способности вызывать аутофагический процесс в клетках рака груди. Одно исследование показало, что это возможно благодаря повышающей регуляции Ген PTEN экспрессия в этих клетках рака груди.[11]
Бергаптен, наряду с другими фуранокумаринами, также участвует в Цитохром P450 торможение.[12]
Синтез

Бергаптен - это натуральное соединение, получаемое из таких растений, как инжир обыкновенный, но его также можно синтезировать. Большинство синтезов линейных фуранокумаринов включает начало с центральной ароматической единицы и добавление двух гетероциклических колец. Желательны альтернативные пути синтеза, чтобы избежать региохимических проблем и умеренных выходов. Описанный здесь синтез включает йод в качестве удаляемой группы для обеспечения региохимической целостности и конвергенции.[13] Как показано на диаграмме, исходным материалом был флороглюцин (соединение 1). Монометилирование проводили с последующей реакцией с этилпропиолатом в присутствии ZnCl.2 с получением 7-гидрокси-5-метоксикумарина (продукт 3, не показан) с выходом 68%. Затем положение 8 7-гидрокси-5-метоксикумарина защищали йодом, чтобы избежать образования угловатого фуранокумарина. Продукт 4 на диаграмме является результатом йодной защиты. Продукт 5 был результатом аллилирования продукта 4. Тетраоксид осмия и метрапериодат натрия использовали для окислительного расщепления O-аллильного производного на альдегидном продукте 7 через промежуточный диол (продукт 6, не показан). Циклизация альдегидного продукта 7 с использованием BF3-Et2О в тетра-н-Затем использовали бромид бутиламмония для построения фуранового кольца. Последним шагом было удаление йодозащитной группы с помощью Pd (OAc).2 в конечном итоге произвести бергаптен (продукт 9) с выходом 90%. Синтетический бергаптен был выделен в виде бесцветного соединения со свойствами, спектроскопически идентичными натуральному продукту.
Известное применение бергаптена - синтез Фраксинол.[14] Ключевой реакцией в этом синтезе является окисление фуранового кольца виснагина и бергаптена хромовой кислотой.[14]
Рекомендации
- ^ Нильсен, Б. Э. (1970). Кумарины зонтичных растений. Копенгаген: Королевская датская фармацевтическая школа. Цитируется Митчеллом и Рук (1979).
- ^ Митчелл, Джон; Ладья, Артур (1979). Ботаническая дерматология: растения и растительные продукты, вредные для кожи. Ванкувер: Гринграсс. С. 692–699.
- ^ а б Dugrand-Judek, Audray; Олри, Александр; Хен, Ален; Костантино, Жиль; Оллитро, Патрик; Froelicher, Янн; Бурго, Фредерик (ноябрь 2015 г.). "Распространение кумаринов и фуранокумаринов в Цитрусовые Виды близко совпадают Цитрусовые Филогения и отражение организации биосинтетических путей ». PLOS ONE. 10 (11): e0142757. Дои:10.1371 / journal.pone.0142757. ЧВК 4641707. PMID 26558757.
- ^ а б c Scott, B.R .; Pathak, M. A .; Мон, Г. Р. (1976). «Молекулярно-генетические основы реакций фурокумарина». Mutat Res. 39 (1): 29–74. Дои:10.1016/0165-1110(76)90012-9. PMID 13299.
- ^ Макговерн, Томас У .; Баркли, Теодор М. (2000). «Ботаническая дерматология». Электронный учебник дерматологии. Интернет-дерматологическое общество. РазделФитофотодерматит. Получено 29 ноября, 2018.
- ^ "Монографии по оценке канцерогенного риска химических веществ для человека". Женева: Всемирная организация здравоохранения, Международное агентство по изучению рака, 1972 г.-НАСТОЯЩЕЕ ВРЕМЯ. 1987. с. S7 66. Получено 4 января 2019.
- ^ «Побочные эффекты чая Эрл Грей».
- ^ Хонигсманн (октябрь 1979 г.). «5-Метоксипсорален (Бергаптен) в фотохимиотерапии псориаза». Британский журнал дерматологии. 101.
- ^ Танью, Адриан (февраль 1988 г.). «5-Метоксипсорален (Бергаптен) для фотохимиотерапии: биодоступность, фототоксичность и клиническая эффективность нового лекарственного препарата при псориазе». Журнал Американской академии дерматологии. 18.
- ^ Тиссеран, Роберт (2014). Безопасность эфирных масел. Черчилль Ливингстон.
- ^ Де Амицис, Франческа (2015). «Бергаптен стимулирует аутофагию за счет усиления экспрессии PTEN в клетках рака груди». Молекулярный рак. 14. Дои:10.1186 / s12943-015-0403-4. ЧВК 4498523. PMID 26148846.
- ^ Олдред, Элейн (2009). Справочник Хашека и Руссо по токсикологической патологии (третье издание). Черчилль Ливингстон.
- ^ Ода, Кадзуаки (июнь 2005 г.). «Эффективный синтез бергаптена». Гетероциклы. 65: 1985–1988. Дои:10.3987 / com-05-10451 - через ResearchGate.
- ^ а б Шенберг, Александр; Бадран, Насри; Старковский, Николай А. (1955). «Фуро-хромоны и -кумарины. XII. Синтез фраксинола из бергаптена и байкалеина из виснагина». Журнал Американского химического общества. 77 (20): 5390–5392. Дои:10.1021 / ja01625a055. ISSN 0002-7863.
