Ацетоуксусная кислота - Acetoacetic acid
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC 3-оксобутановая кислота[1] | |
| Другие имена Диуксусная кислота | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| DrugBank | |
| КЕГГ | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C4ЧАС6О3 | |
| Молярная масса | 102.089 г · моль−1 |
| Внешность | Бесцветная маслянистая жидкость |
| Температура плавления | 36,5 ° С (97,7 ° F, 309,6 К) |
| Точка кипения | Разлагается |
| Растворимый | |
| Растворимость в органических растворителях | Растворим в этиловый спирт, эфир |
| Кислотность (пKа) | 3.58 [2] |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
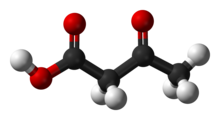
Ацетоуксусная кислота (также диуксусная кислота) является органическое соединение с формулой CH3COCH2COOH. Это самая простая бета-версиякетокислота и, как и другие члены этого класса, нестабилен. Метиловый и этиловый эфиры, которые довольно стабильны, производятся в промышленных масштабах в качестве предшественников красителей. Уксусная кислота - это слабая кислота.[3]
Биохимия
В типичных физиологических условиях ацетоуксусная кислота существует в виде сопряженное основание, ацетоацетат.
Ацетоацетат производится в митохондрии из печень из ацетоацетила коэнзим А (CoA). Во-первых, еще один ацетил группа добавляется из ацетил-КоА формировать 3-гидрокси-3-метилглутерил-КоА, то при этом теряется ацетил-КоА с образованием ацетоацетата. Первоначальный ацетоацетат может быть получен из последнего цикла в бета-окисление из жирная кислота, или он может быть синтезирован из двух молекул ацетил-КоА, катализируемый тиолаза.[4]:393
У млекопитающих ацетоацетат продуцируется в печени (вместе с двумя другими "кетоновые тела ") попадает в кровоток в качестве источника энергии в периоды голодание, упражнения или в результате сахарный диабет 1 типа.[5] Во-первых, группа КоА ферментативно переносится на нее из сукцинил КоА, превращая его обратно в ацетоацетил-КоА; затем он расщепляется тиолазой на две молекулы ацетил-КоА, которые затем попадают в цикл лимонной кислоты. Сердечная мышца и кора почек предпочитают ацетоацетат глюкозе. Мозг использует ацетоацетат, когда уровень глюкозы низкий из-за голодания или диабета.[4]:394
Синтез и свойства
Уксусная кислота может быть получена гидролизом дикетен. Его сложные эфиры получают аналогичным образом посредством реакции между дикетеном и спиртами,[3] и ацетоуксусная кислота может быть получена гидролизом этих соединений.[6]Как правило, ацетоуксусная кислота образуется при 0 ° C и сразу же используется на месте.[7] Разлагается при умеренной ставка к ацетон и углекислый газ:
- CH3C (O) CH2CO2H → CH3C (O) CH3 + CO2
Кислотная форма имеет период полураспада 140 минут при 37 ° C в воде, тогда как основная форма (анион) имеет период полураспада 130 часов. То есть реагирует примерно в 55 раз медленнее.[8]Это слабая кислота (как и большинство алкилкарбоновых кислот), с пKа 3,58.
Уксусная кислота выводит кето-енол таутомеризация, причем енольная форма частично стабилизируется за счет расширенной конъюгации и внутримолекулярной H-соединение. Равновесие сильно зависит от растворителя; при этом кетоформа преобладает в полярных растворителях (98% в воде), а енольная форма составляет 25-49% материала в неполярных растворителях.[9]
Приложения
Эфиры ацетоуксусной кислоты используются для ацетоацетилирование реакция, которая широко используется при производстве арилидные желтые и диарилид красители.[3] Хотя в этой реакции можно использовать сложные эфиры, дикетен также реагирует с спирты и амины к соответствующим производным ацетоуксусной кислоты в процессе, называемом ацетоацетилирование. Примером может служить реакция с 4-аминогруппой.индан:[10]

Обнаружение
Уксусная кислота измеряется в моче людей с диабетом, чтобы проверить: кетоацидоз[11] и для наблюдения за людьми на кетогенный или же низкоуглеводная диета,[12][13] Это делается с помощью щупов, покрытых нитропруссид или аналогичные реагенты. Цвет нитропруссида меняется с розового на фиолетовый в присутствии ацетоацетата, сопряженное основание ацетоуксусной кислоты, и изменение цвета оценивается на глаз. Тест не измеряет β-гидроксибутират, самый распространенный кетон в организме; во время лечения кетоацидоза β-гидроксибутират превращается в ацетоацетат, поэтому после начала лечения тест бесполезен[11] и может быть ложно заниженным при диагностике.[14]
Подобные тесты используются в молочные коровы проверить на кетоз.[15]
Смотрите также
Рекомендации
- ^ «Переднее дело». Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга). Кембридж: Королевское химическое общество. 2014. с. 748. Дои:10.1039 / 9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ Доусон, Р. М. С. и др., Данные для биохимических исследований, Oxford, Clarendon Press, 1959.
- ^ а б c Франц Дитрих Клинглер; Вольфганг Эбертц (2005). «Оксокарбоновые кислоты». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a18_313. ISBN 978-3527306732.
- ^ а б Люберт Страйер (1981). Биохимия (2-е изд.).
- ^ Страйер, Люберт (1995). Биохимия (Четвертое изд.). Нью-Йорк: W.H. Фримен и компания. С. 510–515, 581–613, 775–778. ISBN 0 7167 2009 4.
- ^ Роберт К. Крюгер (1952). «Кристаллическая уксусная кислота». Журнал Американского химического общества. 74 (21): 5536. Дои:10.1021 / ja01141a521.
- ^ Рейнольдс, Джордж А .; Ваналлан, Дж. А. (1952). «Метилглиоксаль-ω-фенилгидразон». Органический синтез. 32: 84. Дои:10.15227 / orgsyn.032.0084.; Коллективный объем, 4, п. 633
- ^ Hay, R.W .; Бонд, М.А. (1967). «Кинетика декарбоксилирования ацетоуксусной кислоты». Aust. J. Chem. 20 (9): 1823–8. Дои:10.1071 / CH9671823.
- ^ Гранде, Карен Д .; Розенфельд, Стюарт М. (1980). «Таутомерные равновесия в ацетоуксусной кислоте». Журнал органической химии. 45 (9): 1626–1628. Дои:10.1021 / jo01297a017. ISSN 0022-3263.
- ^ Киран Кумар Солингапурам Сай; Томас М. Гилберт; Дуглас А. Клумпп (2007). "Циклизации Кнорра и дистонические суперэлектрофилы". J. Org. Chem. 72 (25): 9761–9764. Дои:10.1021 / jo7013092. PMID 17999519.
- ^ а б Nyenwe, EA; Китабчи, А.Е. (апрель 2016 г.). «Эволюция диабетического кетоацидоза: обновление его этиологии, патогенеза и лечения». Метаболизм: клинический и экспериментальный. 65 (4): 507–21. Дои:10.1016 / j.metabol.2015.12.007. PMID 26975543.
- ^ Hartman, AL; Вининг, EP (январь 2007 г.). «Клинические аспекты кетогенной диеты». Эпилепсия. 48 (1): 31–42. Дои:10.1111 / j.1528-1167.2007.00914.x. PMID 17241206.
- ^ Сумитран, Прия; Пройетто, Джозеф (2008). «Кетогенные диеты для похудания: обзор их принципов, безопасности и эффективности». Исследования и клиническая практика ожирения. 2 (1): I – II. Дои:10.1016 / j.orcp.2007.11.003. PMID 24351673.
- ^ Мисра, S; Оливер, Н.С. (28 октября 2015 г.). «Диабетический кетоацидоз у взрослых» (PDF). BMJ (под ред. Клинических исследований). 351: h5660. Дои:10.1136 / bmj.h5660. HDL:10044/1/41091. PMID 26510442.
- ^ Tatone, EH; Гордон, JL; Хаббс, Дж; ЛеБлан, SJ; DeVries, TJ; Даффилд, TF (1 августа 2016 г.). «Систематический обзор и метаанализ диагностической точности тестов в местах оказания медицинской помощи для обнаружения гиперкетонемии у дойных коров». Профилактическая ветеринария. 130: 18–32. Дои:10.1016 / j.prevetmed.2016.06.002. PMID 27435643.

