Ромидепсин - Romidepsin
 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Истодакс |
| Другие имена | FK228; FR901228; Истодакс |
| MedlinePlus | a610005 |
| Данные лицензии |
|
| Беременность категория |
|
| Маршруты администрация | Внутривенное вливание |
| Код УВД | |
| Легальное положение | |
| Легальное положение |
|
| Фармакокинетический данные | |
| Биодоступность | Не применимо (только IV) |
| Связывание с белками | 92–94% |
| Метаболизм | Печеночный (главным образом CYP3A4 -опосредованно) |
| Устранение период полураспада | 3 часа |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| ChemSpider | |
| UNII | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.211.884 |
| Химические и физические данные | |
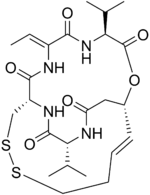
| Формула | C24ЧАС36N4О6S2 |
| Молярная масса | 540.69 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| | |
Ромидепсин, также известный как Истодакс, является противораковое средство используется в кожная Т-клеточная лимфома (CTCL) и другие периферические Т-клеточные лимфомы (PTCL). Ромидепсин - это натуральный продукт полученный из бактерии Chromobacterium violaceum, и работает, блокируя ферменты, известные как гистоновые деацетилазы, тем самым побуждая апоптоз.[1] Иногда его называют депсипептид, после класса молекул, к которому он принадлежит. Ромидепсин является торговой маркой и принадлежит компании Gloucester Pharmaceuticals, которая сейчас является частью Celgene.[2]
История
Впервые ромидепсин был опубликован в научной литературе в 1994 году группой исследователей из Fujisawa Pharmaceutical Company (ныне Астеллас Фарма ) в Цукуба, Япония, который изолировал его в культуре Chromobacterium violaceum из образца почвы, полученного в Префектура Ямагата.[3] Было обнаружено, что он практически не обладает антибактериальной активностью, но очень сильно цитотоксический против нескольких человеческих рак Сотовые линии, не влияя на нормальные клетки; исследования на мышах позже обнаружили его противоопухолевую активность in vivo также.[3]
Первый полный синтез ромидепсина была достигнута Гарвард исследователями и опубликовано в 1996 году.[4] это механизм действия было выяснено в 1998 году, когда исследователи из Фудзисавы и Токийский университет обнаружил, что это ингибитор гистондеацетилазы с эффектами, аналогичными эффектам трихостатин А.[5]
Клинические испытания
Фаза I Исследования ромидепсина, первоначально получившего кодовые обозначения FK228 и FR901228, начались в 1997 году.[6] Фаза II и исследования фазы III проводились по множеству показаний. Наиболее значимые результаты были получены при лечении кожная Т-клеточная лимфома (CTCL) и другие периферические Т-клеточные лимфомы (PTCL).[6]
В 2004 году ромидепсин получил Быстрый трек обозначение FDA для лечения кожной Т-клеточной лимфомы, и орфанный препарат статус от FDA и Европейское агентство по лекарствам по тому же показанию.[6]
FDA одобрило ромидепсин для лечения CTCL в ноябре 2009 г.[7] и одобрил ромидепсин для других периферические Т-клеточные лимфомы (PTCL) в июне 2011 г.[8]
Доклиническое исследование ВИЧ
В 2014, Патогены PLOS опубликовал исследование с участием ромидепсина в испытании, направленном на реактивацию латентного вируса ВИЧ с целью истощения резервуара ВИЧ. Латентно зараженный Т-клетки были разоблачены in vitro и ex vivo на ромидепсин, что приводит к увеличению определяемых уровней клеточно-ассоциированной РНК ВИЧ. В испытании также сравнивали эффект ромидепсина с другим ингибитором гистондеацетилазы, Вориностат [9]
Исследование аутизма на животной модели
Исследование с участием ромидепсина на животных, которое показало, что кратковременное лечение небольшими количествами ромидепсина может обратить вспять социальные дефициты на мышиной модели аутизма.[10]
Фармакодинамика
В фазе II исследования ромидепсина с участием пациентов с CTCL или PTCL были доказательства увеличения ацетилирования гистонов в мононуклеарных клетках периферической крови (PBMC) в течение 4–48 часов. Экспрессия гена ABCB1, маркера экспрессии гена, индуцированного ромидепсином, также была увеличена как в PBMC, так и в образцах биопсии опухоли. Повышенная экспрессия гена после повышенного ацетилирования гистонов является ожидаемым эффектом ингибитора HDAC. Повышенный гемоглобин F (еще один суррогатный маркер изменений экспрессии генов в результате ингибирования HDAC) также был обнаружен в крови после введения ромидепсина, а стойкое ацетилирование гистонов обратно связано с клиренсом лекарства и напрямую связано с ответом пациента на терапию.[11]
Дозировка и администрирование
Утвержденная доза ромидепсина как для CTCL, так и для PTCL составляет четырехчасовую внутривенную дозу. администрация 14 мг / м2 в дни 1, 8 и 15 28-дневного цикла лечения.[12] Этот цикл следует повторять до тех пор, пока пациент продолжает получать пользу и переносит терапию. У некоторых пациентов с высокой степенью токсичности возможно снижение дозы до 10 мг / м2.
Фармакокинетика
В исследованиях с участием пациентов с запущенными формами рака ромидепсин демонстрировал линейную фармакокинетику в диапазоне доз от 1,0 до 24,9 мг / м2 при внутривенном введении в течение четырех часов.[13] Возраст, раса, пол, почечная недостаточность от легкой до тяжелой, а также от легкой до умеренной почечной недостаточности не влияли на фармакокинетику ромидепсина. После повторного приема не наблюдалось накопления концентрации в плазме.[14]
Механизм действия
Ромидепсин действует как пролекарство с дисульфидная связь проходящий снижение внутри клетки, чтобы высвободить цинк-связывающий тиол.[3][15][16] Тиол связывается с атомом цинка в кармане связывания Zn-зависимого гистоновая деацетилаза чтобы заблокировать его деятельность. Таким образом, это Ингибитор HDAC. Много Ингибиторы HDAC являются потенциальными методами лечения рака благодаря способности эпигенетически восстанавливать нормальную экспрессию генов-супрессоров опухоли, что может привести к остановке клеточного цикла, дифференцировке и апоптоз.[17]
Побочные эффекты
Использование ромидепсина всегда связано с: побочные эффекты.[18] В клинических испытаниях наиболее частыми были тошнота и рвота, усталость, инфекционное заболевание, потеря аппетита и заболевания крови (в том числе анемия, тромбоцитопения, и лейкопения ). Это также было связано с инфекциями и метаболическими нарушениями (такими как аномальные электролит уровни), кожные реакции, измененное восприятие вкуса, и изменения в сердечная электрическая проводимость.[18]
Рекомендации
- ^ «Ромидепсин». Национальный институт рака. Получено 2009-09-11.
- ^ «Ромидепсин». Gloucester Pharmaceuticals. Получено 2009-09-11.[постоянная мертвая ссылка ]
- ^ а б c Уэда Х., Накадзима Х., Хори Й. и др. (Март 1994). "FR901228, новый противоопухолевый бициклический депсипептид, производимый Chromobacterium violaceum № 968. I. Таксономия, ферментация, выделение, физико-химические и биологические свойства, противоопухолевая активность ». Журнал антибиотиков. 47 (3): 301–10. Дои:10.7164 / антибиотики.47.301. PMID 7513682.
- ^ Ли К.В., Ву Дж., Син В., Саймон Дж. А. (июль 1996 г.). «Полный синтез противоопухолевого депсипептида FR-901,228». Журнал Американского химического общества. 118 (30): 7237–8. Дои:10.1021 / ja9613724.
- ^ Накадзима Х., Ким И.Б., Терано Х., Йошида М., Хориноути С. (май 1998 г.). «FR901228, мощный противоопухолевый антибиотик, представляет собой новый ингибитор гистондеацетилазы». Экспериментальные исследования клеток. 241 (1): 126–33. Дои:10.1006 / excr.1998.4027. PMID 9633520.
- ^ а б c Масуока Ю., Шиндох Н., Инамура Н. (2008). «Ингибиторы гистон-деацетилазы из микроорганизмов: опыт Astellas». В Petersen F, Amstutz R (ред.). Природные соединения как лекарства. 2. Базель: Биркхойзер. С. 335–59. ISBN 978-3-7643-8594-1. Проверено 8 ноября 2009 г. через Поиск книг Google.
- ^ http://chembl.blogspot.com/2009/11/new-drug-approvals-pt-xxiii-romidepsin.html
- ^ http://www.accessdata.fda.gov/scripts/cder/drugsatfda/index.cfm?fuseaction=Reports.MonthlyApprovalsAll
- ^ Wei, D; и другие. (2014). «Ингибитор гистоновой деацетилазы ромидепсин индуцирует экспрессию ВИЧ в Т-лимфоцитах CD4 у пациентов, проходящих супрессивную антиретровирусную терапию, в концентрациях, достигаемых клиническим дозированием». PLoS Pathog. 10 (4): e1004071. Дои:10.1371 / journal.ppat.1004071. ЧВК 3983056. PMID 24722454.
- ^ Цинь, Луйе; Ма, Кайджи; Ван, Цзы-Цзюнь; Ху, Цзыхуа; Матас, Эммануэль; Вэй, Цзин; Ян, Чжэнь (2018). «Социальный дефицит в моделях аутизма на мышах с дефицитом Shank3 устраняется ингибированием гистондеацетилазы (HDAC)». Природа Неврологии. 21 (4): 564. Дои:10.1038 / s41593-018-0110-8. ЧВК 5876144. PMID 29531362.
- ^ Bates, Susan E .; Чжан, Чжижун; Стедман, Кеннет; Обрзут, Томаш; Лученко Виктория; Фрай, Робин; Роби, Роберт В .; Тернер, Мария; Гарднер, Эрин Р. (январь 2010 г.). «Лабораторные корреляты для фазы II исследования ромидепсина при кожной и периферической Т-клеточной лимфоме». Британский журнал гематологии. 148 (2): 256–267. Дои:10.1111 / j.1365-2141.2009.07954.x. ISSN 0007-1048. ЧВК 2838427. PMID 19874311.
- ^ Накадзима, Хиденори; Ким, Янг Бэ; Терано, Хироши; Ёсида, Минору; Хориноути, Суэхару (май 1998 г.). «FR901228, мощный противоопухолевый антибиотик, представляет собой новый ингибитор гистондеацетилазы». Экспериментальные исследования клеток. 241 (1): 126–133. Дои:10.1006 / excr.1998.4027. ISSN 0014-4827. PMID 9633520.
- ^ Брэднер, Джеймс Э; Уэст, Натан; Grachan, Melissa L; Гринберг, Эдвард Ф; Хаггарти, Стивен Дж; Варнов, Тэнди; Мазичек, Ральф (07.02.2010). «Химическая филогенетика гистондеацетилаз». Природа Химическая Биология. 6 (3): 238–243. Дои:10.1038 / nchembio.313. ISSN 1552-4450. ЧВК 2822059. PMID 20139990.
- ^ Накадзима, Хиденори; Ким, Янг Бэ; Терано, Хироши; Ёсида, Минору; Хориноути, Суэхару (май 1998 г.). «FR901228, мощный противоопухолевый антибиотик, представляет собой новый ингибитор гистондеацетилазы». Экспериментальные исследования клеток. 241 (1): 126–133. Дои:10.1006 / excr.1998.4027. ISSN 0014-4827. PMID 9633520.
- ^ Shigematsu, N .; Ueda, H .; Takase, S .; Tanaka, H .; Ямамото, К .; Тада, Т. (1994). «FR901228, новый противоопухолевый бициклический депсипептид, продуцируемый Chromobacterium violaceum № 968. II. Определение структуры». J. Antibiot. 47 (3): 311–314. Дои:10.7164 / антибиотики.47.311. PMID 8175483.
- ^ Ueda, H .; Manda, T .; Matsumoto, S .; Мукумото, S .; Nishigaki, F .; Кавамура, I .; Шимомура, К. (1994). «FR901228, новый противоопухолевый бициклический депсипептид, продуцируемый Chromobacterium violaceum № 968. III. Противоопухолевое действие на экспериментальные опухоли у мышей». J. Antibiot. 47 (3): 315–323. Дои:10.7164 / антибиотики.47.315. PMID 8175484.
- ^ Грешок, Томас Дж .; Johns, Deidre M .; Ногучи, Ясуо; Уильямс, Роберт М. (2008). «Улучшенный общий синтез мощного ингибитора HDAC FK228 (FR-901228)». Органические буквы. 10 (4): 613–616. Дои:10.1021 / ol702957z. ЧВК 3097137. PMID 18205373.
- ^ а б [Авторы не указаны] (октябрь 2014 г.). «Информация на этикетке ISTODEX (обновлено до октября 2014 г.)» (PDF). Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США.
